МИНОБРНАУКИ РОССИИ
Федеральное государственное бюджетное образовательное учреждение
высшего образования
«Хакасский государственный университет им. Н.Ф. Катанова»
Институт естественных наук и математики
Кафедра геоэкологии и химии
Направление подготовки: 44.03.05. Педагогическое образование с двумя профилями подготовки: Химия, Биология
РЕФЕРАТ
«Химические реакции»
Выполняла:
Соловьева Кристина Валерьевна
4 курс, группа ХБ-41
Абакан, 2025
Оглавление
ВВЕДЕНИЕ 3
Учебный материал 5
Библиографический список 20
ВВЕДЕНИЕ
На сегодняшний день изучено более двух миллионов различных химических реакций, что свидетельствует о колоссальном разнообразии химических превращений. Исследования в области химической кинетики и термодинамики продолжают открывать новые закономерности протекания реакций и возможности их практического применения.
Цель: данной работы является комплексное изучение химических реакций, их классификации и особенностей протекания.
Актуальность изучения химических реакций обусловлена их повсеместным распространением и значимостью для развития различных отраслей науки и техники. Понимание механизмов химических превращений позволяет не только объяснять природные явления, но и создавать новые материалы, разрабатывать экологически безопасные технологии, совершенствовать методы получения необходимых веществ.
Современные направления исследований охватывают широкий спектр областей. Квантовая химия позволяет моделировать химические реакции на атомном уровне, открывая новые горизонты понимания механизмов превращений. Нанотехнологии предоставляют уникальные возможности для управления химическими процессами на молекулярном уровне. Зелёная химия активно развивается в направлении создания экологически безопасных реакций и процессов. Биохимия исследует сложные химические процессы, протекающие в живых организмах, а катализ совершенствует методы ускорения химических реакций.
Значительный прогресс, достигнут в области технологических достижений. Современное оборудование включает высокоточное спектральное оборудование, передовые методы компьютерного моделирования, наноразмерные датчики и системы автоматизированного контроля. Эти инструменты позволяют проводить исследования с беспрецедентной точностью и скоростью.
Особое внимание в современных исследованиях уделяется разработке новых материалов с заданными свойствами, созданию энергоэффективных процессов, экологически чистых технологий и лекарственных препаратов нового поколения. Междисциплинарный подход объединяет физику, биологию, математику, информатику и экологию, что позволяет решать сложные научные задачи на стыке различных областей знания.
Практическое применение полученных знаний находит отражение в промышленном производстве, медицинской диагностике, экологическом мониторинге, энергетических технологиях и создании новых материалов. Исследования химических реакций становятся ключевым фактором технологического прогресса и устойчивого развития общества.
Учебный материал
Химические реакции (от лат. реакция – противодействие, отпор) – это ответное действие других веществ на воздействие других веществ и физических факторов (температура, давление, излучения и др.)
Эволюция в природе была бы невозможна без химических реакций. В открытом космосе присутствуют преимущественно атомы водорода (H) и гелия (He). Это обусловлено отсутствием условий для химических взаимодействий.
На Земле ситуация кардинально отличается. Здесь многообразие химических элементов позволяет им вступать в разнообразные реакции. Богатство природы напрямую связано с количеством и качеством химических процессов. Переход от неорганических соединений к живым организмам стал возможен благодаря химическим реакциям. Человек также является своего рода мини-фабрикой, где происходят как простые, так и сложные химические реакции синтеза и расщепления веществ. Эффективность этой живой системы поражает воображение.
Химические реакции отличаются от физических процессов и ядерных превращений. В физических явлениях состав веществ не меняется, они могут только менять форму или агрегатное состояние (например, вода в пар или лёд). В химических реакциях образуются новые вещества из-за изменений в электронной оболочке атомов, в ядерных — изменяются ядра атомов и возникают атомы новых элементов.
Основные типы химических реакций
Реакция соединения — это процесс, при котором два или более вещества объединяются, образуя одно сложное вещество.
Примером такой реакции является:
Fe + S = FeS
Реакция разложения — это процесс, в ходе которого одно сложное вещество распадается на несколько простых.
Пример такой реакции:
CaCO₃ = CaO + CO₂
Реакция замещения — это взаимодействие между простым и сложным веществами, при котором атомы простого вещества замещают атомы одного из элементов в составе сложного вещества.
Пример данной реакции:
Zn + 2HCL = ZnCl₂ + H₂
Реакция обмена — это процесс, при котором два сложных вещества обмениваются своими составными частями, в результате чего образуются два новых сложных вещества.
Пример такой реакции:
MgO + H₂SO₄ = MgSO₄ + H₂O.

Классификация химических реакций
Химические реакции классифицируют по агрегатному состоянию, изменению степеней окисления, тепловому эффекту, направлению протекания и наличию катализаторов.
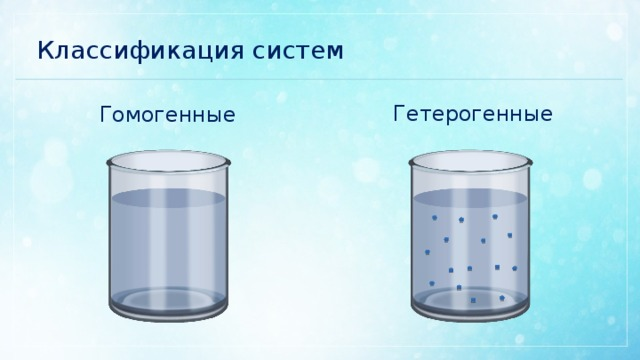
По агрегатному состоянию реагирующих веществ
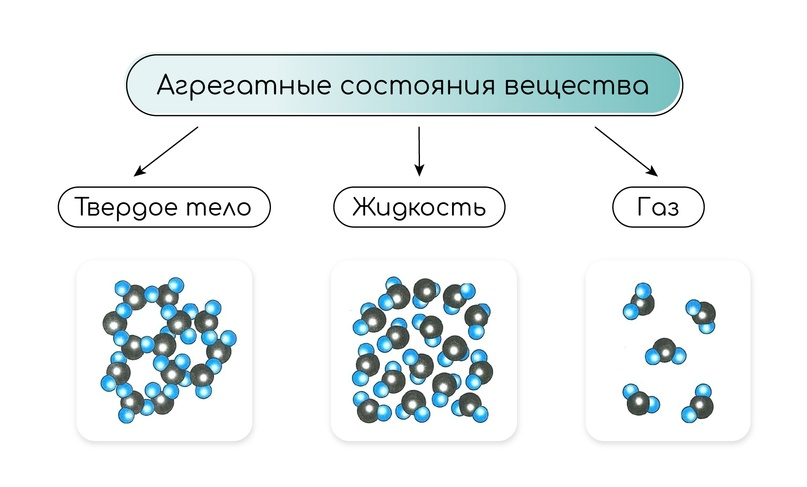
В зависимости от физического состояния реагентов различают два типа реакций. Гомогенные реакции протекают в пределах одной фазы, когда все участники реакции находятся в одинаковом агрегатном состоянии. Примером служит реакция в растворе:
HCl+NaOH→NaCl+H3O
Гетерогенные реакции происходят на границе раздела фаз, когда реагенты находятся в разных агрегатных состояниях. Типичный пример — взаимодействие твёрдого вещества с газом:
C+O3→CO3
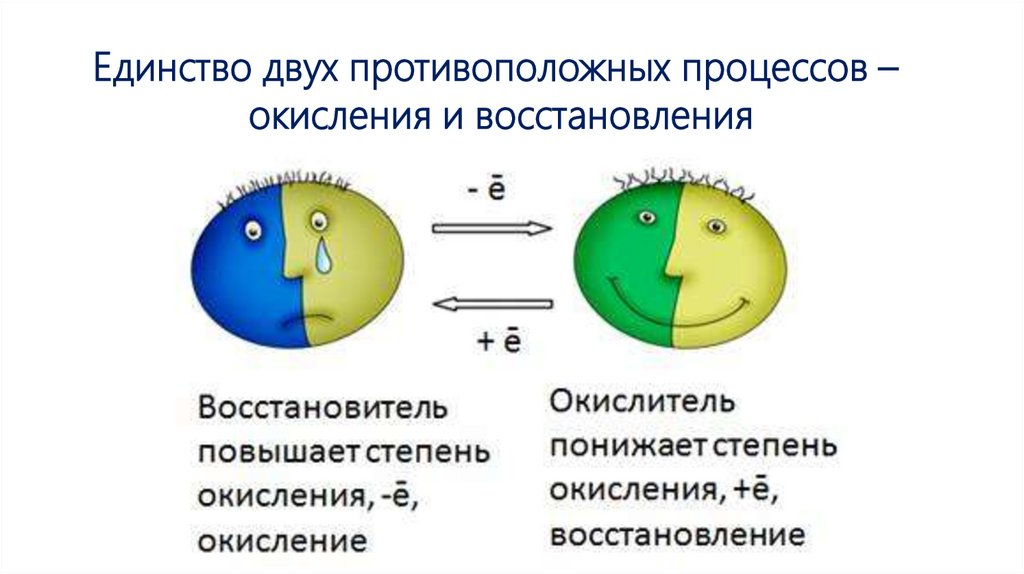
По изменению степеней окисления
Окислительно-восстановительные реакции характеризуются переходом электронов между атомами. При этом окисление представляет собой процесс отдачи электронов, сопровождающийся повышением степени окисления, а восстановление — процесс присоединения электронов, приводящий к понижению степени окисления.
В качестве примера можно привести реакцию:
Fe+CuSO6→FeSO6+Cu
где железо выступает в роли восстановителя (отдаёт электроны), а медь —окислителя (принимает электроны).
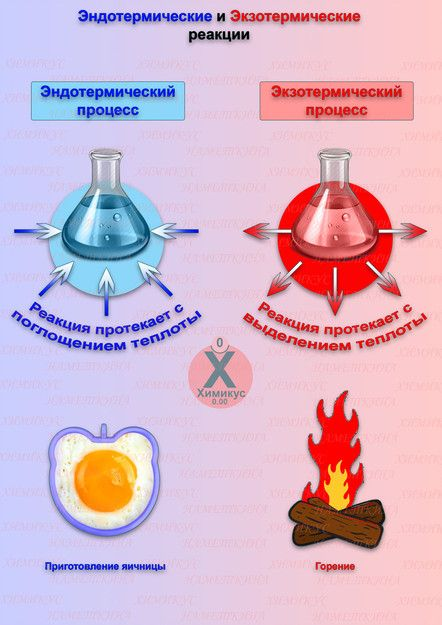
По тепловому эффекту
По тепловому эффекту реакции делятся на два основных типа. Экзотермические реакции сопровождаются выделением теплоты, например:
CH6+2O3→CO3+2H3O+Q
Эндотермические реакции протекают с поглощением теплоты:
CaCO5→CaO+CO2−Q
По направлению протекания
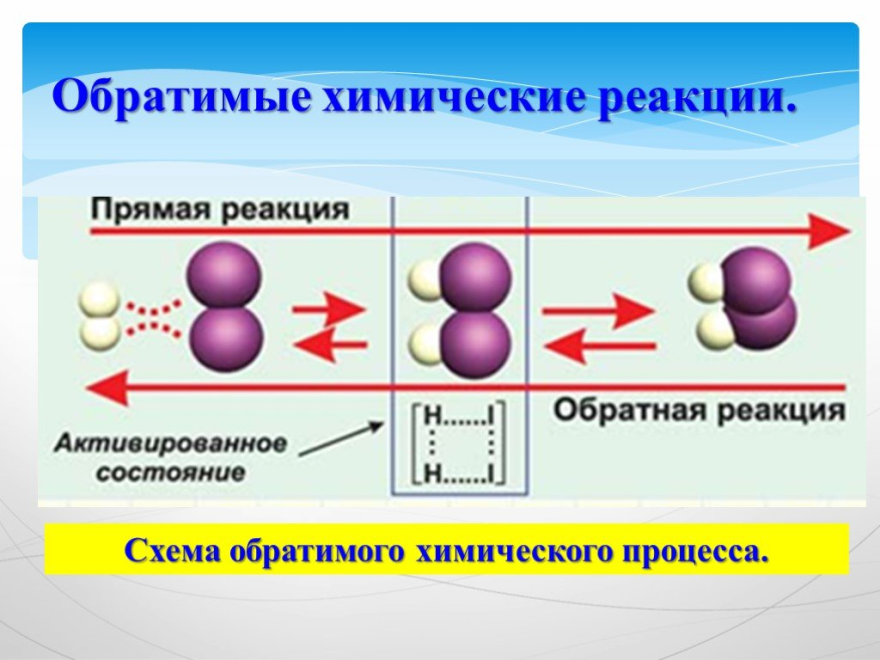
По направлению протекания различают обратимые реакции, способные протекать в обоих направлениях одновременно:
H3+I3⇌2HI
и необратимые реакции, идущие только в одном направлении до полного расходования реагентов:
2Mg+O3→2MgO
По использованию катализаторов
В зависимости от наличия катализаторов, химические реакции делятся на каталитические и некаталитические. В каталитических реакциях участвуют вещества-катализаторы, которые ускоряют процесс, но сами при этом не расходуются. В уравнениях таких реакций формула катализатора указывается над знаком равенства. Некаталитические реакции происходят без использования катализаторов.
Признаки химических реакций
Химические реакции приводят к превращению одних веществ в другие, что сопровождается изменением их свойств. Эти изменения служат признаками химических реакций. Среди них можно выделить:
Искрение и выделение или поглощение тепла. Горение магния сопровождается ярким светом и выделением значительного количества тепла. Это один из наиболее очевидных признаков химической реакции.
Выделение газа. При нагревании порошка малахита в пробирке происходит образование углекислого газа, воды и оксида меди CuO. Аналогично, при взаимодействии уксуса с содой также выделяется газ.
Образование или растворение осадка. Смешивание известковой воды и раствора соды приводит к образованию белого осадка, который растворяется в уксусе.
Изменение цвета и запаха. При горении спички выделяется специфический запах, изменяется цвет пламени и образуется тепло. Добавление йода к крахмалу вызывает появление характерного синего окрашивания.
Поглощение тепла. Некоторые химические реакции поглощают тепло из окружающей среды, что проявляется в охлаждении реакционной смеси.
Изменение агрегатного состояния. Вещества могут переходить из одного состояния в другое: например, твердое вещество может превратиться в газ или жидкость.
Выделение энергии в других формах. Помимо тепла и света, химические реакции могут сопровождаться выделением электрической энергии, как в гальванических элементах.
Изменение физических свойств. Могут изменяться такие характеристики, как плотность, вязкость и электропроводность веществ.
Образование новых соединений. Формируются вещества с новыми химическими свойствами, которые можно обнаружить с помощью качественных реакций.
Скорость химической реакции
Скорость химической реакции представляет собой ключевое понятие химической кинетики и катализа, которое позволяет количественно оценивать протекание химических процессов. Это величина, показывающая изменение концентрации исходных веществ или продуктов реакции за единицу времени.
Теоретические основы
Скорость реакции измеряется изменением концентраций реагирующих веществ в единицу времени. В химической кинетике различают два основных типа реакций:
Гомогенные реакции — протекают в однородной среде
Гетерогенные реакции — протекают на границе раздела фаз
Формулы расчёта скорости
Для гомогенных реакций скорость определяется по формуле:
υ=Δt/ΔC,
где υ — скорость реакции, ΔC — изменение концентрации, Δt — изменение времени.
Для гетерогенных реакций используется формула:
υ=S⋅Δt/Δν,
где Δν — изменение количества вещества, S — площадь реакционной поверхности.
Закон действующих масс
Этот фундаментальный закон устанавливает, что скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ:
v=k⋅[A]x⋅[B]y,
где k — константа скорости, [A] и [B] — концентрации веществ, x и y — порядки реакции.

Факторы, влияющие на скорость реакции
Концентрация реагентов играет первостепенную роль. При увеличении концентрации скорость реакции возрастает согласно закону действующих масс.
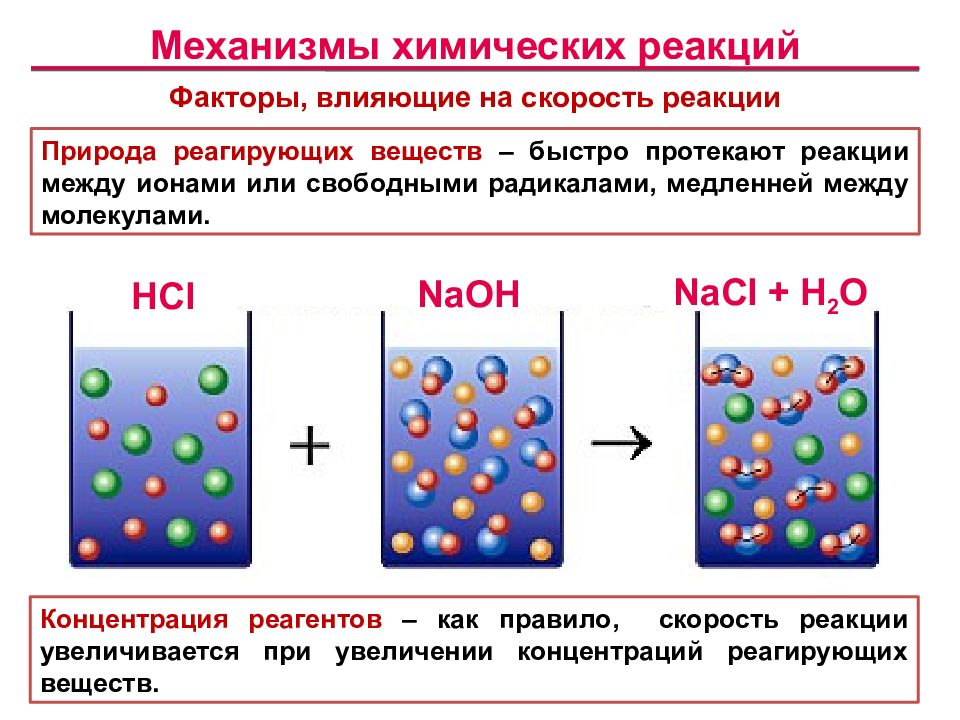
Природа веществ определяет характер взаимодействия. Активные вещества реагируют быстрее. Например, щелочные металлы взаимодействуют с водой с разной скоростью: калий быстрее натрия, а литий — медленнее.
Температурный фактор влияет существенно. По правилу Вант-Гоффа при повышении температуры на 10°C скорость реакции возрастает в 2–4 раза. Математически это выражается формулой:
υ2=υ1⋅γ^10/T2−T1
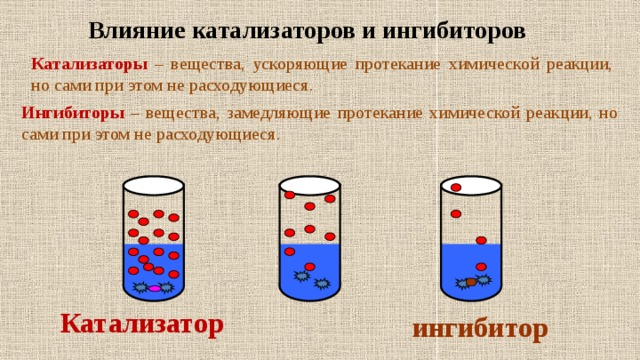
Катализаторы и ингибиторы способны значительно изменять скорость реакции. Катализаторы ускоряют процесс, не расходуясь, а ингибиторы замедляют его.
Давление оказывает влияние на реакции с участием газов, увеличивая скорость при повышении давления.
Площадь поверхности важна для гетерогенных реакций, так как увеличение площади контакта реагентов ускоряет процесс.
Практическое значение
Понимание скорости химических реакций имеет критическое значение для:
Оптимизации промышленных процессов
Контроля химических производств
Разработки новых материалов
Понимания биохимических процессов
Управления технологическими процессами
Примеры влияния факторов
Природа веществ: водород реагирует с кислородом взрывообразно, азот с кислородом — только при высоких температурах
Концентрация: увеличение концентрации кислоты ускоряет растворение металла
Температура: продукты портятся быстрее при комнатной температуре, чем в холодильнике
Катализаторы: синтез аммиака практически не идёт без катализатора
Изучение скорости реакций позволяет:
Прогнозировать длительность процессов
Рассчитывать производительность оборудования
Определять оптимальные условия проведения реакций
Управлять химическими процессами
Создавать новые технологии
В химической промышленности от скорости реакции зависит проектирование аппаратов, их размеры, производительность и качество продукции. Это делает изучение скорости реакций важнейшим направлением современной химии, без которого невозможно развитие многих технологических процессов.
Значение химических реакций в природе и жизни человека
Фундаментальное значение
Химические реакции являются основой существования всего живого на Земле. Они лежат в основе развития природы и эволюции живых организмов, без них невозможно представить формирование и развитие нашей планеты. Именно благодаря этим процессам стало возможным появление и развитие жизни во всех её проявлениях.
Промышленное применение
В сфере промышленного производства химические реакции обеспечивают:
Создание современных удобрений для повышения урожайности сельского хозяйства
Производство синтетических материалов, включая различные виды пластмасс и волокон
Разработку и изготовление лекарственных препаратов
Получение новых видов топлива для различных отраслей промышленности
Бытовое использование
В повседневной жизни химические реакции окружают нас постоянно:
При приготовлении пищи происходит изменение структуры продуктов
В процессах стирки и уборки осуществляется очищение поверхностей
При хранении продуктов применяются различные способы консервации
В сфере личной гигиены используются специальные средства ухода
Биологическая роль
Жизнедеятельность организмов полностью зависит от химических реакций:
Пищеварение и усвоение питательных веществ
Процесс дыхания и газообмена
Рост и развитие клеток
Нервная деятельность и мышление
Репродуктивные процессы
Научная деятельность
Современные исследования активно используют химические реакции в различных областях:
Криминалистика применяет их для анализа следов преступлений
Археология использует для датировки артефактов
Астрономия изучает состав космических объектов
Медицина разрабатывает новые лекарственные препараты
Экология анализирует уровень загрязнений
Природные явления
Естественные процессы в природе основаны на химических реакциях:
Фотосинтез обеспечивает образование органических веществ
Круговорот веществ поддерживает баланс экосистем
Формирование горных пород происходит благодаря химическим превращениям
Погодные явления связаны с химическими процессами
Геологические изменения обусловлены химическими реакциями
Технологический прогресс
Инновационное развитие человечества благодаря химическим реакциям:
Создание материалов с заданными характеристиками
Разработка энергосберегающих технологий
Внедрение экологически чистых производств
Развитие нанотехнологий
Прогресс в медицинской сфере
Практическая значимость
Современные возможности управления химическими процессами позволяют:
Производить необходимые вещества в промышленных масштабах
Контролировать качество выпускаемой продукции
Оптимизировать производственные процессы
Создавать материалы с улучшенными характеристиками
Решать экологические проблемы
В заключение следует отметить, что химические реакции являются фундаментальной основой существования природы и развития цивилизации. Они определяют развитие живых организмов, функционирование экосистем, технологический прогресс и качество жизни человека. Понимание и управление химическими процессами открывает новые возможности для развития науки, промышленности и сохранения экологического баланса планеты. Без этих знаний невозможно представить дальнейшее развитие человечества и решение глобальных проблем современности.
Библиографический список
1. Левицкий М. М. Увлекательная химия. Просто о сложном, забавно о серьезном / М. М. Левицкий. — Москва : АСТ: Астрель, 2008. — 416 с.
2. Френкель Е. Н. Химия. Самоучитель / Е. Н. Френкель. — Москва : АСТ, 2016. — 542 с.
3. Сиборг Г. Химия. Курс для средней школы / Г. Сиборг. — Москва : Мир, 1972.
4. Ленинджер А. Основы биохимии : в 3 т. / А. Ленинджер. — Москва : Мир, 1985.
5. Аликберова Л. Ю. Полезная химия: задачи и истории / Л. Ю. Аликберова, Н. С. Рукк. — 3-е изд. — Москва : Дрофа, 2008. — 192 с.
6. Рудзитис Г. Е. Химия. 8 класс : учеб. для общеобразоват. организаций / Г. Е. Рудзитис, Ф. Г. Фельдман. — 7-е изд. — Москва : Просвещение, 2023. — 207 с.
Приложение
1. Химическая реакция — это…
а) Процесс изменения агрегатного состояния вещества;
б) Превращение одних веществ в другие с образованием новых веществ;
в) Изменение формы тела;
г) Физическое явление;
2. Признак, НЕ являющийся показателем химической реакции…
а) Выделение газа;
б) Изменение цвета вещества;
в) Изменение формы предмета;
г) Образование осадка;
3. При химической реакции на уровне атомов происходит…
а) Изменяется состав ядер атомов;
б) Перераспределяются электроны и ядра;
в) Изменяется общее число ядер атомов;
г) Образуются атомы новых элементов;
4. Для начала большинства химических реакций необходимы условия….
а) Только смешивание веществ;
б) Только нагревание;
в) Сочетание нескольких факторов (температура, смешивание, катализатор);
г) Только освещение;
5. Эндотермическая реакция – это …
а) Реакция с выделением тепла;
б) Реакция с поглощением тепла;
в) Реакция без теплового эффекта;
г) Реакция только при высокой температуре;
6. Проходит взаимодействии металла с кислотой, такой тип реакции называется…
а) Реакция соединения;
б) Реакция разложения;
в) Реакция замещения;
г) Реакция обмена;
7. Катализатор – это…
а) Вещество, которое расходуется в ходе реакции;
б) Вещество, которое образуется в результате реакции;
в) Вещество, которое ускоряет реакцию, не входя в состав продуктов;
г) Вещество, которое замедляет реакцию;
8. Условия, которые НЕ являются обязательными для протекания химической реакции – это…
а) Контакт реагирующих веществ;
б) Определённая температура;
в) Изменение агрегатного состояния;
г) Наличие энергии активации;
9. Обратимая химическая реакция – это …
а) Реакция, идущая только в одном направлении;
б) Реакция, идущая как в прямом, так и в обратном направлении;
в) Реакция, протекающая только при высокой температуре;
г) Реакция, протекающая только в присутствии катализатора;
10. НЕ зависит скорость химической реакции …..
а) От природы реагирующих веществ;
б) От площади соприкосновения реагирующих веществ;
в) От цвета реакционного сосуда;
г) От концентрации реагирующих веществ;
Правильные ответы:
1-б, 2-в, 3-б, 4-в, 5-б, 6-в, 7-в, 8-в, 9-б, 10-в
Тест Онлайн: https://forms.yandex.ru/u/68efadb0f47e7318fda2a321


























