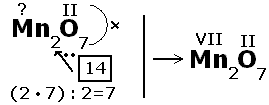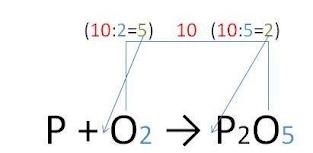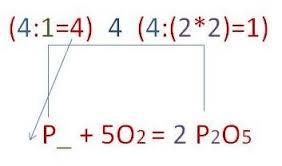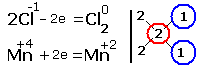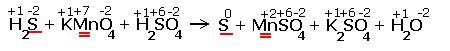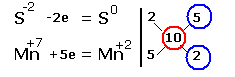Алгоритмы составления химических формул и уравнений химических реакций.
Валентность
Составление формул по валентности
|
Алгоритм решения
|
Пример
|
|
1. Запишите символы элементов (согласно ряду электроотрицательности)
|
Аl О
|
|
2. Запишите валентность элементов (по периодической системе)
|
III II
Аl О
|
|
3. Найдите наименьшее общее кратное (нок) между числовыми значениями валентности
|
6
III II
Аl О
НКО =6
|
|
4. Найдите соотношение между атомами элементов (деля НОК на соответствующую валентность). Полученные значения являются индексами
|
6
III II
Аl О
6 : 3=2
6 : 2= 3 →2:3
|
|
5. Запишите формулы веществ
|
Аl2 О3
|
Определение валентности по формуле
|
Алгоритм решения
|
Пример
|
|
1. Запишите формулу вещества
|
Р2 О5
|
|
2. Обозначьте известную валентность элемента
|
II
Р2 О5
|
|
3. Найдите наименьшее общее кратное (нок) между числовыми значениями валентности
|
10
II
Р2 О5
НОК =10
|
|
4. Поделите наименьшее общее кратное на количество атомов другого элемента. Полученный ответ и является искомой валентностью
|
10
V II
Р2 О5
10: 2=5
|
|
5. Сделайте проверку перемножьте валентность на индекс каждой части формулы. Их производные должны быть равны
|
V II
Р2 О5
10 = 10
|
Степень окисления
1.Элемент в простом веществе имеет нулевую степень окисления. 2.Все металлы имеют положительную степень окисления. 3. Водород имеет в соединениях степень окисления (+1), исключая гидриды ( соединения водорода с металлами главной подгруппы первой, второй групп, степень окисления -1, например Na+H- ); 5.Кислород имеет степень окисления (-2),за исключением соединения кислорода со фтором O+2F-2 и в перекисях( Н2О2 - степень окисления кислорода (-1). 6.Фтор имеет степень окисления (-1)
7. Алгебраическая сумма степеней окисления равна 0
Алгоритм определения степени окисления по формуле
|
Задание . Определите степень окисления в соединении Р2О5
|
|
1.Запишите формулу заданного вещества
|
Р2О5
|
|
2. Запишите значение степени окисления элемента, у которого она постоянна
|
Р2О5 -2
|
|
3. Найдите общее число степени окисления известного элемента
|
(-2) ∙ 5= - 10
|
|
4. Общее число положительной степени окисления численно равно общему числу отрицательной степени окисления
|
Р2 О5 -2
+10 -10
|
|
5. Найдите величину положительной степени окисления, разделив ее на индекс у этого элемента
|
(+10) ꞉ 2 = +5
|
|
6. Поставьте значение степени окисления
|
Р2 +5 О5 -2
|
Определить степени окисления в соединении K2Cr2O7 У двух химических элементов калия и кислорода степени окисления постоянны и равны соответственно +1 и -2. Число степеней окисления у кислорода равна (-2)·7=(-14), у калия (+1)·2=(+2). Число положительных степеней окисления равно числу отрицательных.
Следовательно (-14)+(+2)=(-12). Значит у атома хрома число положительных степеней равно 12, но атомов 2, значит на один атом приходится (+12):2=(+6), записываем степени окисления над элементами К+2Cr+62O-27
Алгоритм составление химических формул по степени окисления
|
1. Записать химические знаки элементов
|
Аl S
|
|
2. Определить степень окисления
|
Аl+3 S-2
|
|
3. Найти наименьшее общее кратное и определить индексы
|
Аl+3 S-2
НОК =6
|
|
4.Формула
|
Аl2+3 S3-2
|
Алгоритм составления уравнений реакций
|
Последовательность действий
|
Пример
|
|
1. В левой части уравнения приведем формулы веществ, вступающих в реакцию (реагентов)
|
Р+ O2→
|
|
2. В правой части после стрелки пишем формулы веществ, образующихся в результате реакции(продуктов)
|
Р + O2→Р2O5
|
|
3 С помощью коэффициентов начинаем уравнивать число тех атомов ,которых в реакцию вступает больше (через НОК)
|
нок 10
Р+ 5O2→2Р2O5
|
|
4. С помощью коэффициентов уравниваем число других атомов
|
4Р+ 5O2→2Р2O3
|


Составление уравнений окислительно-восстановительных реакций
В методе электронного баланса сравнивают степени окисления атомов в исходных веществах и в продуктах реакции, при этом руководствуемся правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединённых окислителем.
Алгоритм составления окислительно- восстановительных реакций
|
Последовательность действий
|
Пример
|
|
Составить схему реакции.
|
CuCl2 + Al ® AlCl 3 + Cu
|
|
Определить элементы, атомы которых изменили степень окисления в результате реакции.
|
+2-1 0 +3-1 0
CuCl2 + Al ® AlCl3 + Cu
|
|
Найти окислитель и восстановитель.
|
+2 0
Cu + 2ē = Cu восстановление
окислитель
0 +3
Al - 3ē = Al окисление
Восстановитель
|
|
Составить электронные уравнения для процессов окисления и восстановления
|
+2 0
Cu + 2ē = Cu 3 восстановление
окислитель
0 +3
Al - 3ē = Al 2 окисление
Восстановитель
|
|
Найденные коэффициенты поставить перед формулами продуктов окисления и восстановления, а затем – перед формулами окислителя и восстановителя
|
3 CuCl2 + 2Al ® 2AlCl3 + 3Cu
|
Составление ионных уравнений реакций
|
Последовательность действий
|
Пример
|
|
1. Записать молекулярное уравнение реакции, подобрать коэффициенты
|
АlСl3 + 3КОН→Аl(ОН)3↓+ 3КСl
|
|
2. С помощью таблицы растворимости определить растворимость каждого вещества
|
АlСl3 – р; КОН – р; Аl(ОН)3↓- н;
КСl - р
|
|
3. Составить полное ионное уравнение реакции, записав электролиты в виде ионов, неэлектролиты – в молекулярном виде
|
Аl3+ +3Сl- + 3К++3ОН-→Аl(ОН)3↓+ 3К++3Сl-
|
|
4. Составить сокращенное ионное уравнение реакции, сократив одинаковые ионы в левой и правой частях уравнения
|
Аl3+ +3ОН-→Аl(ОН)3↓
|
Просмотр содержимого документа
«Алгоритмы составления формул и уравнений химических реакций»
Алгоритмы составления химических формул и уравнений химических реакций.
Валентность
Валентность – способность атомов присоединять к себе определенное число других атомов
Составление формул по валентности
| Алгоритм решения | Пример |
| 1. Запишите символы элементов (согласно ряду электроотрицательности) | Аl О
|
| 2. Запишите валентность элементов (по периодической системе) | III II Аl О |
| 3. Найдите наименьшее общее кратное (нко) между числовыми значениями валентности | 6 III II Аl О НКО =6 |
| 4. Найдите соотношение между атомами элементов (деля НКО на соответствующую валентность). Полученные значения являются индексами | 6 III II Аl О 6 : 3=2 6 : 2= 3 →2:3 |
| 5. Запишите формулы веществ | Аl2 О3 |
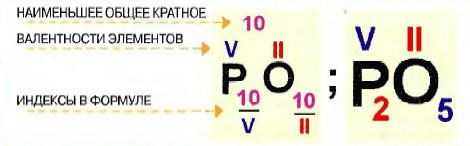
Определение валентности по формуле
| Алгоритм решения | Пример |
| 1. Запишите формулу вещества | Р2 О5 |
| 2. Обозначьте известную валентность элемента
| II Р2 О5 |
| 3. Найдите наименьшее общее кратное (нко) между числовыми значениями валентности | 10 II Р2 О5 НКО =10 |
| 4. Поделите наименьшее общее кратное на количество атомов другого элемента. Полученный ответ и является искомой валентностью | 10 V II Р2 О5 10: 2=5 |
| 5. Сделайте проверку перемножьте валентность на индекс каждой части формулы. Их производные должны быть равны | V II Р2 О5 10 = 10
|
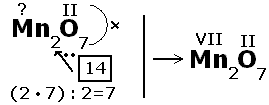
Степень окисления
1.Элемент в простом веществе имеет нулевую степень окисления.
2.Все металлы имеют положительную степень окисления.
3. Водород имеет в соединениях степень окисления (+1), исключая гидриды ( соединения водорода с металлами главной подгруппы первой, второй групп, степень окисления -1, например Na+H- );
5.Кислород имеет степень окисления (-2),за исключением соединения кислорода со фтором O+2F-2 и в перекисях( Н2О2 - степень окисления кислорода (-1).
6.Фтор имеет степень окисления (-1)
7. Алгебраическая сумма степеней окисления равна 0
Алгоритм определения степени окисления по формуле
| Задание . Определите степень окисления в соединении Р2О5 |
| 1.Запишите формулу заданного вещества | Р2О5
|
| 2. Запишите значение степени окисления элемента, у которого она постоянна
| Р2О5 -2 |
| 3. Найдите общее число степени окисления известного элемента | (-2) ∙ 5= - 10 |
| 4. Общее число положительной степени окисления численно равно общему числу отрицательной степени окисления | Р2 О5 -2 +10 -10 |
| 5. Найдите величину положительной степени окисления, разделив ее на индекс у этого элемента | (+10) ꞉ 2 = +5 |
| 6. Поставьте значение степени окисления | Р2 +5 О5 -2 |
Определить степени окисления в соединении K2Cr2O7
У двух химических элементов калия и кислорода степени окисления постоянны и равны соответственно +1 и -2. Число степеней окисления у кислорода равна (-2)·7=(-14), у калия (+1)·2=(+2). Число положительных степеней окисления равно числу отрицательных.
Следовательно (-14)+(+2)=(-12). Значит у атома хрома число положительных степеней равно 12, но атомов 2, значит на один атом приходится (+12):2=(+6), записываем степени окисления над элементами К+2Cr+62O-27
Алгоритм составление химических формул по степени окисления
| 1. Записать химические знаки элементов | Аl S |
| 2. Определить степень окисления
| Аl+3 S-2 |
| 3. Найти наименьшее общее кратное и определить индексы | Аl+3 S-2 НКО =6 |
| 4.Формула | Аl2+3 S3-2
|
Алгоритм составления уравнений реакций
| Последовательность действий | Пример |
| 1. В левой части уравнения приведем формулы веществ, вступающих в реакцию (реагентов)
| Р+ O2→ |
| 2. В правой части после стрелки пишем формулы веществ, образующихся в результате реакции(продуктов)
| Р + O2→Р2O5 |
| 3 С помощью коэффициентов начинаем уравнивать число тех атомов ,которых в реакцию вступает больше (через НОК)
| нок 10 Р+ 5O2→2Р2O5 |
| 4. С помощью коэффициентов уравниваем число других атомов
| 4Р+ 5O2→2Р2O3 |
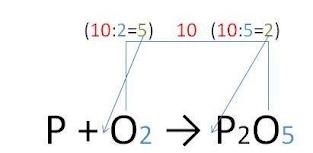
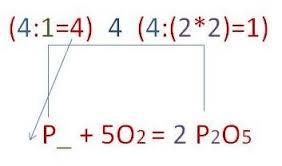
Составление уравнений окислительно-восстановительных реакций
В методе электронного баланса сравнивают степени окисления атомов в исходных веществах и в продуктах реакции, при этом руководствуемся правилом: число электронов, отданных восстановителем, должно равняться числу электронов, присоединённых окислителем.
Для составления уравнения надо знать формулы реагирующих веществ и продуктов реакции.
| Расставить коэффициенты в реакции, схема которой: HCl + MnO2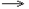 Cl2 + MnCl2 + H2O Cl2 + MnCl2 + H2O |
| Алгоритм расстановки коэффициентов |
| 1.Указываем степени окисления химических элементов. 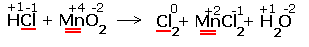 Подчёркнуты химические элементы, в которых изменились степени окисления. |
| 2.Составляем электронные уравнения, в которых указываем число отданных и принятых электронов. 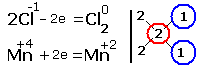 За вертикальной чертой ставим число электронов, перешедших при окислительном и восстановительном процессах. Находим наименьшее общее кратное ( взято в красный кружок). Делим это число на число перемещённых электронов и получаем коэффициенты (взяты в синий кружок). Значит, перед марганцем будет стоять коэффициент-1, который мы не пишем, и перед Cl2 тоже -1. Перед HCl коэффициент 2 не ставим, а считаем число атомов хлора в продуктах реакции. Оно равно - 4.Следовательно, и перед HCl ставим - 4,уравниваем число атомов водорода и кислорода справа, поставив перед H2O коэффициент - 2. В результате получится химическое уравнение: 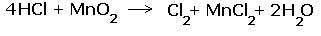 |
| Рассмотрим более сложное уравнение: |
| H2S + KMnO4 + H2SO4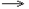 S + MnSO4 + K2SO4 + H2O S + MnSO4 + K2SO4 + H2O |
| Расставляем степени окисления химических элементов: 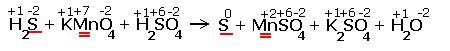 |
| Электронные уравнения примут следующий вид 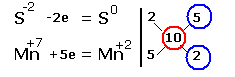 Перед серой со степенями окисления -2 и 0 ставим коэффициент 5, перед соединениями марганца -2, уравниваем число атомов других химических элементов и получаем окончательное уравнение реакции |
| 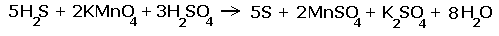
|
Алгоритм составления окислительно- восстановительных реакций
| Последовательность действий | Пример |
| Составить схему реакции. | CuCl2 + Al AlCl 3 + Cu |
| Определить элементы, атомы которых изменили степень окисления в результате реакции.
| +2-1 0 +3-1 0 CuCl2 + Al AlCl3 + Cu |
| Найти окислитель и восстановитель.
| +2 0 Cu + 2ē = Cu восстановление окислитель 0 +3 Al - 3ē = Al окисление Восстановитель
|
| Составить электронные уравнения для процессов окисления и восстановления | +2 0 Cu + 2ē = Cu 3 восстановление окислитель 0 +3 Al - 3ē = Al 2 окисление Восстановитель
|
| Найденные коэффициенты поставить перед формулами продуктов окисления и восстановления, а затем – перед формулами окислителя и восстановителя
| 3 CuCl2 + 2Al 2AlCl3 + 3Cu |
Составление ионных уравнений реакций
| Последовательность действий | Пример |
| 1. Записать молекулярное уравнение реакции, подобрать коэффициенты | АlСl3 + 3КОН→Аl(ОН)3↓+ 3КСl |
| 2. С помощью таблицы растворимости определить растворимость каждого вещества | АlСl3 – р; КОН – р; Аl(ОН)3↓- н; КСl - р |
| 3. Составить полное ионное уравнение реакции, записав электролиты в виде ионов, неэлектролиты – в молекулярном виде | Аl3+ +3Сl- + 3К++3ОН-→Аl(ОН)3↓+ 3К++3Сl- |
| 4. Составить сокращенное ионное уравнение реакции, сократив одинаковые ионы в левой и правой частях уравнения | Аl3+ +3ОН-→Аl(ОН)3↓ |