8 класс
Конспект урока по теме
"Химические свойства оснований. Реакция нейтрализации. Применение оснований"
Задачи урока:
Образовательные: продолжить формирование представлений об основных классах неорганических соединений - основаниях; рассмотреть и изучить свойства растворимых (щелочей) и нерастворимых оснований; сформировать понятие о реакции нейтрализации как частном случае реакции обмена; формирование умений проводить химический эксперимент в соответствии с правилами ТБ, обращаться с химической посудой и оборудованием; продолжить развивать навыки в составлении уравнений реакций и расстановке коэффициентов.
Развивающие: развивать самостоятельность в работе с учебником и при проведении эксперимента; совершенствовать умения сравнивать вещества, выявлять общие черты и различия в свойствах и составе оснований; развитие мыслительных операций; познавательной деятельности через ИКТ, межпредметных связей; развитие речи с использованием химической терминологии.
Воспитательные: формирование научного мировоззрения; воспитание коллективизма и развитие навыков индивидуальной работы; коммуникативных способностей учащихся; Профориентационное воспитание.
Способы достижения цели и задач:
Метод обучения: Словесный, наглядный и практический. Использование фрагментов презентации, демонстрация опытов, химический эксперимент (работа сотрудников ХАЛ), работа у доски, индивидуальные карточки-задания для проверки усвоения полученных знаний, работа с учебником, таблицами.
Тип урока: Изучение нового материала с проведением практических опытов и записью основных положений в тетрадь.
Оборудование: Ящички для проведения лабораторных опытов, пробирки, штативы для пробирок, спиртовки, стеклянные палочки, пипетки, спички, держатели, пробка с газоотводной трубкой, колбы конические, чашки фарфоровые.
Реактивы: растворы NaOH, NH4OH, йода, фенолфталеин, метиловый оранжевый, лакмус, универсальная индикаторная бумага, HCl, H2SO4; CuSO4; AlCl3; CaCO3(k); Ca(OH)2; Fe2(SO4)3; CoCl2, NH4Cl, Al (фольга).
Требования к учащимся:
Должны знать: определение оснований, признаки классификации, получение и свойства оснований, особенности свойств нерастворимых оснований.
Должны уметь: составлять формулы оснований и называть их, находить соответствие между основными оксидами и основаниями.
Отрабатываемые навыки: написание уравнений ионных реакций, работы с Таблицей растворимости, составление формул сложных веществ, проведение химического эксперимента и описание наблюдаемых явлений.
Ход урока:
1. Организационный момент. (1мин)
Приветствие, проверка готовности к уроку, отметка отсутствующих.
Здравствуйте мои коллеги, уважаемые гости, ребята.
-Обратите внимание, у нас сегодня урок, который мы проводим совместно с представителями «НОВАТЭК-ТАРКОСАЛЕНЕФТЕГАЗ».
Учитель:
Сегодня мы продолжим говорить о важном классе химических соединений. Чтобы узнать, что это за класс веществ, прослушайте и отгадайте загадку.
Из нас не сваришь супа,
Содержим мы гидроксогруппу,
И активного металла
В нашей формуле немало.
Красим лакмус в синий цвет,
Мы опасны, спору нет. (Основания.)
Вы правильно отгадали загадку. Именно об основаниях мы и продолжим говорить.
2. Актуализация знаний. (6 мин) (Словесный метод)
Учитель: Прежде чем приступить к изучению новой темы, давайте повторим, тот материал, который мы изучили на прошлом уроке. Те знания, которые вы получили на прошлом уроке, сегодня вам понадобятся.
Игра «крестики-нолики»
3 учеников у доски показывают выигрышный путь:
| а) основные оксиды |
| б) растворимые основания |
| в) нерастворимые основания |
| CuO | SO3 | P2O5 | KOH | Cr(OH)3 | Al(OH)3 |
| Ba(OH)2 | NaOH | Cu(OH)2 |
| Na2O | BaO | N2O3 | Fe(OH)2 | NaOH | Fe(OH)3 |
| Ca(OH)2 | Al(OH)3 | LiOH |
| K2O | CO2 | SO2 | Cu(OH)2 | Mg(OH)2 | Ba(OH)2 |
| Fe(OH)3 | Cr(OH)3 | KOH |
Учитель: Напомню вам, что тема нашего прошлого урока была «Основания, их состав и классификация». Поэтому исходя из темы сразу же 1 вопрос:
Какой класс веществ называют основаниями? (определение)
О.: Основаниями, называют сложные вещества, в состав которых входят атомы металлов, соединенные с одной или несколькими гидроксогруппами. (Слайд 1)
Учитель: Зная определение оснований, выведите общую формулу для этого класса веществ?
О.: Me(OH)n.
Учитель: Давайте попытаемся расшифровать, что означает эта запись - сочетание букв Me?
О.: На месте этих букв может быть химический знак любого металла из периодической таблицы. Д.И. Менделеева.
Учитель: «– ОН» что это за сочетание?
О.: Гидроксильная группа – ОН или её второе название гидроксогруппа.
Учитель: Какова валентность гидроксогруппы? (Слайд 2)
О.: Валентность гидроксогруппы равна I.
Учитель: Что означает буква n стоящая после гидроксогруппы?
О.: n – это индекс, показывающий число гидроксильных групп ОН входящих в данное соединение, и показывает валентность металла, образовавшего данный гидроксид.
Учитель: Как мы даем названия основаниям? (Слайд 3)
Учитель: Руководствуясь всеми перечисленными правилами, составьте и произнесите формулы следующих гидроксидов: (Слайд 4)
«гидроксид натрия, гидроксид кальция, гидроксид железа (III), гидроксид калия, гидроксид алюминия, гидроксид магния».
О: NaOH Ca(OH)2 Fe(OH)3 KOH Al(OH)3 Mg(OH)2
(Фронтальная беседа)
Учитель: Раз существует в химии целый класс веществ, называемых «основания», и известно большое их количество, то встает вопрос о необходимости объединить все эти вещества с одинаковыми свойствами в одну группу, то есть другими словами основания тоже классифицируют.
Перечислите, на какие группы можно классифицировать все основания по растворимости? (Слайд 5)
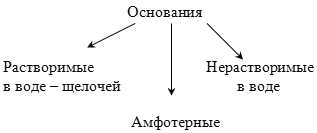
Учитель: Какие основания называются амфотерными?
О.: Амфотерные – это основания, которые могут проявлять свойства характерные как для оснований, так и для кислот.
Учитель: Еще по какому признаку классифицируют основания? (Слайд 6)
О.: по числу гидроксогрупп.
Однокислотные: NaOH – гидроксид натрия, KOH – гидроксид калия.
Двухкислотные: Pb(OH)2 – гидроксид свинца, Fe(OH)2 – гидроксид железа (III)
Трехкислотные: Al(OH)3 – гидроксид алюминия
3. Сообщение темы, цели урока. (2 мин)
Учитель: Все, что касается состава и классификации оснований мы с вами повторили. Но все же наши знания об основаниях будут неполными, если мы не расскажем об их химических свойствах. (Слайд 7)
Поэтому тема нашего сегодняшнего урока «Химические свойства оснований и их применение. Реакция нейтрализации».
Запишите число и тему урока в тетради.
Ребята на сегодняшнем уроке мы с вами:
изучим химические свойства оснований;
познакомимся с реакцией нейтрализации, как частным случаем реакции обмена.
и поговорим о применении оснований.
4. Изучение нового материала. (20 мин)
Учитель: Для оснований характерны не только различные физические свойства, но и целый ряд химических свойств. Давайте рассмотрим эти свойства. В этом мне помогут сотрудники ХАЛ «НОВАТЭК-ТАРКОСАЛЕНЕФТЕГАЗ»
(Слайд 8)
Учитель: Первое свойство - это изменение цвета индикаторов, при действии растворов щелочей.
Индикатор - это определитель или указатель среды любого раствора.
Обратите внимание на цвета индикаторов в нейтральной среде.
(Слайд 9)
Учитель: Запишите схемы к себе в тетрадь.
лакмус + любая щелочь синий.
метиловый оранжевый + любая щелочь жёлтый.
фенолфталеин + любая щелочь малиновый.
Нерастворимые основания не меняют окраску индикаторов.
А теперь понаблюдаем с помощью опыта, как изменяют свой цвет эти же индикаторы в щелочной среде
Опыт 1. (ХАЛ) В качестве первого свойства оснований мы приведем свойство - изменять окраску индикаторов.
В водном растворе любой щёлочи сильной или слабой и даже щелочи с осадком содержатся гидроксид-ионы, и именно они, фактически взаимодействуют с индикаторами. При этом протекает химическая реакция с образованием нового продукта, признаком протекания которой является изменение окраски веществ.
Таким образом любая щелочь взаимодействуя с лакмусом окрашивает его в синий цвет. Это мы можем продемонстрировать при помощи лакмусовой бумажки.
Также любая щелочь взаимодействуя с метиловым оранжевым окрашивает его в желтый цвет. И любая щелочь при взаимодействии с фенолфталеином окрашивает его в малиновый цвет.
(Слайд 10)
Учитель: Второе свойство: – это взаимодействие щелочей с кислотными оксидами с образованием соли и воды.
2KOH + N2O5 = 2KNO3 + H2O
2NaOH + SO3 = Na2SO4 + H2O
А нерастворимые основания с кислотными оксидами не взаимодействуют!
(Слайд 11)
Учитель: Третье свойство: – это взаимодействие щелочей с растворами солей, в результате образуются нерастворимое основание и новая соль.
2NaOH + СоCl2 = 2NaCl + Со(OH)2
голубой осадок
NaOH + NH4Cl = NaCl + NH4OH или (NH3↑ + H2O)
Опыт 2. (ХАЛ) Выясним, взаимодействуют ли щелочи с солями, проведем следующий опыт. В раствор хлорида кобальта добавим раствор гидроксида натрия. В результате выпадает синий осадок. Это, конечно, свидетельствует о том, что реакция прошла успешно и в качестве синего осадка в нашем случае гидроксид кобальта. Данная реакция является реакцией обмена, т.е. это реакция между сложными веществами, в ходе которых они обмениваются своими составными частями. Соли могут взаимодействовать со щелочами, если в результате реакции образуется нерастворимое в воде вещество.
Продемонстрируем следующую реакцию. При сливании растворов хлорида аммония и гидроксида натрия видимых изменений не происходит. Но попробуем нагреть полученную смесь почти до кипения. Теперь поднесем к пробирке смоченную водой бумажку лакмуса, как видим лакмус синеет. Из пробирки выделяется газ с резким характерным запахом. Это аммиак.
Мы с вами даже можем сделать вывод о том, что реакции солей аммония со щелочами могут быть использованы в лаборатории для получения аммиака.
(Слайд 12)
Учитель: Четвертое свойство: – это взаимодействие оснований с кислотами,
в результате образуются соль и вода.
а) Рассмотрим взаимодействие щелочей с кислотами.
NaOH + HCl = NaCl + H2O
Продемонстрируем это свойство на опыте, который сейчас нам покажут специалисты ХАЛ.
Опыт 3. (ХАЛ) Рассмотрим следующее свойство.
Щёлочи, как основания, взаимодействуют с кислотами с образованием соли и воды, эта реакция называется реакцией нейтрализации. Это одно из самых важных химических свойств щелочей.
На данном слайде это свойство отражает следующая реакция. Взаимодействия гидроксида натрия с соляной кислотой - с образованием хлорида натрия и воды.
Получившийся водный раствор хлорида натрия можно выпарить, т.е. вода испариться и останутся белые кристаллики, это и есть кристаллики поваренной соли.
Продемонстрируем эту реакцию опытным путем. Возьмем три пробирки с гидроксидом натрия, о его наличии свидетельствует окрашенный малиновый раствор. Теперь в одну из пробирок добавим раствор соляной кислоты в недостатке. Т.е. не весь гидроксид натрия прореагировал, и мы видим, что розовый оттенок остался в пробирке. А в другую пробирку добавим соляную кислоту в избытке, т.о. весь гидроксид натрия прореагировал и щелочи в пробирке совсем не осталось, теперь в этой пробирке соль и вода.
Еще раз повторим, что реакция между кислотой и основаниями, в результате которой образуется – соль и вода, называется реакцией нейтрализации.
Нерастворимые основания также взаимодействуют с кислотами, но реакция происходит лишь в том случае, если соль, которая образуется при реакции, растворяется в воде.
Учитель: Получившийся раствор можно выпарить, и получить белые кристаллики поваренной соли.
б) Рассмотрим взаимодействие нерастворимых оснований с кислотами. При этом образуется соль и вода.
Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Запишем определение:
• Реакция между кислотой и основаниями, в результате которой образуется – соль и вода, называется реакцией нейтрализации.
• Реакции между сложными веществами, входе которых они обмениваются своими составными частями, называют реакциями обмена.
(Слайд 13)
Учитель: А нерастворимые в воде основания разлагаются при нагревании. Продуктами разложения будут оксиды соответствующих металлов и вода.
t0
Cu(OH)2 = CuO + H2O
t0
Mg(OH)2 = MgO + H2O
(Слайд 14)
Опыт 4. (ХАЛ)
Один из способов получения водорода в лаборатории основан на реакции алюминия с раствором щелочи - едкого натра.
Насыпаем в колбу несколько грамм едкого натра, нальём воды и перемешаем содержимое до растворения щелочи. Добавим в колбу несколько кусочков алюминия. Начнется выделение водорода - сначала слабое, потом все более сильное. Раствор при этом будет разогреваться.
Алюминий - довольно активный металл, он легко реагировал бы с водой, если бы не прочная оксидная пленка на поверхности алюминия. Поэтому алюминий может очень долго контактировать с водой без каких-либо признаков разрушения. Вспомните, что еще недавно на кухнях активно использовали алюминиевую посуду. Алюминиевые линии электропередач десятилетиями служат в любую погоду - и в солнце, и в дождь.
Но при контакте со щелочью оксидная пленка на поверхности алюминия разрушается, и он начинает реагировать с водой. В результате выделяется водород, а металл растворяется.
(Слайд 15)
Опыт 5. (ХАЛ) Также рассмотрим еще одно свойство, которое является как химическим свойством, так и свойством гидроксида, которое можно применять в быту. Это свойство связано с обесцвечиванием йодного раствора.
Конечно, испачкать одежду, мебель, ковер, предметы обихода йодом надо еще умудриться, но, к сожалению, случается и такое. Рассмотрим эффективный способ удаления пятен йода с одежды, мебели и других вещей.
Гидроксид натрия приобрести можно в аптеках или в хозяйственных магазинах. Пожалуй, это одно из самых эффективных средств для борьбы с пятнами от йода. Гидроксид натрия моментально обесцвечивает кристаллы йода, проникшие в волокна ткани. Для реализации этого метода нанесите немного гидроксида натрия на пятно. Оно исчезнет буквально на глазах. Но следует поспешить и, не теряя времени, прополоскать вещь в проточной воде. В противном случае ткань может повредиться.
5. Обобщение и закрепление знаний, учащихся. (5 мин)
Учитель: Теперь давайте обобщим изученные свойства: Итак, сделаем вывод, какие свойства характерны щелочей?
О.: Для щелочей характерно, их взаимодействие с кислотами, кислотными оксидами и солями, а также щелочи изменяют цвет индикаторов.
Учитель:
А теперь так же попытайтесь сделать вывод для нерастворимых оснований.
О.: Для нерастворимых оснований характерно их взаимодействие с кислотами и разложения при нагревании.
Учитель: Найдите свойство, которое характерно и для щелочей, и для нерастворимых оснований?
О.: И для щелочей, и для нерастворимых оснований характерно их взаимодействие с кислотами.
Подведем итог: таким образом, сегодня на уроке, мы с вами изучили химические свойства оснований, и выяснили, что для щелочей (растворимых в воде оснований) характерны одни свойства, а для нерастворимых оснований – другие свойства.
6. Подведение итогов урока (2 мин).
И с учетом ответов, а так же оценю вашу работу сегодня на уроке.
(Выставление оценок за ответы учащихся).
7. Информация о домашнем задании и его комментарий (3 мин) (Слайд 16)
Учитель: Домашнее задание для вас сегодня приготовлено на последнем листочке раздаточного материала. Вы выполните его в тетради. С применением оснований вы можете ознакомиться в раздаточном материале.
Занятие наше подошло к концу.
Давайте поблагодарим Розу Айратовну и Оксану Сергеевну за помощь и демонстрацию опытов. Если нет вопросов, то всем Спасибо.
Д/з § 42, в 2,4 стр.144-145
Варианты индивидуальных заданий:
на «3»: Закончите первые 4 уравнения реакций;
на «4»: Закончите 5 уравнений реакций,
на «5»:Закончите 5 уравнения реакций, назовите продукты реакции.
1) NaOH + CuSO4 =
2) КOH + AlCl3 =
3) Fe(OH)3 =
4) KOH+ HNO3 =
5) Ca(OH)2 + SO3 =
8. Рефлексия (1 мин). (Слайд 18)
Какое настроение сложилось в ходе урока?
Понравился ли урок и ВАША работа на нем?
12.03.2018г.
Тестовые задания по вариантам.
Вариант 1.
1. С основаниями не реагируют:
1) SiO2 2) SO2 3) Fe2O3 4) NiO
2. При нагревании гидроксида меди (II) образуются:
1) Cu и H2O 2) CuO и H2 3) CuO и H2O 4) Cu2O и H2O
3. Гидроксид натрия взаимодействует с:
1) SO3 2) Na2O 3) Mg(OH)2 4) N2O
4. Гидроксид калия не реагирует с:
1) Al(OH)3 2) ZnO 3) H2SO4 4) Mg(OH)2
5. Реакция нейтрализации возможна между:
1) Солью и водой.
2) Кислотой и основанием.
3) Кислотным оксидом и основанием.
4) Кислотой и основным оксидом.
Вариант 2.
1. С основаниями не реагируют:
1) SrO 2) SO3 3) N2O3 4) P2O3
2. При нагревании гидроксида алюминия образуются:
1) Al2O3 и H2O 2) Al и H2 3) Al и H2O 4) Al2O3 и H2
3. Гидроксид калия взаимодействует с:
1) CaO 2) CH4 3) Ba(OH)2 4) HCl
4. Гидроксид натрия не реагирует с:
1) Al(OH)3 2) ZnO 3) H2SO4 4) Ba(OH)2
5. Реакция нейтрализации возможна между:
1) Кислотным оксидом и основанием.
2) Кислотой и основным оксидом.
3) Солью и водой.
4) Кислотой и основанием.
Ответы на тестовые задания.
Вариант 1.
1) 4 2) 3 3) 1 4) 4 5) 2
Вариант 2.
1) 1 2) 1 3) 4 4) 4 5) 4

















