Урок №40 8 класс «_____»_____20____г.
Тема: Химические свойства оснований. Получение. Применение. Лабораторный опыт №3. Взаимодействие щелочей с кислотами в растворе.
Цель: Сформировать понятия о химических свойствах оснований, основных способах получения и применения; сравнить химические свойства растворимых и нерастворимых оснований.
Задачи:
Образовательные: формировать умение составлять формулы оснований, давать им названия; рассмотреть химические свойства оснований; сравнить химические свойства растворимых и нерастворимых оснований;
Развивающие: продолжить развивать навыки составления уравнений химических реакций;
Воспитательные: рассмотреть правила техники безопасности при работе с основаниями.
Планируемые результаты обучения
Предметные. Знать химические свойства оснований. Уметь составлять уравнения реакций нейтрализации.
Метапредметные. Развивать умения самостоятельно определять цели своего обучения, ставить и формулировать для себя новые задачи в учёбе и познавательной деятельности, развивать мотивы и интересы своей познавательной деятельности, соотносить свои действия с планируемыми результатами, осуществлять контроль своей деятельности в процессе достижения результата.
Личностные. Формировать ответственное отношение к учению, коммуникативную компетентность.
Оборудование и материалы: Периодическая система химических элементов Д. И. Менделеева, таблица растворимости, растворы гидроксида натрия, соляной кислоты, серной кислоты, сульфата меди, фенолфталеина; индикаторная бумага, гидроксид меди, гидроксид железа (III), углекислый газ, газоотводная трубка, нагревательное оборудование, пробирки, держатели для пробирок, штативы.
Базовые понятия и термины: реакция нейтрализации, индикаторы, среда раствора (кислая, щелочная, нейтральная), известковое молоко, реакции обмена, растворимость.
Тип урока: Комбинированный.
Структура урока
I. Организационный этап
II. Актуализация опорных знаний
III. Ознакомление с темой урока, постановка его целей и задач (мотивация)
IV. Изучение нового материала
Получение и применение оснований.
Правила техники безопасности при работе со щелочами.
Химические свойства оснований.
Лабораторный опыт №3
Применение
V. Первичное закрепление изученного материала
VI. Подведение итогов урока, постановка домашнего задания
VII. Рефлексия
ХОД УРОКА
ОРГАНИЗАЦИОННЫЙ ЭТАП (Учет отсутствующих учащихся).
II. АКТУАЛИЗАЦИЯ ОПОРНЫХ ЗНАНИЙ (проверка выполнения домашнего задания; проверка ранее усвоенных знаний)
Какие вещества называются основаниями? (Основания — сложные неорганические вещества, состоящих из атомов металлов и одной или нескольких гидроксильных групп (Гидроксогруппа одновалентна).
Назовите общую формулу гидроксидов (Ме(ОН)п , где Me — обозначение металла, п — его валентность)
Какие бывают основания? (Основания делятся на растворимые и нерастворимые в воде, растворимые основания называются щелочам).
Задание. Пользуясь таблицей растворимости, приведите формулы и названий растворимых и нерастворимых гидроксидов.
Д/з §41 с.137-139 №4

III. ОЗНАКОМЛЕНИЕ С ТЕМОЙ УРОКА ПОСТАНОВКА ЕГО ЦЕЛЕЙ И ЗАДАЧ (МОТВАЦИЯ)
Формулировка и запись темы урока. Тема: Химические свойства оснований. Получение. Применение.
Самостоятельное выделение и формулирование познавательной цели
IV. ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА
Рассказ учителя.
Рассмотрение схемы в учебнике
ПОЛУЧЕНИЕ ОСНОВАНИЙ
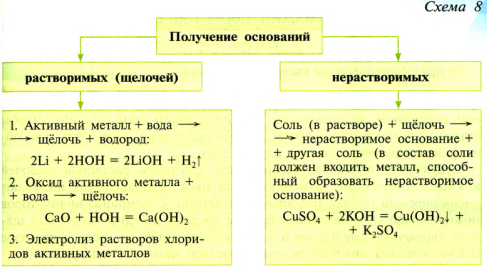
ПРАВИЛА ТЕХНИКИ БЕЗОПАСНОСТИ ПРИ РАБОТЕ СО ЩЕЛОЧАМИ.
Рассказ учителя.
При попадании раствора щелочи и кожу или одежду необходимо смыть ее большим количеством проточной воды до исчезновения чувства мылкости, а затем нейтрализовать слабой кислотой — борной или уксусной.
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ.

а) Взаимодействие щелочей с кислотными оксидами.
При этом наблюдается помутнение раствора из-за выпадения в осадок нерастворимого карбоната кальция: Са (ОН)2 + СО2 = СаСО3 + Н2О .
Вывод: все щелочи имеют примесь карбонатов за счет взаимодействии углекислым газом воздуха.
б) Взаимодействие щелочей с растворимыми солями.
Выпадает бурый осадок гидроксида железа (III): FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl.
Вывод: эта реакция является реакцией получения нерастворимых оснований.
Выполнение лабораторного опыта
Лабораторный опыт №3.
Тема: Взаимодействие щелочей с кислотами в растворе.


Работа с учебником


Работа с учебником
Применение.
Самостоятельно работают с учебником С. 143, записывают, а потом озвучивают свои записи.
ПЕРВИЧНОЕ ЗАКРЕПЛЕНИЕ ИЗУЧЕННОГО МАТЕРИАЛА
Работа по вопросам в конце §42


ПОДВЕДЕНИЕ ИТОГОВ УРОКА, ПОСТАНОВКА ДОМАШНЕГО ЗАДАНИЯ (выставление оценок, записывают задание Изучить §42 Выполнить задания №2,5)
РЕФЛЕКСИЯ
Ребята, давайте поделимся своими впечатлениями по уроку.Ответьте на следующие вопросы:
- я узнал…
- я хотел узнать…
- я узнал…

































