
Химическое равновесие

Химическое равновесие
Химическое равновесие – состояние реакционной системы, при котором скорости прямой и обратной реакций равны и отличны от нуля:
υ (прям.) = υ (обрат.)
При неизменных условиях протекания реакции система продолжает находиться в равновесии, но при изменении какого-либо параметра равновесие смещается в сторону прямой или обратной реакции.
Принцип Ле-Шателье
Направление смещения равновесия определяется универсальным принципом подвижного равновесия ( принцип Ле-Шателье ): «внешнее воздействие находящуюся в равновесии, приводит к смещению этого равновесия в направлении, ослабляющем эффект внешнего воздействия».
Классификация химических реакций по направлению
Реакция
Обратимые
Необратимые
Обратимые реакции обозначаются знаком «⇄»
Необратимые реакции обозначаются знаком «→»
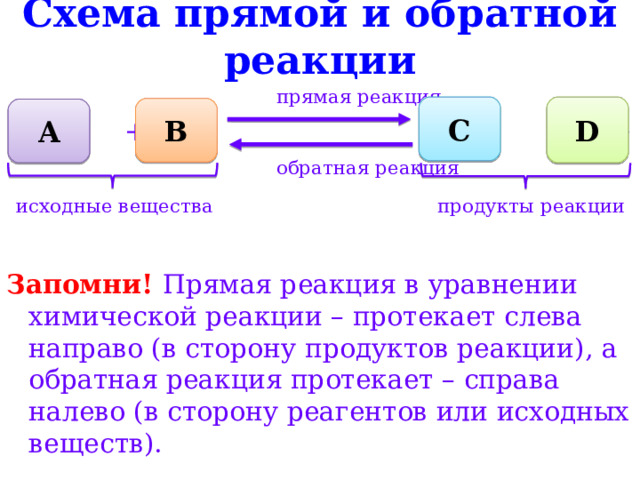
Схема прямой и обратной реакции
прямая реакция
+ +
обратная реакция
исходные вещества продукты реакции
Запомни! Прямая реакция в уравнении химической реакции – протекает слева направо (в сторону продуктов реакции), а обратная реакция протекает – справа налево (в сторону реагентов или исходных веществ).
С
D
B
A

Обратимые химические реакции
Обратимые реакции – это химические реакции, которые одновременно протекают как в прямом, так и в обратном направлениях.
Примеры некоторых обратимых реакций:
t º, p , Fe
N 2 + 3H 2 2NH 3 ↑
↯
N 2 + O 2 ↔ 2NO↑
t º, V 2 O 5
2SO 2 + O 2 2SO 3

Необратимые химические реакции
Практически необратимыми (необратимыми) – это химические процессы и реакции, протекающие только в одном направлении: продукты реакции не реагируют друг с другом с образованием исходных веществ.
Примеры необратимых реакций:
А. Реакции в которых происходит выделение теплоты:
t °
S + O 2 → SO 2 ↑ + Q

Необратимые химические реакции
Б. Реакции разложения некоторых веществ:
t °
2 KClO 3 → 2KCl + 2O 2 ↑ – Q
В. Реакции, в ходе которых один из продуктов уходит из сферы реакции в виде осадка или газа:
AgNO 3 + NaCl → AgCl↓ + NaNO 3
Na 2 CO 3 + 2HCl → 2NaCl + CO 2 ↑ + H 2 O
Г. Реакции, в растворах между сильными электролитами, в результате которых образуется слабый электролит, например, вода:
KOH + HNO 3 → KNO 3 + H 2 O

Факторы, не оказывающие влияние на смещение равновесия
1. Катализатор и ингибитор;
2. Перемешивание и измельчение веществ;
3. Давление, при условии, что в системе нет газообразных веществ.
Запомни! Перечисленные факторы не оказывают влияние на смещение равновесия, а могут изменять время установления равновесия.
Факторы, оказывающие влияние на смещение равновесия
Факторы влияющие на равновесия
Концентрация
Давление (объём)
Температура

Влияние изменения температуры
Запомни! Если прямая реакции является экзотермической ( +Q ) , то обратная эндотермической ( –Q ) и наоборот.
– + + → +
А. При повышении t ° равновесие смещается в сторону эндотермической реакции.
Б. При понижении t ° равновесие смещается в сторону экзотермической реакции.
Q
А
Б
А B
Q

Влияние изменения давления ( только для газообразных веществ )
А. При повышении P равновесие смещается в сторону реакции, идущей с уменьшением числа молекул газов .
Б. При понижении P равновесие смещается в сторону реакции, идущей с увеличением числа молекул газов .
Запомни! Давление не влияет на равновесие, если число молекул газов при протекании реакции не изменяется.

Влияния объема реакционной системы
А. При уменьшении объёма системы (давление увеличивается) положение равновесия смещается в сторону меньшего количества газообразных веществ.
Б. При увеличении объёма системы (давление уменьшается) положение равновесия смещается в сторону большего количества газообразных веществ.

Влияние концентраций ( только для жидкостей и газов)
А. При введение в равновесную систему дополнительного количества какого-либо из веществ, участвующих в реакции, равновесие смещается в сторону реакции, в ходе которой это вещество расходуется.
Б. Наоборот, выведение из равновесной системы какого-либо из вещества, способствует смещению равновесия в сторону реакции, идущей с образованием этого вещества.

Добавление реагента
При добавление вещества, которого нет в реакции, то возможно это вещество может реагировать с кем-то из участников реакции и уменьшать его концентрацию или может диссоциировать на ионы и повышать концентрацию какого либо из участников в реакции.































