Просмотр содержимого документа
«Химия элементов - Водород»

Водород

План конспекта
I. Общая характеристика
II. Нахождение в природе
III. Основные соединения
IV. Значение и применение
- Способы получения
- Химические свойства

I. Общая характеристика
- Водород ( hydrogenium – рождающий воду ) был открыт английским химиком Генри Кавендишем в 1766 г.
- Водород – легкий газ без цвета, без запаха, плохо растворим в воде, в смеси с воздухом (гремучий газ) горюч и крайне взрывоопасен.
- Молекула водорода состоит из двух атомов, связанных между собой ковалентной неполярной связью: Н–Н (Н 2 )
- Электронная конфигурация водорода в основном состоянии : 1s 1
- Атом водорода содержит на внешнем энергетическом уровне один неспаренный электрон в основном энергетическом состоянии. Возбужденного состояния у атома водорода нет.
- Степени окисления водорода: -1, 0, +1.
- В природе существуют три изотопа водорода. Наиболее распространен протий - 99,9885 ± 0,0070 %. Тритий радиоактивен.
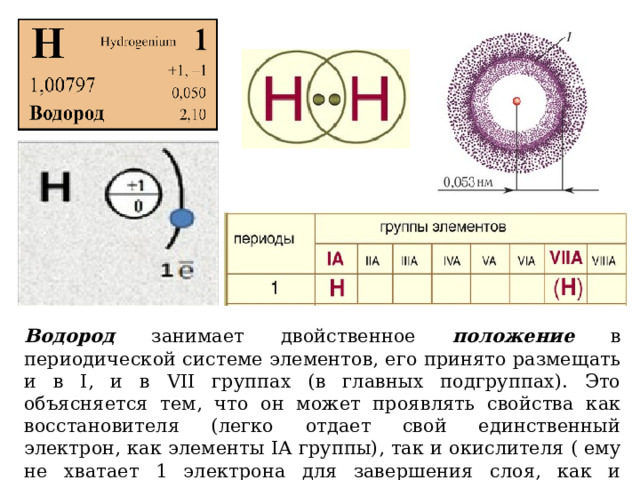
Водород занимает двойственное положение в периодической системе элементов, его принято размещать и в I, и в VII группах (в главных подгруппах). Это объясняется тем, что он может проявлять свойства как восстановителя (легко отдает свой единственный электрон, как элементы IА группы), так и окислителя ( ему не хватает 1 электрона для завершения слоя, как и элементам VIIA группы).
II. Нахождение в природе
- В настоящее время водород является самым распространённым элементом во Вселенной. На его долю приходится около 88,6% всех атомов (около 11,3% составляют атомы гелия, доля всех остальных вместе взятых элементов — порядка 0,1 %). Таким образом, водород — основная составная часть звезд и межзвездного газа.
- В условиях звёздных температур (например, температура поверхности Солнца ~6000°C) водород существует в виде плазмы, в межзвёздном пространстве в виде отдельных молекул, атомов и ионов.
- На планете Земля в свободном состоянии водорода практически нет (0,00005% по объёму для сухого воздуха). В основном он находится в виде соединений (вода, нефть, природный газ, гидроксиды и другие).
- Массовая доля водорода в земной коре составляет 1% — это 10-й по распространённости элемент. Однако его роль в природе определяется не массой, а числом атомов, доля которых среди других элементов составляет 17% (второе место после кислорода, доля атомов которого равна ~52%).
- Водород входит в состав практически всех органических веществ и присутствует во всех живых клетках, где по числу атомов на водород приходится почти 63%.

- Термоядерные реакции, в которых из ядер малой массы синтезируются более массивные , — основной источник энергии звёзд, причём наибольший вклад в общее количество выделяемой энергии вносят реакции термоядерного горения водорода
- При сверхвысоком давлении водород может стать металлическим. Считается, что большие количества металлического водорода присутствуют в ядрах планет-гигантов — Юпитера, Сатурна

III. Основные соединения
IV. Значение и применение
Заполните в конспекте самостоятельно
![Способы получения водорода В промышленности: Электролиз воды Паровая конверсия угля C + H 2 O → CO + H 2 ↑ Паровая конверсия метана СН 4 + Н 2 O → СО + 3Н 2 ↑ В лаборатории: Вытеснением из растворов кислот металлами средней активности: При взаимодействии амфотерных металлов с растворами щелочей: Zn + 2KOH + 2H 2 O = K 2 [Zn(OH) 4 ] + H 2 ↑ 2Al + 2NaOH + 6H 2 O → 2Na[Al(OH) 4 ] + 3H 2 ↑](https://static.multiurok.ru/multiurok/html/2025/02/09/s_67a7f544754c3/img8.jpg)
Способы получения водорода
- Электролиз воды
- Паровая конверсия угля C + H 2 O → CO + H 2 ↑
- Паровая конверсия метана СН 4 + Н 2 O → СО + 3Н 2 ↑
- Вытеснением из растворов кислот металлами средней активности:
- При взаимодействии амфотерных металлов с растворами щелочей:
Zn + 2KOH + 2H 2 O = K 2 [Zn(OH) 4 ] + H 2 ↑
2Al + 2NaOH + 6H 2 O → 2Na[Al(OH) 4 ] + 3H 2 ↑

Сбор водорода и проверка на чистоту
Собирают водород двумя способами:
- вытеснением воздуха (при том пробирку переворачивают вверх дном, так как водород легче воздуха)
- вытеснением воды (водород плохо растворяется в воде)
Проверяют водород на чистоту: подносят пробирку с газом к пламени спиртовки, водород сгорает с характерным «лающим» хлопком. Чем чище водород, тем тише хлопок.

Химические свойства водорода
- Реагирует с активными металлами (в ряду до Al), как окислитель, образуя гидриды:
2Na + H 2 2NaH
Ca + H 2 CaH
- Реагирует с большинством неметаллов (кроме Si и P), как восстановитель, образуя летучие водородные соединения (кроме Si и P):
S + H 2 H 2 S
Cl 2 + H 2 2HCl
- Не реагирует с водой, кислотами и основаниями

Химические свойства водорода
- Реагирует с некоторыми солями, как восстановитель:
BaSO 4 +4H 2 BaS + 4H 2 O
- Реагирует с оксидами металлов (в ряду от Mn), как восстановитель (металлургия):
ZnO + H 2 Zn + H 2 O
CuO + H 2 Cu + H 2 O
Fe 2 O 3 + H 2 2FeO + H 2 O
FeO + H 2 Fe + H 2 O
Этот способ восстановления металлов из руд (нерастворимых оксидов) лежит в основе пирометаллургии.
Но таким образом не получают очень активные металлы (ЩМ и ЩЗМ), а также алюминий














![Способы получения водорода В промышленности: Электролиз воды Паровая конверсия угля C + H 2 O → CO + H 2 ↑ Паровая конверсия метана СН 4 + Н 2 O → СО + 3Н 2 ↑ В лаборатории: Вытеснением из растворов кислот металлами средней активности: При взаимодействии амфотерных металлов с растворами щелочей: Zn + 2KOH + 2H 2 O = K 2 [Zn(OH) 4 ] + H 2 ↑ 2Al + 2NaOH + 6H 2 O → 2Na[Al(OH) 4 ] + 3H 2 ↑](https://static.multiurok.ru/multiurok/html/2025/02/09/s_67a7f544754c3/img8.jpg)













