КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ СЕРЫ
Романова Вероника Олеговна
Муниципальное общеобразовательное учреждение «Лицей № 2»
Октябрьского района г. Саратова
Аннотация урока
| Тема урока | Кислородсодержащие соединения серы |
| Класс | 9 |
| Рекомендуемые сроки проведения урока | 2 четверть, ноябрь. |
| Профиль | базовый общеобразовательный |
| Наглядные пособия | Карточки «Химические превращения сернистого газа в атмосфере»; карточки-инструкции «Нейтрализация сточных вод сернокислотного производства» |
| Оборудование: Для учителя: Для учащихся: | оборудование для мультимедийной презентации штатив для пробирок с 3 пробирками с образцами сточных вод сернокислотного производства на каждый стол. |
| Реактивы: Для учителя: Для учащихся |
раствор серной кислоты известковое молоко, карбонаты кальция и магния в виде суспензии |
| Электронные образовательные ресурсы | http://school-sector.relarn.ru/nsm/chemistry/Rus/chemy.html http://experiment.edu.ru/catalog.asp?cat_ob_no=12603 |
| Элементы содержания урока | 1. Организационный момент 2. Целеполагание и мотивация 3. Актуализация знаний и умений 4. Усвоение новых знаний и способов действия 5. Осознание и осмысление учебной информации 6. Контроль и самооценка знаний и способов действия 7. Подведение итогов занятия, информация о домашнем задании. 8. Рефлексия |
| Учебник | Рудзитис Г.Е. Химия. Неорганическая химия. Органическая химия. 9 класс: учеб. Для общеобразоват. учреждений / Г.Е. Рудзитис, Ф.Г. Фельдман – 13-е изд. – М.: Просвещение, 2009. – 191 с. |
| Дополнительная литература | Егоров А.С. и др. «Химия. Пособие-репетитор для поступающих в вузы», «Феникс», Ростов-на-Дону, 2006 г. |
Таблица 1. Технологическая карта урока.
| Этап урока | Деятельность | Планируемые результаты |
| учителя | учащихся | личностные | метапредметные | предметные |
| 1. Организационный момент | Приветствует учащихся, организовывает актуализацию требований к учащимся со стороны учебной деятельности | Приветствуют учителя, проверяют свои рабочие места | умение самонастраиваться на деятельность учения |
|
|
| 2. Целеполагание и мотивация | Сообщает учащимся информацию о событиях 1952 г. в Лондоне (Приложение 1, п. 1) и предлагает учащимся ответить на вопросы: 1. Назовите молекулярную формулу сернистого газа, о котором шла речь в сообщении. 2. Назовите и напишите формулу еще одного оксида серы. 3. Какие кислоты соответствуют перечисленным оксидам? Предлагает сформулировать тему и цель урока. | Отвечают на вопросы и формулируют тему и цель урока | умение использовать экологическое мышление для выбора стратегии собственного поведения в качестве одной из ценностных установок | умение структурировать знания, умение ставить и формулировать проблему | умение объяснять функции веществ в связи с их строением |
| 3. Актуализация знаний и умений | Проводит мини-опрос по плану: 1. Электронные и структурные формулы оксидов серы. 2. Характер оксидов серы, их свойства в ОВР. 3. Классификация сернистой и серной кислот по признакам: а) наличие или отсутствие кислорода, б) по основности, в) по степени диссоциации, г) по растворимости, д) по летучести, е) по стабильности. 4. Типы и названия солей, образуемых сернистой и серной кислотами. | Отвечают на вопросы, делают записи в свои опорные конспекты | умение самонастраиваться на коммуникативную деятельность, связанную с учением | умение устанавливать причинно-следственные связи, строить логическое рассуждение, умозаключение и делать выводы | умение объяснять свойства веществ на основе их строения |
| 4. Усвоение новых знаний и способов действия | Предлагает учащимся назвать возможные пути поступления сернистого газа в атмосферу и оценить степень его влияния на экологию, исходя из его физико-химических свойств.
Затем предлагает рассмотреть рис. 1 «Химические превращения сернистого газа в атмосфере» (Приложение 1, п. 2) и записать уравнения реакций. Для ОВР расставить коэффициенты методом электронного баланса.
Предлагает рассмотреть уравнения реакций, взятых из работ учащихся, писавших контрольную работу, и дать мотивированный ответ, какие из этих уравнений верны, в каких допущены небольшие погрешности, а какие записаны совершенно неправильно (Приложение 1, п. 3).
Предлагает сделать вывод о химических свойствах оксидов серы и соответствующих им растворов кислот. Акцентирует внимание на двух последних реакциях, являющихся качественными на сульфит- и сульфат ионы. | Называют пути поступления SO2 в атмосферу и оценивают степень его влияния на экологию планеты. Записывают уравнения реакции в опорных конспектах. Проверяют уравнения реакций, исправляют ошибки. Делают вывод о том, что оксидам серы присущи все свойства, характерные для кислотных оксидов, а растворы сернистой и серной кислот проявляют все свойства, характерные для кислот. Делают вывод о их поведении в ОВР. | умение убеждать других людей в необходимости овладения стратегией рационального природопользования
умение самонастраиваться на перемену деятельности
умение давать самооценку в ходе учения | умение оценивать правильность выполнения учебной задачи, собственные возможности ее решения, умение создавать обобщения, устанавливать аналогии. | умение характеризовать экологические проблемы, стоящие перед человечеством умение составлять уравнения химических реакций, подтверждающие свойства веществ, умение составлять электронный баланс для ОВР, умение раскрывать генетические связи между классами веществ |
| 5. Осознание и осмысление учебной информации | Предлагает провести учащимся лабораторные опыты по очистке сточных вод сернокислотного производства (Приложение 1, п. 4) и предлагает записать уравнения реакций, составить полные и сокращенные ионные уравнения. Предлагает решить задачу с целью подготовки к ОГЭ по очистке сточных вод аккумуляторного завода (Приложение 1, п. 5) с целью совершенствования навыка расчета массовой доли вещества в растворе. Предлагает выполнить задание (Приложение 1, п. 6) с целью подготовки к ОГЭ. После выполнения задания, отмечает, что уравнение реакции второй стадии используется для очистки отходящих газов теплоэлектростанций от сернистого газа. | Выполняют лабораторные опыты, акцентируют внимание на признаках реакций, записывают уравнения реакций в опорных конспектах, знакомятся со способами очистки сточных вод и отходящих газов различных производств | умение соотносить новые знания с уже имеющимся личностным опытом | умение работать индивидуально и в группе, умение оценивать правильность выполнения учебной задачи, собственные возможности ее решения | умение проводить простейшие химические эксперименты, умение раскрывать генетические связи между различными классами веществ, умение находить массовую долю вещества в растворе |
| 6. Контроль и самооценка знаний и способов действия | Проводит тестовую работу (Приложение 1, п.7). Затем предлагает учащимся обменяться с соседом по парте работами и проверить работу друг друга. После этого осуществляется проверка тестовой работы с помощью слайда презентации. | Работают с тестом, проверяют самостоятельно работу соседа по парте и проводят самопроверку с использованием слайда | умение ставить индивидуально-значимую цель, умение давать самооценку в ходе учения | умение работать индивидуально, умение оценивать правильность выполнения учебной задачи, собственные возможности ее решения | умение создавать причинно-следственные связи между составом, строением, свойствами и применением веществ |
| 7. Подведение итогов занятия, информация о домашнем задании. | Подводит итоги урока и предлагает просмотреть задачи и упражнения домашнего задания, условие которых приведено в опорном конспекте. Отмечает, что учащиеся сами могут выбирать из предложенного перечня задания для его выполнения (Приложение 1, п.8). | Знакомятся с домашним заданием. | умение делать выбор из предложенных преподавателем заданий с учётом своих индивидуальных возможностей | умение структурировать знания, умение планировать свою индивидуальную образовательную траекторию. | умение составлять уравнения химических реакций, умение решать задачи по отработанным алгоритмам |
| 8. Рефлексия | Предложить учащимся карточки с заданием «Продолжить фразу» (Приложение 1, п.9) | Оценивают свою работу на уроке | умение оценивать степень успешности своей индивидуальной образовательной деятельности | умение давать оценку процессов и результатов деятельности | умение выявлять взаимосвязанность химии, как науки, и практической стороны ее реализации |
Приложение 1
1. 5 декабря 1952 г. в Лондоне возник густой туман, в котором происходило медленное образование аэрозоля серной кислоты. Эта смесь получила название «смог» (от англ. smoke – дым и fog – туман). За 4 суток лондонский смог погубил более 4 тыс. человек. Английские специалисты определили, что в этом смоге содержалось несколько сотен тонн дыма и сернистого газа. Была зафиксирована прямая, непосредственная связь между концентрацией в воздухе этих веществ и смертностью населения.
2.
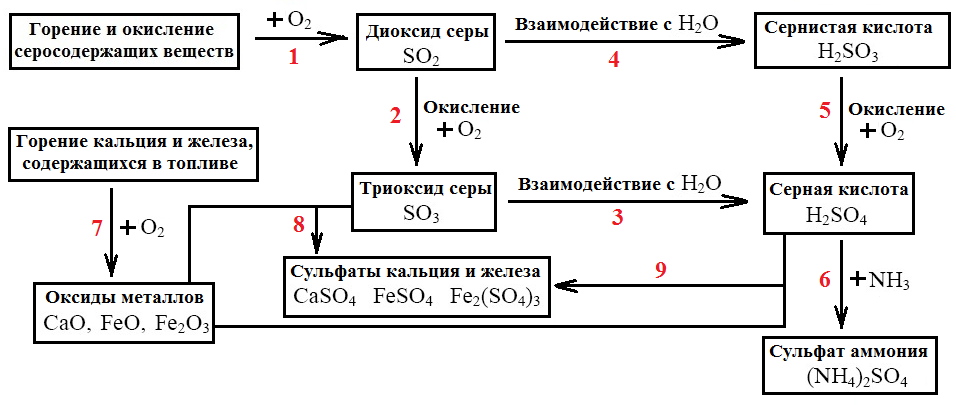
Рис. 1. Химические превращения сернистого газа в атмосфере.
| 1. S + O2 SO2 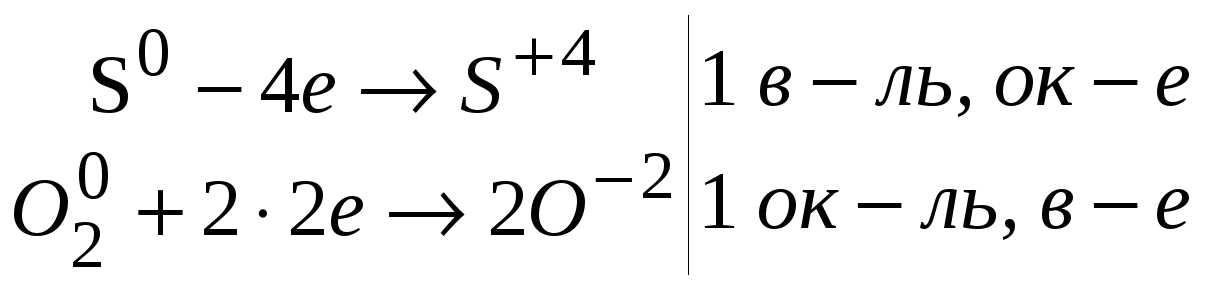
| 2. 2SO2 + O2 2SO3 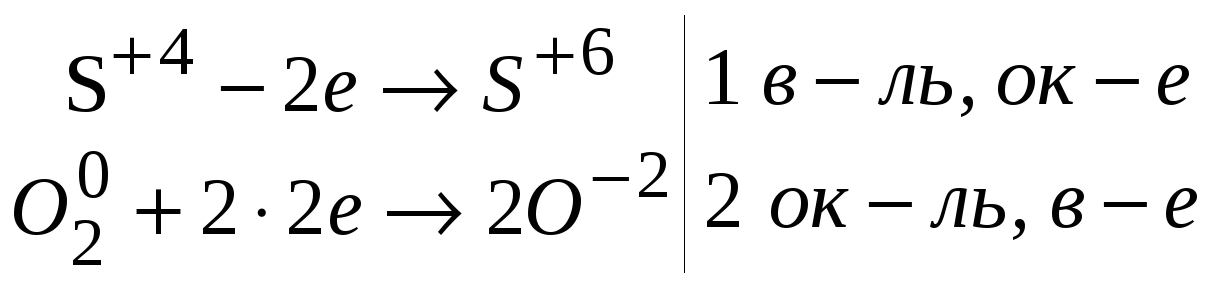
|
| 3. SO3 + H2O H2SO4 | 4. SO2 + H2O H2SO3 |
| 5. 2H2SO3 + O2 2H2SO4 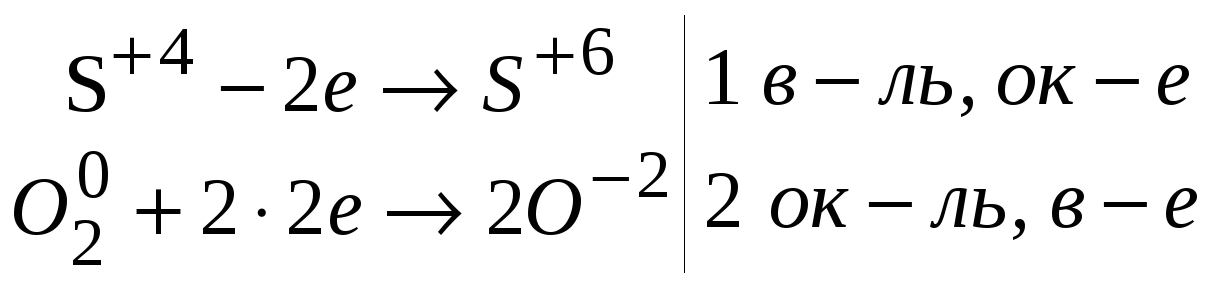
| 6. H2SO4 + 2NH3 (NH4)2SO4 |
| 7. 2Ca + O2 2CaO 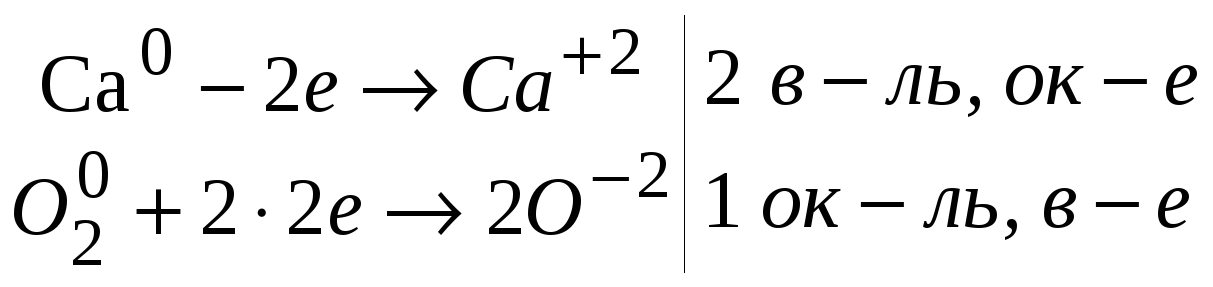
|
| 8. CaO + SO3 CaSO4 FeO + SO3 FeSO4 Fe2O3 + 3SO3 Fe2(SO4)3
| 2Fe + O2 2FeO 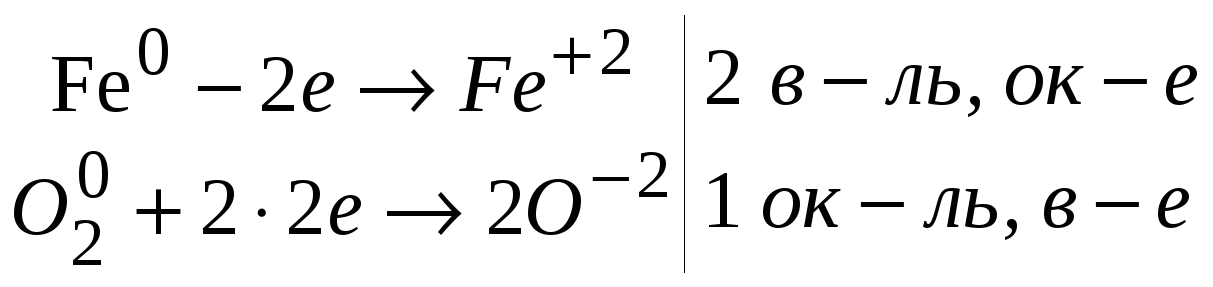
|
| 9. CaO + H2SO4 CaSO4 + H2O FeO + H2SO4 FeSO4 + H2O Fe2O3 + 3H2SO4 Fe2(SO4)3 + 3H2O | 4Fe + 3O2 2Fe2O3 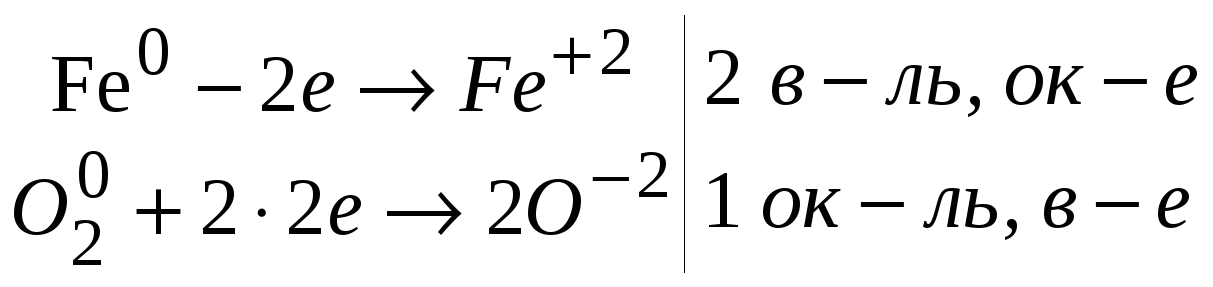
|
3. Ниже приведены уравнения реакций взятые из работ учащихся, писавших контрольную работу. Дайте мотивированный ответ, какие из этих уравнений верны, в каких допущены небольшие погрешности, а какие записаны совершенно неправильно:
1) NaOH + SO2 = Na2SO3 + Н2О
2) SO2 + Br2 + H2O = H2SO4 + HBr
3) SO2 + 4CO = 4CO2 + S
4) Zn + H2SO4 (раствор) = ZnSO4 + Н2↑
5) Сu + H2SO4 (раствор) = СuSO4 + Н2↑
6) Сu(ОН)2 + H2SO4 (раствор) = СuSO4 + Н2О
7) NaNO3 + H2SO4 (раствор) = Na2SO4 + HNO3
8) К2SO3 + H2SO4 (раствор) = K2SO4 + SO2 + Н2О
9) BaCl2 + H2SO4 (раствор) = BaSO4 + HCl
Сделайте вывод о химических свойствах оксидов серы и соответствующих им растворов кислот.
4. Сточные воды, содержащие минеральные кислоты или щелочи, перед сбросом их в водоемы или перед использованием в технологических процессах нейтрализуют. Для нейтрализации минеральных кислот применяется любой щелочной реагент, чаще всего известковое молоко, карбонаты кальция и магния в виде суспензии. Проведите нейтрализацию выданных вам образцов сточных вод сернокислотного производства предложенными реактивами и составьте уравнения реакций в молекулярной, полной ионной и сокращенно-ионной форме.
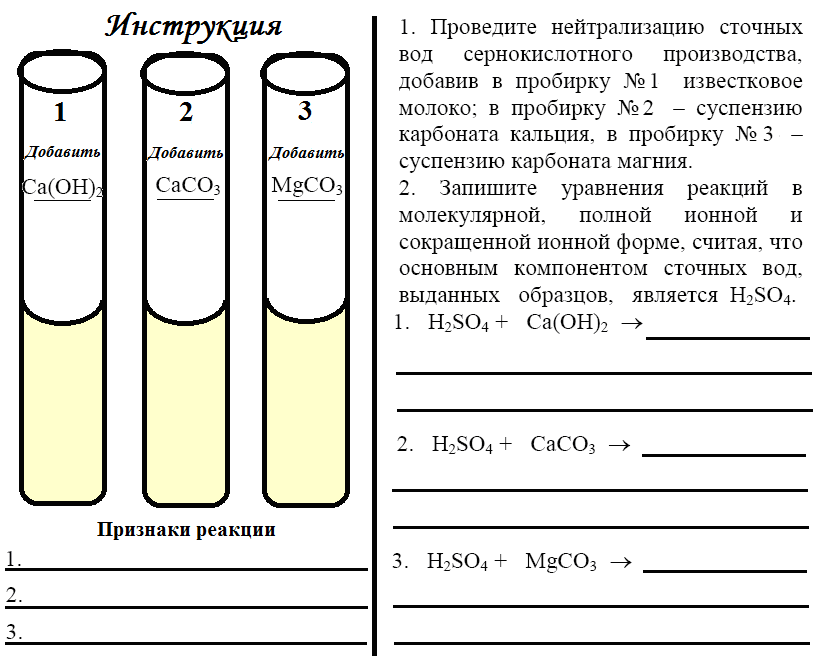
5. Для очистки сточных вод аккумуляторного завода, содержащих сульфат свинца (II), используют фильтры, в состав которых входит магнезитовый щебень состава MgCO3. Составьте уравнение реакции и вычислите массовую долю сульфата свинца (II) в 160 г сточных вод, если после прохождения фильтра произошло выпадение осадка в количестве 18 г.
| Дано: m(сточных вод) = 160 г m(осадка) = 18 г
Найти: (PbSO4) = ? | Решение:
PbSO4 + MgCO3 = PbCO3 + MgSO4
1. Количество вещества PbCO3: 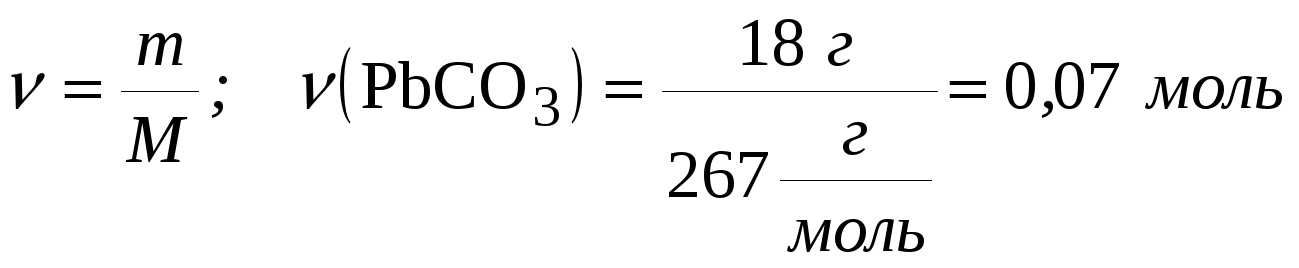
|
| 2. Согласно уравнению реакции, (PbSO4) = (PbCO3) = 0,07 моль. 3. Масса сульфата свинца (II) в исходном растворе сточных вод:  4. Массовая доля сульфата свинца (II) в исходном растворе сточных вод: 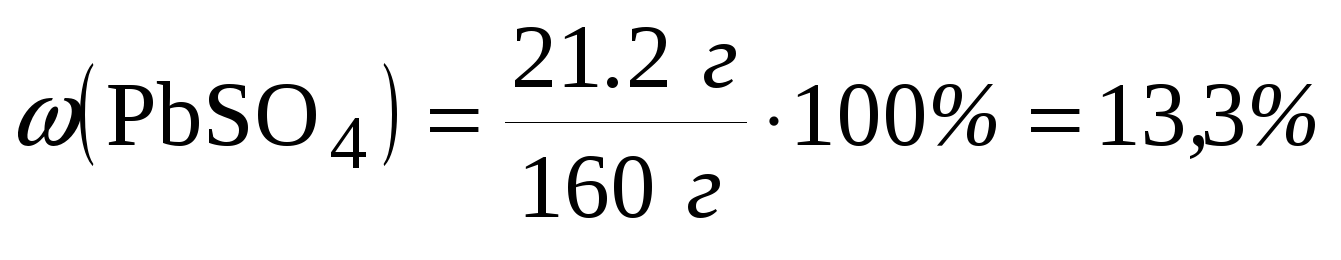 Ответ: 13,3%. |
6. Даны вещества: FeS, H2SO4 (раствор), Fe, SO2, NaOH, CuSO4.
Используя воду и необходимые вещества только из этого списка, получите в две стадии простое вещество – серу. Запишите уравнения проведённых химических реакций. Опишите признаки этих реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
Решение:
FeS + H2SO4 (раствор) = FeSO4 + H2S - выделение газа с запахом «тухлых яиц»
2H2S(раствор) + SO2 3S + 2Н2О – образование желтого осадка элементарной серы.
Сокращённое ионное уравнение первой реакции:
5) FeS + 2H+ = Fe2+ + H2S
7. Мини-тест
| Вопрос | Варианты ответов |
| 1. В результате взаимодействия каких оксидов с водой в атмосфере образуются кислотные дожди? | 1) оксидов серы и азота |
| 2) оксидов азота и фосфора |
| 3) оксидов серы и углерода |
| 4) оксидов фосфора и углерода |
| 2. Вещества, формулы которых – SO2 и CaSO4, являются соответственно | 1) основным оксидом и солью |
| 2) кислотным оксидом и кислотой |
| 3) основным оксидом и основанием |
| 4) кислотным оксидом и солью |
| 3. Как называется процесс кипячения сточной воды, в процессе которого в пар переходит вода и летучие вещества, а минеральные соли остаются в кубе? | 1) фильтрация |
| 2) дистилляция |
| 3) ректификация |
| 4) очистка |
| 4. В молекуле оксида серы (VI) химическая связь | 1) ионная |
| 2) ковалентная полярная |
| 3) ковалентная неполярная |
| 4) металлическая |
| 5. Какой газ высвобождается при выплавке меди из руды Cu2S? | 1) Н2S |
| 2) CO2 |
| 3) SO3 |
| 4) SO2 |
| 6. В каком соединении степень окисления серы равна +6? | 1) Na2S |
| 2) H2SO3 |
| 3) Al2(SO4)3 |
| 4) SO2 |
| 7. Укажите кислоту средней силы, существующей только в водном растворе. | 1) H2SO3 |
| 2) HNO3 |
| 3) H2SO4 |
| 4) HCl |
| 8. Одинаковое число молей катионов и анионов образуется при полной диссоциации в водном растворе 1 моль | 1) H2SO4 |
| 2) (NH4)2S |
| 3) CuSO4 |
| 4) Н2S |
8. Рефлексия
Предложить учащимся карточки с заданием «Продолжить фразу»:
- Мне было интересно…
- Мы сегодня разобрались….
- Я сегодня понял, что…
- Мне было трудно…
- На следующем уроке я хочу…
9. Домашнее задание.
Задача № 1. Отработанный травильный раствор для стальных заготовок содержит 4,5% серной кислоты. Сколько негашеной извести CaO потребуется для нейтрализации 200 г этого стока.
Задача № 2. Основным загрязнителем окружающей среды является металлургическое производство. Так, при обжиге серосодержащих руд в атмосферу попадает большой объем сернистого газа SO2, который окисляется кислородом до оксида серы (VI) SO3, а затем, соединяясь с водяным паром, образует серную кислоту Н2SO4, что приводит к появлению «кислотных дождей». Составьте уравнения описанных реакций и вычислите массу серной кислоты, образуемой из 100 л оксида серы (IV).
Задача №3. Один из методов, предложенных для удаления SO2 из отходящих газов теплоэлектростанций, заключается в реакции диоксида серы с водным раствором сероводорода, идущий с образованием серы. Какой объем газообразного сероводорода потребуется для удаления SO2, образующегося при сжигании 500 кг угля, в котором содержится 3,5% серы?
Упражнение. На основе данных, представленных в таблице 1, составьте уравнения возможных реакций диссоциации, ионного обмена, протекающих в стоке сточных вод различных производств до и после прохождения фильтрующего материала.
| Происхождение стока | Примеси в стоке | Фильтрующий материал | Уравнения реакций |
| Сток травильной ванны гальванического цеха | FeSO4, Fe2(SO4)3 | Доломитовая крошка |
|
| Стоки промывного цеха по производству серной кислоты | H2SO4, H2SO3, Fe2(SO4)3 | Известняк |
|
Список литературы
1. Голдовская Л.Ф. Химия окружающей среды: Учебник для вузов. – М.: Мир, 2005. – 296 с.
2. Чекмарева Л.И. Химия окружающей среды: Методические указания к практическим занятиям и контрольные задания для студентов-заочников дистанционной формы обучения по специальности 280201.65 «Охрана окружающей среды и рациональное использование природных ресурсов». – Хабаровск: Изд-во ТОГУ, 2011. – 53 с.
3. Штриплинг Л.О., Туренко Ф.П. Основы очистки сточных вод и переработки твердых отходов. Учебное пособие – Омск: Изд-во ОмГТУ, 2005. – 192 с.
2