
«КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ»

Комплексные соединения - это частицы (нейтральные молекулы
или ионы), которые образуются в результате присоединения к данному иону
(или атому), называемому комплексообразователем, нейтральных молекул
или других ионов, так называемые лиганды.
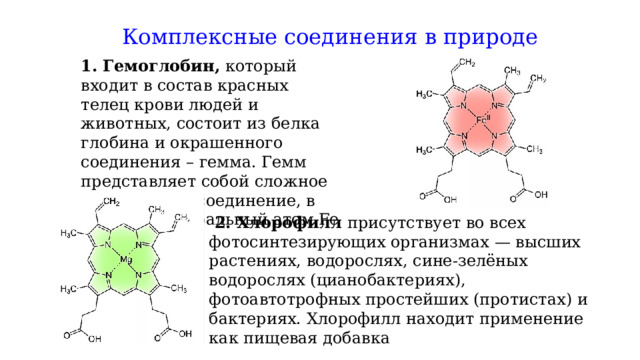
Комплексные соединения в природе
1. Гемоглобин, который входит в состав красных телец крови людей и животных, состоит из белка глобина и окрашенного соединения – гемма. Гемм представляет собой сложное комплексное соединение, в котором центральный атом Fe (+2)
2. Хлорофилл присутствует во всех фотосинтезирующих организмах — высших растениях, водорослях, сине-зелёных водорослях (цианобактериях), фотоавтотрофных простейших (протистах) и бактериях. Хлорофилл находит применение как пищевая добавка
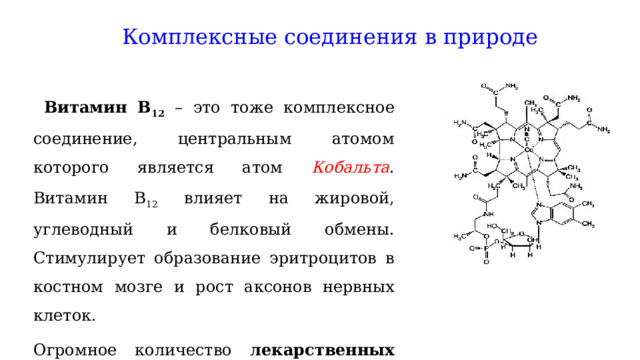
Комплексные соединения в природе
Витамин В 12 – это тоже комплексное соединение, центральным атомом которого является атом Кобальта . Витамин В 12 влияет на жировой, углеводный и белковый обмены. Стимулирует образование эритроцитов в костном мозге и рост аксонов нервных клеток.
Огромное количество лекарственных препаратов представляют собой комплексные соединения.
![Комплексные соединения в природе минералы Гранат (Fe,Mn) 3 Al 2 [SiO 4 ] 3 Изумруд Be 3 Al 2 [Si 6 O 18 ] Бирюза CuAl 6 (OH) 8 [PO 4 ] 4](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img4.jpg)
Комплексные соединения в природе
минералы
Гранат (Fe,Mn) 3 Al 2 [SiO 4 ] 3
Изумруд
Be 3 Al 2 [Si 6 O 18 ]
Бирюза CuAl 6 (OH) 8 [PO 4 ] 4
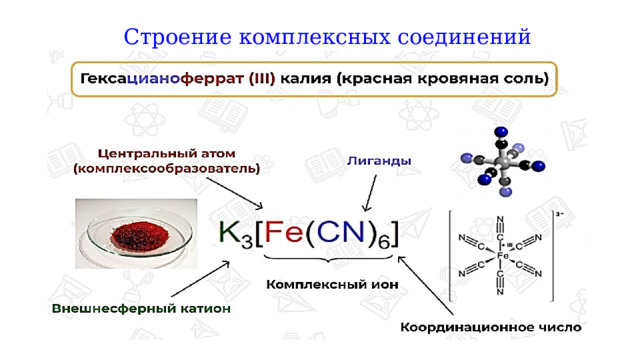
Строение комплексных соединений
![Классификация комплексных соединений По составу: соли (например, K 3 [Fe(CN) 6 ] соли (например, K 3 [Fe(CN) 6 ] основания (например, [Ag(NH 3 ) 2 ]OH) кислоты (например, H[AuCl 4 ]) основания (например, [Ag(NH 3 ) 2 ]OH) кислоты (например, H[AuCl 4 ]) 2. По заряду внутренней сферы : катионный (например, [Cu(NH 3 ) 4 ] 2+ SO 4 2- ) анионнай (например, K 3 + [Fe(CN) 6 ] 3- ) катионный (например, [Cu(NH 3 ) 4 ] 2+ SO 4 2- ) анионнай (например, K 3 + [Fe(CN) 6 ] 3- ) нейтральный (например, [Cu(NH 3 ) 4 ] 2+ [PtCl 4 ] 2- ) катионно-анионный (например, [PtCl 4 (NH 3 ) 2 ] 0 ) нейтральный (например, [Cu(NH 3 ) 4 ] 2+ [PtCl 4 ] 2- ) катионно-анионный (например, [PtCl 4 (NH 3 ) 2 ] 0 )](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img6.jpg)
Классификация комплексных соединений
- соли (например, K 3 [Fe(CN) 6 ]
- соли (например, K 3 [Fe(CN) 6 ]
- основания (например, [Ag(NH 3 ) 2 ]OH) кислоты (например, H[AuCl 4 ])
- основания (например, [Ag(NH 3 ) 2 ]OH)
- кислоты (например, H[AuCl 4 ])
2. По заряду внутренней сферы :
- катионный (например, [Cu(NH 3 ) 4 ] 2+ SO 4 2- ) анионнай (например, K 3 + [Fe(CN) 6 ] 3- )
- катионный (например, [Cu(NH 3 ) 4 ] 2+ SO 4 2- )
- анионнай (например, K 3 + [Fe(CN) 6 ] 3- )
- нейтральный (например, [Cu(NH 3 ) 4 ] 2+ [PtCl 4 ] 2- ) катионно-анионный (например, [PtCl 4 (NH 3 ) 2 ] 0 )
- нейтральный (например, [Cu(NH 3 ) 4 ] 2+ [PtCl 4 ] 2- )
- катионно-анионный (например, [PtCl 4 (NH 3 ) 2 ] 0 )
![Реакции образования комплексных соединений Комплексные соединения обычно получают действием избытка лигандов на содержащее комплексообразователь соединение. Координационное число, как правило, в 2 раза больше степени окисления комплексообразователя. Из этого правила бывают, однако, исключения. Образование гидроксокомплексов: AlCl 3 + 6NaOH (изб) = Na 3 [Al(OH) 6 ] + 3NaCl AlCl 3 + 4NaOH (изб) = Na[Al(OH) 4 ] + 3NaCl ZnSO 4 + 4NaOH (изб) = Na 2 [Zn(OH) 4 ] + Na 2 SO 4](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img7.jpg)
Реакции образования комплексных соединений
Комплексные соединения обычно получают действием избытка лигандов на содержащее комплексообразователь соединение. Координационное число, как правило, в 2 раза больше степени окисления комплексообразователя. Из этого правила бывают, однако, исключения.
Образование гидроксокомплексов:
AlCl 3 + 6NaOH (изб) = Na 3 [Al(OH) 6 ] + 3NaCl
AlCl 3 + 4NaOH (изб) = Na[Al(OH) 4 ] + 3NaCl
ZnSO 4 + 4NaOH (изб) = Na 2 [Zn(OH) 4 ] + Na 2 SO 4
![Реакции разрушения комплексных соединений действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода: действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода: действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода: К 3 [Al(OH) 6 ] + 6HCl (изб) = 3KCl + AlCl 3 + 6H 2 O нагревания некоторых комплексных соединений: нагревания некоторых комплексных соединений: нагревания некоторых комплексных соединений: [Cu(NH 3 ) 4 ]SO 4 → CuSO 4 + 4NH 3 ↑ Na 3 [Al(OH) 3 ] → Na 3 AlO 3 + 3H 2 O окислительно-восстановительных реакций: окислительно-восстановительных реакций: окислительно-восстановительных реакций: 2Na[Ag(CN) 2 ] + Zn = Na 2 [Zn(CN) 4 ] + 2Ag 6K 4 [Fe(CN) 6 ] +K 2 Cr 2 O 7 +7H 2 SO 4 =6K 3 [Fe(CN) 6 ]+Cr 2 (SO 4 ) 3 +4K 2 SO 4 +7H 2 O](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img8.jpg)
Реакции разрушения комплексных соединений
- действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода:
- действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода:
- действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода:
К 3 [Al(OH) 6 ] + 6HCl (изб) = 3KCl + AlCl 3 + 6H 2 O
- нагревания некоторых комплексных соединений:
- нагревания некоторых комплексных соединений:
- нагревания некоторых комплексных соединений:
[Cu(NH 3 ) 4 ]SO 4 → CuSO 4 + 4NH 3 ↑
Na 3 [Al(OH) 3 ] → Na 3 AlO 3 + 3H 2 O
- окислительно-восстановительных реакций:
- окислительно-восстановительных реакций:
- окислительно-восстановительных реакций:
2Na[Ag(CN) 2 ] + Zn = Na 2 [Zn(CN) 4 ] + 2Ag
6K 4 [Fe(CN) 6 ] +K 2 Cr 2 O 7 +7H 2 SO 4 =6K 3 [Fe(CN) 6 ]+Cr 2 (SO 4 ) 3 +4K 2 SO 4 +7H 2 O
![Применение комплексных соединений Гальванические покрытия – защита одного металла другим. Например, медное покрытие крепко соединяется с железом, если использовать в процессе комплексные соединения. Электролитическое получение металлов. Например, алюминий в расплаве криолита образует комплекс Nа 3 [AlF 6 ]. Из расплавов соединений комплексных солей получают такие металлы, как Nb, Tl, Th, Mg. Защита металлов от коррозии. Ингибиторы – комплексные соли, где лигандами выступают и органические вещества.](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img9.jpg)
Применение комплексных соединений
- Гальванические покрытия – защита одного металла другим. Например, медное покрытие крепко соединяется с железом, если использовать в процессе комплексные соединения.
- Электролитическое получение металлов. Например, алюминий в расплаве криолита образует комплекс Nа 3 [AlF 6 ]. Из расплавов соединений комплексных солей получают такие металлы, как Nb, Tl, Th, Mg.
- Защита металлов от коррозии. Ингибиторы – комплексные соли, где лигандами выступают и органические вещества.
![Применение комплексных соединений • Аналитическая химия. Многие индикаторы, реактивы, которые помогают распознать вещества, ионы и даже заряды ионов, – комплексные соединения. Катион Fe 2+ можно распознать в реакции с гексацианоферратом(III) калия: FeCl 2 + K 3 [Fe(CN) 6 ] = KFe[Fe(CN) 6 ] + 2 KCl образуется синий осадок (турнбулева синь). Катион Fe 3+ можно распознать гексацианоферратом(II) калия: 4FeCl 3 + 3K 4 [Fe(CN) 6 ] = Fe 4 [Fe(CN 6 )] 3 + 12KCl Образуется темно-синий осадок (берлинская лазурь)](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img10.jpg)
Применение комплексных соединений
- • Аналитическая химия. Многие индикаторы, реактивы, которые помогают распознать вещества, ионы и даже заряды ионов, – комплексные соединения. Катион Fe 2+ можно распознать в реакции с гексацианоферратом(III) калия:
FeCl 2 + K 3 [Fe(CN) 6 ] = KFe[Fe(CN) 6 ] + 2 KCl
образуется синий осадок (турнбулева синь).
Катион Fe 3+ можно распознать гексацианоферратом(II) калия:
4FeCl 3 + 3K 4 [Fe(CN) 6 ] = Fe 4 [Fe(CN 6 )] 3 + 12KCl
Образуется темно-синий осадок (берлинская лазурь)
![Применение комплексных соединений Получение металлов. Например золота: золотой песок растворяется в растворе цианида натрия (NaCN) в присутствии кислорода и воды, потому что образуется очень устойчивое комплексное соединение золота: 4Au + O 2 + 2H 2 O + 8NaCN = 4Na[Au(CN) 2 ] + 4NaOH. Из полученного комплекса золото вытесняют цинком: Zn + 2Na[Au(CN) 2 ] = Na 2 [Zn(CN) 4 ] + 2Au Фотографический процесс также немыслим без комплексных соединений. Комплексные соединения платины, Co(III), Fe(III) используются в химиотерапии при лечении раковых заболеваний и влияют на развитие раковых клеток](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img11.jpg)
Применение комплексных соединений
- Получение металлов. Например золота: золотой песок растворяется в растворе цианида натрия (NaCN) в присутствии кислорода и воды, потому что образуется очень устойчивое комплексное соединение золота:
4Au + O 2 + 2H 2 O + 8NaCN = 4Na[Au(CN) 2 ] + 4NaOH.
Из полученного комплекса золото вытесняют цинком:
Zn + 2Na[Au(CN) 2 ] = Na 2 [Zn(CN) 4 ] + 2Au
- Фотографический процесс также немыслим без комплексных соединений.
- Комплексные соединения платины, Co(III), Fe(III) используются в
химиотерапии при лечении раковых заболеваний и влияют на развитие
раковых клеток











![Комплексные соединения в природе минералы Гранат (Fe,Mn) 3 Al 2 [SiO 4 ] 3 Изумруд Be 3 Al 2 [Si 6 O 18 ] Бирюза CuAl 6 (OH) 8 [PO 4 ] 4](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img4.jpg)

![Классификация комплексных соединений По составу: соли (например, K 3 [Fe(CN) 6 ] соли (например, K 3 [Fe(CN) 6 ] основания (например, [Ag(NH 3 ) 2 ]OH) кислоты (например, H[AuCl 4 ]) основания (например, [Ag(NH 3 ) 2 ]OH) кислоты (например, H[AuCl 4 ]) 2. По заряду внутренней сферы : катионный (например, [Cu(NH 3 ) 4 ] 2+ SO 4 2- ) анионнай (например, K 3 + [Fe(CN) 6 ] 3- ) катионный (например, [Cu(NH 3 ) 4 ] 2+ SO 4 2- ) анионнай (например, K 3 + [Fe(CN) 6 ] 3- ) нейтральный (например, [Cu(NH 3 ) 4 ] 2+ [PtCl 4 ] 2- ) катионно-анионный (например, [PtCl 4 (NH 3 ) 2 ] 0 ) нейтральный (например, [Cu(NH 3 ) 4 ] 2+ [PtCl 4 ] 2- ) катионно-анионный (например, [PtCl 4 (NH 3 ) 2 ] 0 )](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img6.jpg)
![Реакции образования комплексных соединений Комплексные соединения обычно получают действием избытка лигандов на содержащее комплексообразователь соединение. Координационное число, как правило, в 2 раза больше степени окисления комплексообразователя. Из этого правила бывают, однако, исключения. Образование гидроксокомплексов: AlCl 3 + 6NaOH (изб) = Na 3 [Al(OH) 6 ] + 3NaCl AlCl 3 + 4NaOH (изб) = Na[Al(OH) 4 ] + 3NaCl ZnSO 4 + 4NaOH (изб) = Na 2 [Zn(OH) 4 ] + Na 2 SO 4](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img7.jpg)
![Реакции разрушения комплексных соединений действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода: действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода: действия любой сильной кислоты на гидрокомплексы; в этом случае образуется соль и вода: К 3 [Al(OH) 6 ] + 6HCl (изб) = 3KCl + AlCl 3 + 6H 2 O нагревания некоторых комплексных соединений: нагревания некоторых комплексных соединений: нагревания некоторых комплексных соединений: [Cu(NH 3 ) 4 ]SO 4 → CuSO 4 + 4NH 3 ↑ Na 3 [Al(OH) 3 ] → Na 3 AlO 3 + 3H 2 O окислительно-восстановительных реакций: окислительно-восстановительных реакций: окислительно-восстановительных реакций: 2Na[Ag(CN) 2 ] + Zn = Na 2 [Zn(CN) 4 ] + 2Ag 6K 4 [Fe(CN) 6 ] +K 2 Cr 2 O 7 +7H 2 SO 4 =6K 3 [Fe(CN) 6 ]+Cr 2 (SO 4 ) 3 +4K 2 SO 4 +7H 2 O](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img8.jpg)
![Применение комплексных соединений Гальванические покрытия – защита одного металла другим. Например, медное покрытие крепко соединяется с железом, если использовать в процессе комплексные соединения. Электролитическое получение металлов. Например, алюминий в расплаве криолита образует комплекс Nа 3 [AlF 6 ]. Из расплавов соединений комплексных солей получают такие металлы, как Nb, Tl, Th, Mg. Защита металлов от коррозии. Ингибиторы – комплексные соли, где лигандами выступают и органические вещества.](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img9.jpg)
![Применение комплексных соединений • Аналитическая химия. Многие индикаторы, реактивы, которые помогают распознать вещества, ионы и даже заряды ионов, – комплексные соединения. Катион Fe 2+ можно распознать в реакции с гексацианоферратом(III) калия: FeCl 2 + K 3 [Fe(CN) 6 ] = KFe[Fe(CN) 6 ] + 2 KCl образуется синий осадок (турнбулева синь). Катион Fe 3+ можно распознать гексацианоферратом(II) калия: 4FeCl 3 + 3K 4 [Fe(CN) 6 ] = Fe 4 [Fe(CN 6 )] 3 + 12KCl Образуется темно-синий осадок (берлинская лазурь)](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img10.jpg)
![Применение комплексных соединений Получение металлов. Например золота: золотой песок растворяется в растворе цианида натрия (NaCN) в присутствии кислорода и воды, потому что образуется очень устойчивое комплексное соединение золота: 4Au + O 2 + 2H 2 O + 8NaCN = 4Na[Au(CN) 2 ] + 4NaOH. Из полученного комплекса золото вытесняют цинком: Zn + 2Na[Au(CN) 2 ] = Na 2 [Zn(CN) 4 ] + 2Au Фотографический процесс также немыслим без комплексных соединений. Комплексные соединения платины, Co(III), Fe(III) используются в химиотерапии при лечении раковых заболеваний и влияют на развитие раковых клеток](https://fsd.multiurok.ru/html/2025/09/24/s_68d41239a0c1e/img11.jpg)










