Тема: Кремний и его соединения.
| Цели урока: ОБРАЗОВАТЕЛЬНЫЕ: обеспечить в ходе урока усвоение химических и физических свойств кремния его соединений, их получение, распространение в природе, их значение для человека. выработка умений и навыков: обращения с лабораторным оборудованием, текстом учебника, дополнительной литературой; проводить наблюдения, систематизировать и обобщать знания, делать выводы. ВОСПИТАТЕЛЬНЫЕ всестороннее развитие личности: формирование умений ставить цели, выделять главное, планирование своей деятельности при работе в группе; осуществлять самоконтроль, подводить итоги, работать в оптимальном темпе, беречь время; воспитание эмоционально – ценностного отношения к миру. РАЗВИВАЮЩАЯ обеспечить условия для развития познавательного интереса и интеллектуальных способностей, развития творческих способностей детей; |
Средства обучения: периодическая система химических элементов Д. И. Менделеева, схемы, коллекции, «Природные силикаты», «Стекло и изделия из стекла», дополнительная литература, лабораторное оборудование, презентация к уроку, химические реактивы: раствор соляной кислоты, раствор карбоната натрия, раствор силикатного клея; штативы с пробирками; образцы природных соединений кремния ( гранит, горный хрусталь, кварц и др.), образцы изделий из стекла, фаянса, фарфора, керамики.
Ход урока:
1.Организационный момент.
-Здравствуйте, ребята! Садитесь. Сегодня у нас открытый урок и у нас на уроке присутствуют гости. Давайте мы им улыбнемся и пожелаем доброго дня. На уроке мы с вами повторим пройденный материал, познакомимся с темой «Кремний и его соединения», решим задачи, проведем опыты.
2. Повторение пройденной темы.
-На предыдущих уроках мы с вами познакомились с углеродом и с его соединениями. Давайте, мы с вами повторим. Для этого выполним задания ГИА.
Задание № 1. (А)
Число электронов во внешнем электронном слое атома с зарядом ядра +6 равно:
1) 6 2) 3 3) 4 4) 2
Задание № 2
Кислотным оксидом является:
1) CO2 2)Al2 O3 3) Na 2O 4) NO
Задание № 3
Оксид углерода (IV) взаимодействует с
1) NaCl 2) P2 O5 3) Ca(OH)2 4) HNO3
Задание № 4 (В 1)
В ряду химических элементов Ge – Si – C
увеличиваются радиусы атомов
увеличивается электроотрицательность
усиливаются кислотные свойства их высших оксидов
возрастает значение высшей степени окисления
увеличивается число электронов во внешнем электронном слое атомов
Задание № 5 (С2)
К избытку карбоната кальция добавили 146 г раствора с массовой долей соляной кислоты 5 %. Вычислите объем (н.у.) выделившегося газа.
Ответ: 2,24 л.
Молодцы, ребята!
3. Целеполагание. Новая тема.
Вступительное слово учителя. В одной из своих книг А.Е. Ферсман рассказывал: «Показывают мне самые разнообразные предметы: прозрачный шар, сверкающий на солнце чистотой холодной ключевой воды; красивый, пестрого рисунка агат; яркой игры многоцветный опал; чистый песок на берегу моря; тонкую, как шелковинка, нитку из плавленого кварца или жаропрочную посуду из него; красиво ограненные груды горного хрусталя; грубо обработанный наконечник стрелы древнего человека… - все это одно и то же химическое соединение элементов кремния и кислорода» (SiO2)
А также персональные компьютеры, мобильные телефоны. А из чего же сделана начинка всех электронных устройств, процессоры и чипы, флэшки и сим-карты? Все сделаны из вещества – имя которому – кремний. Кремний – символ высоких технологий.
Учитель формулирует цель учебного занятия, исходя из темы урока.
Тема урока: Кремний и его соединения
1.Строение.
Кремний – элемент IV группы и 3-го периода, порядковый номер 14, А=28, 14 протонов и 14 нейтронов, 14 электронов. Строение его электронной оболочки следующая: 14 Si 2e 8e 4e
3. Открытие кремния.
(материал по этому вопросу может быть подготовлен и освещён обучающимися)
Кремний – самый распространенный элемент земной коры, причем последняя на 75% состоит из соединений кремния. В человеческом организме кремний есть почти повсеместно, больше всего в костях, коже, соединительной ткани. При переломах костей содержание кремния в месте перелома возрастает почти в 50 раз.
Нельзя сказать, что роль кремния в жизни выяснена уже окончательно, скорее наоборот. Установлено, что с возрастом содержание этого элемента в костной ткани, артериях, коже существенно уменьшается.
Б) Историческая справка.
Кремний в свободном виде был выделен в 1811 Ж.Гей-Люссаком и Л.Тенаром при пропускании паров фторида кремния над металлическим калием, однако он не был описан ими как элемент. Шведский химик Й.Берцелиус в 1823 дал описание кремния, полученного им при обработке калиевой соли K2SiF6 металлическим калием при высокой температуре. Новому элементу было дано название "силиций" (от лат. silex - кремень)
С греческого языка «кремнос» - утёс, скала.
4. Физические свойства (слайд 12)
(материал по этому вопросу может быть подготовлен и освещён учащимися)
- Вы обратили внимание, что когда мы говорим о содержании в природных условиях элемента кремния, то упоминаем только его соединения, но не простое вещество.
Кремний в свободном виде в природе не встречается в отличие от углерода (алмаз, графит, аморфный С и т.д.)
кремний – неметалл, существует в кристаллическом и аморфном виде.
Кристаллический кремний – серовато-стального цвета с металлическим блеском, твёрдый (7 баллов по шкале Мооса), но хрупкий, малореакционноспособный; полупроводник, (с повышением температуры электропроводность повышается), и с нарушением правильности структуры.
Такие свойства обусловлены строением кристаллов, аналогичным структуре алмаза.
Физические константы: g = 2,33 г/см3; t пл.= 1415 0С; t кип.= 3500 0С
Аморфный кремний представляет собой белый порошок.
5. Получение кремния (слайд 13)
- Способы получения кремния основаны в основном на восстановлении оксида кремния (IV) сильными восстановителями – активными металлами (Mg, Al) и углеродом.
Лабораторный способ: SiO2 + 2Mg = 2MgO + Si
Промышленный способ:
1900oC
S iO2 + 2C 2CO + Si
iO2 + 2C 2CO + Si
SiCi4 + 2Zn = 2ZnCi2 + Si
6. Химические свойства (слайд 14)
а) кремний - восстановитель
Все реакции протекают при нагревании!
Si + O2 = SiO2 (оксид кремния (IV))
S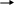 i0 – 4e- Si+4 восстановитель
i0 – 4e- Si+4 восстановитель
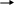 O2 + 4e- 2O-2 окислитель
O2 + 4e- 2O-2 окислитель
Si + 2Cl2 = SiCl4 (хлорид кремния)
Si + 2S = SiS2 (сульфид кремния)
20000C
S
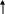 i + C Si+4C-4 (карбид кремния или карборунд, по твёрдости близок к алмазу)
i + C Si+4C-4 (карбид кремния или карборунд, по твёрдости близок к алмазу)
S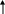 i + 2H2O(пар) = SiO2 + H2
i + 2H2O(пар) = SiO2 + H2
Si + 2NaOH(конц.) + H2O = Na2SiO3 + 2H2
б) кремний – окислитель
Si + 2Ca = Ca2Si (силицид кальция)
Вывод: свойства кремния и углерода похожи. Оба неметалла взаимодействуют с кислородом, галогенами, серой, металлами. Но в отличие от углерода кремний напрямую не соединяется с водородом.
7. Соединения кремния
Свойства кремнезёма (слайд15,16)
Учитель подробно рассматривает свойства оксида кремния (IV) и проводит сравнительный анализ двух оксидов – SiO2 и CO2. результаты обсуждения в виде таблицы выводятся на экран.
Обратите внимание на одно важное свойство оксида кремния:
SiO2 + 4HF = 2H2O + SiF4
Оксид кремния входит в состав стекла, поэтому плавиковую кислоту нельзя хранить в стеклянной посуде.
Вывод: физические свойства оксидов резко отличаются, т.к. они образуют разные кристаллические решётки – молекулярную (CO2) и атомную (SiO2), но химические свойства схожи. Отличие состоит в различном отношении к воде.
Силан SiH4 (слайд 17)
-
 Силан получают косвенно, действуя на силициды металлов водой или кислотами:
Силан получают косвенно, действуя на силициды металлов водой или кислотами:
Mg2Si + 4H2O = 2Mg(OH)2 + SiH4
Силан – бесцветный газ, самовоспламеняющийся на воздухе и сгорающий с образованием оксида кремния и воды:
SiH4 + 2O2 = SiO2 + 2H2O
Кремниевая кислота и её соли (слайд 18)
-кремниевая кислота H2SiO3 -единственная нерастворимая неорганическая кислота, - двухосновная,
- слабая H2SiO3 H2O +SiO2
слабая H2SiO3 H2O +SiO2
При высыхании образует силикагель, используемый в качестве адсорбента.
Получить кремниевую кислоту можно только из её солей.
Лабораторная работа: «Ознакомление с образцами природных силикатов»
Рассмотрите выданные образцы природных силикатов. Обратите внимание на внешний вид. Проверьте их твердость.
I. SiO2 - оксид кремния (IV), песок, кварц, кремень – нерастворимое в воде твердое вещество, очень тугоплавкое, tпл. =17000 С. Атомная кристаллическая решетка.
Кварц – белый – горный хрусталь – поделочный камень;
Молочный, серый, дымчатый – опал, агат, яшма, халцедон
Кремень – имеет очень острые края; в древности изготавливали орудия труда и оружие.
Химические свойства: SiO2 - кислотный оксид
1) При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов с образованием солей — силикатов:
SiO2 + CaO → CaSiO3
SiO2 + 2NaOH → Na2SiO3 + H2O
SiO2 + CaCO3 → CaSiO3 + CO2
SiO2 + K2CO3 → K2SiO3 + CO2
2) С водой не реагирует
3) Окислительно — восстановительные реакции
Взаимодействие с металлами
При температуре выше 1000 °С реагирует с активными металлами,
при этом образуется кремний:
SiO2 + 2Mg → Si + 2MgO
II. H2SiO3 – кремниевая кислота.
Оксид кремния – песок, нерастворимый в воде. Следовательно, получить кремниевую кислоту растворением ее соответствующего оксида в воде невозможно. Ставится проблемный вопрос: «Как получить кремниевую кислоту?» H2SiO3 — очень слабая (слабее угольной), непрочная, в воде малорастворима (образует коллоидный раствор).
Получение кремниевой кислоты:
Na2SiO3 + 2HCl → 2NaCl + H2SiO3
При нагревании разлагается:
H2SiO3 –t°→ H2O + SiO2
Соли кремниевой кислоты – силикаты. Обычно они нерастворимы в воде, исключения составляют силикаты натрия и калия, их называют «жидким стеклом». Силикаты широко распространены в природе. Свойства силикатов различны в зависимости от их состава и строения, очень часто они имеют красивую окраску, некоторые из них используются в ювелирном деле (гранат, топаз, изумруд).
Лабораторный опыт: Качественные реакции на силикат-ион (Повторение ТБ).
Ход работы: Обнаружение силикат-иона. В пробирку налейте 1 мл силиката натрия прилейте по каплям раствор соляной кислоты. Что наблюдаете? Сделайте вывод о способе обнаружения силикат-ионов?
8. Применение соединений кремния в народном хозяйстве (слайды 20,21,22)
Для получения полупроводников.
Кислотоупорных сплавов.
Стекло, цемент, бетон, железобетон, кирпич, фарфор, фаянс.
Закрепление.
Работа с учебником.
Задание № 4, стр. 185
Напишите уравнения реакций с помощью которых можно осуществить следующие превращения:
SiO 2 - Si - Ca 2 Si - SiH 4 - SiO 2 - Si
9. Заключительные выводы (слайд 23)






 iO2 + 2C 2CO + Si
iO2 + 2C 2CO + Si  i0 – 4e- Si+4 восстановитель
i0 – 4e- Si+4 восстановитель i + C Si+4C-4 (карбид кремния или карборунд, по твёрдости близок к алмазу)
i + C Si+4C-4 (карбид кремния или карборунд, по твёрдости близок к алмазу) i + 2H2O(пар) = SiO2 + H2
i + 2H2O(пар) = SiO2 + H2










