Конспект урока по химии в 9 классе
«Производство серной кислоты.».
Учитель ЧОУ «Средняя школа “Возрождение”»
Абасова Тамара Джабраиловна.
Дата проведения: 07.02.2022.

Тип урока:
урок изучения нового материала.
Цель:
1. На примере производства серной кислоты продолжить формирование понимания роли химии в развитии цивилизации.
2. Повышение эрудированности школьников в химии
Задачи урока:
Учащиеся должны познакомиться с производством серной кислоты, рассмотреть основные стадии производственного процесса. Знать и уметь написать уравнения реакций, лежащих в основе получения серной кислоты.
Оборудование:
На каждый стол:
1. индикатор настроения - химический стакан, в котором лежат вырезанные разноцветные кружочки с изображением грустного, равнодушного или улыбающегося лица.
2. конверт с карточками, на которых весь процесс производства серной кислоты разбит на отдельные мелкие фрагменты (см. приложение 1)
3. клей
4. бумага (альбомная или формата А4)
5. дополнительная литература: учебники других авторов, тезаурус.
Методы и приемы проведения урока:
Ученикам предложена на выбор самостоятельная работа, работа в парах или группах.
Принцип формирования групп:
коммуникативные качества (дети добровольно выбирают с кем они будут работать)
Ход урока
1. Мотивационный момент.
Учитель: Здравствуйте! Как ваше настроение? Для ответа выберите из стаканчика – индикатора тот кружок, который соответствует вашему настроению. Ребята, вы любите приключения?
Ученики: (как правило) Да!
Учитель: Значит, вы читали роман «Таинственный остров». Автор Жюль Верн. В этом романе группа людей, потерпев катастрофу воздушного корабля, попадает на необитаемый остров. Они не имеют с собой никаких запасов и инструментов, поэтому, используя свои научные и технические знания, создают цивилизацию заново. Далее зачитывается отрывок из названного романа о работе химической лаборатории и о производстве серной кислоты. Сообщается, для чего она нужна и как в дальнейшем используется колонистами.
2. Изучение нового материала:
Учитель: сегодня на уроке мы познакомимся с современным способом производства серной кислоты. Ваша задача, разбившись на группы, пары или работая самостоятельно, из этих карточек составить производственную схему. При составлении схемы используйте материал § 22 с. 104 – 106, а также дополнительную литературу. (Можно раздать или положить на отдельный стол).
При самостоятельном изучении материала учитель наблюдает за работой учеников, отвечает на возникающие вопросы, направляет деятельность учащихся.
3. Завершение урока:
Учитель: Ребята до конца урока осталось 5 минут, давайте подведем итоги. Вам понравилось сегодня на уроке? Что не понравилось? Что нового вы узнали?
Ученики: (выражают свое отношение к уроку)
Учитель: Ваше настроение изменилось? Воспользуйтесь индикатором настроения еще раз. Все, кто хочет получить отметку, сдайте свои работы на проверку, кто не успел наклеить в схему все карточки, может взять схему домой.
На доске записаны вопросы для домашнего задания. Прочтите их. Выберите себе задание.
До свидания!
Приложение 1.
Фигуры для индикатора настроения:



Приложение 2 Вопросы для домашнего задания
Приготовьте сообщение:
Получил ли Сайрос Смитт серную кислоту?
Почему говорят, что серная кислота – кровь химии.
Приложение 3.
(Перед уроком разрезать и положить в конверт).
| Выбор сырья и его подготовка | Сырье: S, H2S, FeS2 | Очистка полученного SO2 |
| Обжиг колчедана - гетерогенная реакция | SO2 осушают в сушильной башне | обжиг колчедана FeS2 проводят в кипящем слое |
| для увеличения поверхности соприкосновения руду измельчают | Сушильная башня заполнена керамическими кольцами | очищенный и осушенный газ SO2 подогревают в теплообменнике |
| H2SO4 конц. в поглотительную башню подают сверху, а газ SO3 снизу (противотоком) | В контактном аппарате происходит окисление оксида серы (IV) в оксид серы (VI) | В контактном аппарате на полочках -решетках размещают слоями катализатор V2O5 |
| для увеличения поверхности соприкосновения газа SO2 и концентрированной серной кислоты | Очистка от крупной пыли происходит в циклоне, электрофильтр служит для очистки от мелкой пыли | Поглотительная башня для увеличения поверхности соприкосновения заполнена керамическими кольцами |
| Вторая стадия | Третья стадия | Первая стадия |
| Получение SO2 | Получение H2SO4 | Получение SO3 |
| В сушильную башню конц. H2SO4. подают сверху,а газ SO2 снизу (противотоком) | Полученный олеум направляется на склад готовой продукции | SO3 растворяют в концентрированной серной кислоте |
| SO3 + Н2О = H2SO4 + Q | V2O5 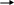 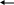 2SO2 + О2 2SO3 + Q 2SO2 + О2 2SO3 + Q
| 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q |











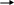
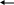 2SO2 + О2 2SO3 + Q
2SO2 + О2 2SO3 + Q









