Контрольная работа №2: Металлы
Вариант 1
1. Установите правильную последовательность. Характеристика элемента – металла:
1 – сравнение свойств простого вещества со свойствами простых веществ – соседних элементов по подгруппе;
2 – строение атома;
3 – состав и характер высшего гидроксида элемента;
4 – положение элемента в ПС Д. И. Менделеева;
5 – состав и характер высшего оксида элемента;
6 – характер простого вещества;
7 – сравнение свойств простого вещества со свойствами простых веществ – соседних элементов по периоду.
2. Ряд элементов, относящихся к металлам:
1 – Ca, Zn, B;
2 – Al, Cr, Fe;
3 – B, As, S;
4 – H, Na, P
3. Установите соответствие.
Характер оксида: Формула:
1. Основный а) CrO3
2. Амфотерный б) CrO
в) Cr2O3
4. Выпишите номер правильного ответа. Изменения, происходящие в периоде ПС с увеличением заряда ядер атомов:
1 – усиление металлических свойств и увеличение степени окисления;
2 – усиление металлических свойств и уменьшение степени окисления;
3 – ослабление металлических свойств и увеличение степени окисления;
4 – ослабление металлических свойств и уменьшение степени окисления.
5. Установите соответствие. Сокращенное ионное уравнение реакции:
1) H2ZnO2 + 2OH- = ZnO22- + 2H2O;
2) Be(OH)2 + 2H+ = Be2+ + 2H2O
Молекулярное уравнение реакции:
А) Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O;
Б) Be(OH)2 + 2NaOH = Na2BeO2 + 2H2O;
В) Be(OH)2 + 2HCl = BeCl2 + 2H2O;
Г) H2ZnO2 + 2KOH = K2ZnO2 + 2H2O
6. Дополните. Химическая связь, обусловливающая электро- и теплопроводность металлов, - … .
7. Установите соответствие.
Признак классификации: Группы металлов:
1. Плотность а) мягкие и твердые;
2. Твердость б) плохо и хорошо проводящие ток;
в) легкие и тяжелые;
г) легкоплавкие и тугоплавкие.
8. Установите соответствие (дополнит.)
Признак классификации: Вид сплава:
1. Легирующие добавки а) чугун, сталь;
2. Состав сплавов б) медный, алюминиевый;
в) однородные и неоднородные;
г) легированная сталь.
9. Особые свойства стали:
1).твердость, коррозионная стойкость;
2) устойчивость к воздействию кислот.
Изделия:
а) детали дробильных установок, железнодорожные рельсы;
б) инструменты, резцы, зубила;
в) детали самолетов, ракет, судов, химическая аппаратура;
г) трансформаторы, кислотоупорные аппараты.
10. Установите правильную последовательность.
Сплав –
1 – состоящий
2 – из которых по крайней мере
3 – металл,
4 – материал
5 – или более компонентов,
6 – один –
7 –с характерными свойствами,
8 – из двух
11. Установите соответствие.
Схема реакции: Продукты реакции:
1) Li + O2 → а) → Fe3O4 + H2;
2) Hg + O2 → б) → реакция не идет;
3) Fe + H2O → в) → Li2O;
г) → HgO;
д) → LiOH + H2;
е) → Fe3O4
12. Коэффициент перед формулой восстановителя в реакции, схема которой
Ca + HNO3 конц → Ca(NO3)2 + N2 + H2O
равен … .(1 балл)
Расставьте коэффициенты в уравнении ОВР методом электронного баланса.* (Полный ответ – 3 балла).
13. Формулы кислот, на которые не распространяются правила применения электрохимического ряда напряжений металлов, - … .
14. Дополните. (Полное решение – 2 балла)
Для выплавки 200 кг нержавеющей стали, содержащей 12% хрома и 10% никеля, необходимо … кг хрома и … кг никеля.
15. Выпишите номер правильного ответа.
В ряду металлов K – Na – Li слева направо:
1 – возрастает температура плавления и возрастает плотность;
2 – возрастает температура плавления и убывает плотность;
3 – убывает температура плавления и возрастает плотность;
4 – убывает температура плавления и убывает плотность.
16. Выпишите номер правильного ответа.
Скорость образования водорода в реакции, схема которой 2М + 2Н2О → 2МОН + Н2↑, если металлы взяты в последовательности Na – K – Li:
1 – возрастает;
2 – не изменяется;
3 – убывает.
17. Осуществить превращение: (3 балла)
Ва → ВаО → Ва(ОН)2 → BaSO4.
Реакцию №3 представить в молекулярном и ионном виде (2 балла)
18. Пара реагентов, характеризующих амфотерные свойства гидроксида алюминия:
1 – NaOH и H2SiO3
2 – H3SiO3 и H2SO4
3 – H2SO4 и KOH
4 – KOH и NaOH
19. Дополните. (Полное решение – 3 балла)
Масса железа, полученного при восстановлении красного железняка массой 5 т, содержащего 15% пустой породы, оксидом углерода (II) СО при массовой доле выхода железа 0,8, равна … .
Контрольная работа №2: Металлы
Вариант 2
1. Установите правильную последовательность. Амфотерный оксид -
1 – проявляет
2 – который в зависимости
3 – или основные
4 – свойства
5 – оксид
6 – кислотные
7 – от условий.
2. Ряд элементов, не относящихся к металлам:
1 – Ca, Zn, B;
2 – Al, Cr, Fe;
3 – B, As, S;
4 – H, Na, P
3. Установите соответствие.
С. О. элемента-металла Свойства оксида:
1. Высшая а) кислотные
2. Промежуточная б) основные
в) амфотерные
4. Выпишите номер правильного ответа. Изменения, происходящие в периоде ПС с уменьшением заряда ядер атомов:
1 – усиление металлических свойств и увеличение степени окисления;
2 – усиление металлических свойств и уменьшение степени окисления;
3 – ослабление металлических свойств и увеличение степени окисления;
4 – ослабление металлических свойств и уменьшение степени окисления.
5. Установите соответствие. Сокращенное ионное уравнение реакции:
1) H2ZnO2 + 2H+ = Zn2+ + 2H2O;
2) Be(OH)2 + 2ОH- = BeО22- + 2H2O
Молекулярное уравнение реакции:
А) Zn(OH)2 + H2SO4 = ZnSO4 + 2H2O;
Б) Be(OH)2 + 2NaOH = Na2BeO2 + 2H2O;
В) Be(OH)2 + 2HCl = BeCl2 + 2H2O;
Г) H2ZnO2 + 2KOH = K2ZnO2 + 2H2O
6. Дополните. Химическая связь, обусловливающая металлический блеск и пластичность металлов, - … .
7. Установите соответствие.
Признак классификации: Группы металлов:
1.Температура плавления а) мягкие и твердые;
2.Электропроводность б) плохо и хорошо проводящие ток;
в) легкие и тяжелые;
г) легкоплавкие и тугоплавкие.
8. Установите соответствие (дополн.)
Признак классификации: Вид сплава:
1. Состояние компонентов а) чугун, сталь;
2. Содержание неметалла б) медный, алюминиевый;
в) однородные и неоднородные;
г) легированная сталь.
9. Особые свойства стали:
1) твердость, механическая прочность, устойчивость против ударов и трения;
2) жаростойкость, механическая прочность при высоких температурах, коррозионная стойкость.
Изделия:
а) детали дробильных установок, железнодорожные рельсы;
б) инструменты, резцы, зубила;
в) детали самолетов, ракет, судов, химическая аппаратура;
г) трансформаторы, кислотоупорные аппараты.
10. Установите правильную последовательность.
Сплав –
1 – из двух
2 – один –
3 – материал
4 – с характерными свойствами
5 – из которых по крайней мере
6 – металл,
7 – или более компонентов
8 – состоящий
11. Установите соответствие.
Схема реакции: Продукты реакции:
1) Li + Н2О → а) → Fe3O4 + H2;
2) Fe + O2 → б) → реакция не идет;
3) Hg + Н2O → в) → Li2O;
г) → HgO;
д) → LiOH + H2;
е) → Fe3O4
12. Коэффициент перед формулой восстановителя в реакции, схема которой
Ca + HNO3 конц → Ca(NO3)2 + N2 + H2O
равен … .( 1балл)
Расставьте коэффициенты в уравнении ОВР методом электронного баланса.* (Полный ответ – 3 балла)
13.Названия группы металлов, на которые не распространяются правила применения электрохимического ряда напряжений металлов, - … .
14. Дополните. (Полное решение – 3 балла)
Масса железа, полученного из красного железняка Fe2O3 массой 80 кг, содержащего 30% примесей, алюмотермическим методом при массовой доле выхода железа 95%, равна … .
15. Выпишите номер правильного ответа.
В ряду металлов Li – Na – K слева направо:
1 – возрастает температура плавления и возрастает плотность;
2 – возрастает температура плавления и убывает плотность;
3 – убывает температура плавления и возрастает плотность;
4 – убывает температура плавления и убывает плотность.
16. Выпишите номер правильного ответа.
Скорость образования водорода в реакции, схема которой 2М + 2Н2О → 2МОН + Н2↑, если металлы взяты в последовательности Li – K – Na:
1 – возрастает;
2 – не изменяется;
3 – убывает.
17. Осуществить превращение: (3 балла)
Са → СаО → Са(ОН)2 → СaSO4.
Реакцию №3 представить в молекулярном и ионном виде (2 балла)
18. Пара формул реагентов, которые взаимодействуют с оксидом алюминия как амфотерным соединением:
1 – NaOH и H2SiO3
2 – H3SiO3 и H2SO4
3 – H2SO4 и KOH
4 – KOH и NaOH
19. Дополните (Полное решение – 3 балла)
Масса гашенной извести СаО, полученной из известняка СаСО3 массой 3 т, содержащего 25% примесей, равна …т.
Контрольная работа №2: Металлы
Ответы:
Вариант 1
| 1 1 балл | 2 1 балл | 3 1 балл | 4 1 балл | 5 2 балла | 6 1 балл | 7 1 балл | 8доп 1 балл | 9 1 балл | 10 1 балл |
| 4271635
| 2 | 1б 2в
| 3 | 1г 2в
| металлич | 1в 2а
| 1г 2б | 1б 2г
| 36815724
|
| 11 3 балла | 12 1 балл 3 балла | 13 1 балл | 14 2 балла
| 15 1 балл | 16 1 балл | 17 3 балла 2 балла | 18 1 балл | 19 3 балла |
|
| 1в 2г 3а
| 5 | Серная конц. H2SO4, азотная HNO3 кислоты
| 24 и 20
| 2 | 1 | - | 3 | 2,0 |
|
Вариант 2
| 1 1балл | 2 1 балл | 3 1 балл | 4 1 балл | 5 2 балла | 6 1 балл | 7 1 балл | 8 доп 1 балл | 9 1 балл | 10 1 балл |
| 4267153
| 3 | 1а 2в | 2 | 1а 2б
| маталлич | 1г 2б
| 1в 2а
| 1а 2в
| 47126853
|
| 11 3 балла | 12 1 балл 3 балла | 13 1 балл | 14 3 балла | 15 1 балл | 16 1 балл | 17 3 балла 2 балла | 18 1 балл | 19 3 балла |
|
| 1д 2е 3б
| 5 | щелочн | 48 и 40
| 3 | 3 | - | 3 | 1,7 |
|
Максимальное количество баллов 30 баллов
«5» 23 и более
«4» 19 – 22 балл
«3» 13 – 18 баллов
Контрольная работа №3: Подгруппа VII и VI групп.
Вариант 1
1. Установите правильную последовательность. Усиление окислительных свойств.
1 - Cl2
2 - I2
3 - F2
4 - Br2
Выпишите номер правильного ответа (1 балл за каждый правильный ответ).
2. Признак протекания реакции между хлором и раствором бромида калия:
1 – выделение газа;
2 – выпадение осадка;
3 – появление бурой окраски;
4 – растворение осадка.
3. Электроотрицательность галогенов в ряду F, Cl, Br, I:
1 – возрастает;
2 – не изменяется;
3 – убывает.
4. Пара формул соединений хлора со степенью окисления +5:
1 – HClO и KClO2;
2 – KClO2 и KClO3;
3 – KClO3 и HClO3;
4 – HСlO3 и HClO.
5. Дополните (Полный ответ – 2 балла).
Объем хлора, необходимого для вытеснения всего брома из 206 гр 10%-ного раствора бромида натрия, равен … л.
6. Увеличение степени диссоциации кислот:
1 - HCl
2 - HF
3 - HI
4 - HBr
7. Установите соответствие. Сокращенное ионное уравнение:
1. Ag+ + Br- → AgBr;
2. Ag+ + F- → AgF
Признаки реакции:
а) белый осадок;
б) светло-желтый осадок;
в) без изменений;
г) желтый осадок.
8. Выпишите номер правильного ответа. Формулы реагентов для плавиковой кислоты:
1 – Zn;
2 – Zn, CaO;
3 - Zn, CaO, NaOH;
4 - Zn, CaO, NaOH, SiO2.
9. Формула соединения, в котором массовая доля хлора наибольшая:
1 – KClO4;
2 - KClO3;
3 – KClO2;
4 – KClO
10. Дополните (Полный ответ – 2 балла).
Объем хлороводорода, полученного из 44,8 л Cl2 и 22,4 л Н2, равен … л.
11. Установите соответствие.
Вещество: Область применения:
1. Фтор а) производство фотобумаги, лечение нервных заболеваний;
2. Бром б) фармацевтическая , химическая промышленность, производство
светочувствительных материалов;
в) ядерная промышленность, электротехника, производство алюминия,
тефлона;
г) получение брома и иода, соляной кислоты, беление бумаги и ткани,
производство красителей, растворителей, синтетического каучука,
волокон, средств защиты растений.
Дополните (1 балла за каждый правильный ответ).
12. Объемная доля кислорода в воздухе составляет …%.
13. Степень окисления кислорода в соединениях, формулы которых Na2O2 и HClO2, равна … и … .
14. Тип реакции, схема которой Р + О2 → (при нагревании), по характеру теплового эффекта … (+Q или -Q).
15. Окраска газообразного кислорода и озона … и … .
16. Выпишите номер правильного ответа.
Промышленный способ получения кислорода:
1 – разложение воды;
2 – разложение пероксида водорода;
3 – перегонка жидкого воздуха;
4 – действие металла на кислоту.
17. Дополните (полный ответ 3 балла).
Объем кислорода, полученного из перманганата калия массой 15,8 гр при объемной доле выхода 0,95, составляет … .
Выпишите номер правильного ответа (1 балла за каждый правильный ответ).
18. Свойство серы как простого вещества:
1 – окислительные;
2 – восстановительные;
3 – окислительные и восстановительные.
19. Физические свойства серы:
1 – твердая;
2 – твердая, желтого цвета;
3 - твердая, желтого цвета, не растворяется в воде;
4 - твердая, желтого цвета, не растворяется в воде, реагирует с металлами.
20. Пара формул соединений со степенью окисления, равной +4:
1 – H2S и Al2S3;
2 - Al2S3 и Na2SO3;
3 - Na2SO3 и SO2;
4 – SO2 и H2S
21. Установите соответствие.
Название соединения: Формула:
1. гидросульфит натрия а) Na2SO3;
2. сульфид натрия б) NaHS;
3. сульфат натрия в) NaHSO4;
г) NaHSO3;
д) Na2S;
е) Na2SO4.
Выпишите номер правильного ответа (1 балла за каждый правильный ответ).
22. Правило разбавления концентрированной серной кислоты:
1 – необходимо вливать воду в кислоту;
2 – необходимо вливать кислоту в воду.
23. Ряд формул реагентов для разбавленного раствора H2SO4:
1 – Fe, Cu, CuO, BaCl2;
2 – Zn, ZnO, Zn(OH)2, BaCl2;
3 – Cu, CuO, Cu(OH)2, BaCl2;
4 – Al, Cu, Cu(OH)2, BaCl2.
24. Схема химических процессов, происходящих при производстве серной кислоты из пирита:
1 – H2S → SO2 → SO3 → H2SO4;
2 - H2S → SO3 → SO2 → H2SO4;
3 – FeS2 → SO3 → SO2 → H2SO4;
4 - FeS2 → SO2 → SO3 → H2SO4.
25. Дополните (полный ответ 3 балла).
Количество вещества оксида серы (IV), выделившегося при взаимодействии 245 гр 80%-го раствора серной кислоты с медью, равно … моль.
Контрольная работа №3: Подгруппа VII и VI групп.
Вариант 2
1. Установите правильную последовательность. Ослабление окислительных свойств.
1 - Cl2
2 - I2
3 - F2
4 - Br2
Выпишите номер правильного ответа (1 балла за каждый правильный ответ).
2. Признак протекания реакции, схема которой:
Cl2 + H2O + AgNO3 →
1 – выделение газа;
2 – выпадение осадка;
3 – появление бурой окраски;
4 – растворение осадка.
3. Неметаллические свойства галогенов в ряду от иода к фтору:
1 – возрастает;
2 – не изменяется;
3 – убывает.
4. Пара формул соединений хлора со степенью окисления -1:
1 – HCl и NaCl;
2 – NaCl и KClO3;
3 – KClO3 и HClO3;
4 – HСlO3 и HCl.
5. Дополните (Полный ответ – 2 балла).
Объем хлора, необходимого для вытеснения всего брома из 20,6 гр 5%-ного раствора бромида натрия, равен … л.
6. Уменьшение степени диссоциации кислот:
1 - HCl
2 - HF
3 - HI
4 - HBr
7. Установите соответствие. Сокращенное ионное уравнение:
1. Ag+ + I- → AgI;
2. Ag+ + Cl- → AgCl
Признаки реакции:
а) белый осадок;
б) светло-желтый осадок;
в) без изменений;
г) желтый осадок.
8. Выпишите номер правильного ответа. Формулы реагентов для соляной кислоты:
1 – Zn;
2 – Zn, CaO;
3 - Zn, CaO, NaOH;
4 - Zn, CaO, NaOH, SiO2.
9. Формула соединения, в котором массовая доля хлора наименьшая:
1 – KClO4;
2 - KClO3;
3 – KClO2;
4 – KClO
10. Дополните (Полный ответ – 2 балла).
Объем хлороводорода, полученного из 22,4 л Cl2 и 44,8 л Н2, равен … л.
11. Установите соответствие.
Вещество: Область применения:
1. Хлор а) производство фотобумаги, лечение нервных заболеваний;
2. Иод б) фармацевтическая , химическая промышленность, производство
светочувствительных материалов;
в) ядерная промышленность, электротехника, производство алюминия,
тефлона;
г) получение брома и иода, соляной кислоты, беление бумаги и ткани,
производство красителей, растворителей, синтетического каучука,
волокон, средств защиты растений.
Дополните (1 балл за каждый правильный ответ).
12. Название самого распространенного элемента на нашей планете - … .
13. Степень окисления кислорода в соединениях HClO и OF2 равна … .
14. Тип реакции, схема которой N2 + O2 → (при нагревании), по характеру теплового эффекта (+Q или -Q) .
15. Название и формула аллотропного видоизменения кислорода - … .
16. Выпишите номер правильного ответа.
Лабораторный способ получения кислорода:
1 – разложение воды;
2 – разложение пероксида водорода;
3 – перегонка жидкого воздуха;
4 – действие металла на кислоту.
17. Дополните (полный ответ 3 балла).
Объем кислорода, полученного из перманганата калия массой 3,16 гр при объемной доле выхода 0,90, составляет … .
Выпишите номер правильного ответа (1 балл за каждый правильный ответ).
18.Все возможные степени окисления серы в соединениях:
1 - -2, 0;
2 - -2, +2;
3 - -2, 0, +4;
4 - -2, 0, +4, +6.
19. Название минерала, содержащего сульфатную форму серы:
1 – киноварь;
2 – гипс;
3 – пирит.
20. Пара формул соединений со степенью окисления, равной -2:
1 – H2S и Al2S3;
2 - Al2S3 и Na2SO3;
3 - Na2SO3 и SO2;
4 – SO2 и H2S
21. Установите соответствие.
Название соединения: Формула:
1. гидросульфат натрия а) Na2SO3;
2. гидросульфид натрия б) NaHS;
3. сульфит натрия в) NaHSO4;
г) NaHSO3;
д) Na2S;
е) Na2SO4.
Выпишите номер правильного ответа (1 балл за каждый правильный ответ).
22. Соли серной кислоты, имеющие наибольшее значение:
1 – глауберова соль, медный купорос;
2 - глауберова соль, гипс;
3 - глауберова соль, гипс, медный купорос;
4 - глауберова соль, гипс, медный купорос, поваренная соль.
23. Ряд формул реагентов для концентрированного раствора H2SO4:
1 – Fe, Cu, CuO, BaCl2;
2 – Zn, ZnO, Zn(OH)2, BaCl2;
3 – Cu, CuO, Cu(OH)2, BaCl2;
4 – Al, Cu, Cu(OH)2, BaCl2.
24. Схема химических процессов, происходящих при производстве серной кислоты из сероводорода:
1 – H2S → SO2 → SO3 → H2SO4;
2 - H2S → SO3 → SO2 → H2SO4;
3 – FeS2 → SO3 → SO2 → H2SO4;
4 - FeS2 → SO2 → SO3 → H2SO4.
25. Дополните (полный ответ 3 балла)
Количество вещества оксида серы (IV), выделившегося при взаимодействии 280 гр 70%-го раствора серной кислоты с медью, равно … моль.
Контрольная работа №3: Подгруппа VII и VI групп.
Ответы
Максимальное количество баллов - 31
«5» более 21 балла
«4» 16 – 20 баллов
«3» 10 – 15 баллов
Вариант 1
| 1 | 2 | 3 | 4 | 5 2балла | 6 | 7 | 8 | 9 | 10 2 балла |
| 3142
| 3 | 3 | 3 | 2 | 2143
| 1б2в | 4 | 4 | 44,8 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 3балла | 18 | 19 | 20 |
| 1в2а | 21 | -1, -2 | экзо | б∕цв, голуб | 3 | 1,06л | 3 | 3 | 3 |
| 21 | 22 | 23 | 24 | 25 3балла |
|
|
|
|
|
| 1г2д3е | 2 | 2 | 4 | 1 моль |
|
|
|
|
|
Вариант 2
| 1 | 2 | 3 | 4 | 5 2балла | 6 | 7 | 8 | 9 | 10 2балла |
| 2413 | 2 | 1 | 1 | 0,1 | 3412 | 1г2а | 3 | 1 | 44,8 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 3балла | 18 | 19 | 20 |
| 1г2б | кислород | -2, +2 | эндо | Озон О3 | 2 | 0,20л | 4 | 2 | 1 |
| 21 | 22 | 23 | 24 | 25 3балла |
|
|
|
|
|
| 1в2б3а | 3 | 3 | 1 | 1 моль |
|
|
|
|
|
Контрольная работа № _________ Дата __________
Тема: ________________________________________________________________
Класс _______________ фамилия, имя ___________________________________
Бланк ответов
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
|
|
|
|
|
|
|
|
|
|
|
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
|
|
|
|
|
|
|
|
|
|
|
| 21 | 22 | 23 | 24 | 25 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Контрольная работа № _________ Дата __________
Тема: ________________________________________________________________
Класс _______________ фамилия, имя ___________________________________
Бланк ответов
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
|
|
|
|
|
|
|
|
|
| | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |
|
|
|
|
|
|
|
|
|
| | 21 | 22 | 23 | 24 | 25 |
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
Контрольная работа № _________ Дата __________ Тема: ________________________________________________________________ Класс _______________ фамилия, имя ___________________________________ Бланк ответов
|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | |
|
|
|
|
|
|
|
|
|
| | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | |
|
|
|
|
|
|
|
|
|
| | 21 | 22 | 23 | 24 | 25 |
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
|
Контрольная работа №4: Подгруппа азота.
Вариант 1
Выпишите номер правильного ответа (1 балл за каждый правильный ответ).
1. Физические свойства азота при комнатной температуре:
1 – бесцветный газ;
2 – бесцветный газ, без запаха;
3 - бесцветный газ, без запаха, малорастворим в воде;
4 - бесцветный газ, без запаха, малорастворим в воде, тяжелее воздуха.
2. Промышленный способ получения азота:
1 – разложение оксида ртути;
2 – перегонка жидкого воздуха;
3 – разложение бертолетовой соли;
4 – разложение нитрита аммония.
3. Места нахождения газообразного азота:
1 – воздух;
2 – воздух, море;
3 - воздух, море, почва;
4 - воздух, море, почва, растения и животные.
4. Условия, смещающие равновесие в системе:
2NO + O2 ↔ 2NO2 + Q влево:
1 – повышение давления и повышение температуры;
2 - повышение давления и понижение температуры;
3 – понижение давления и повышение температуры;
4 – понижение давления и понижение температуры.
5. Формула соединения, массовая доля азота в котором максимальна:
1 – NO;
2 – NO2;
3 – N2O3;
4 – N2O5
6. Физические свойства аммиака (при н. у.):
1 – бесцветный газ;
2 – бесцветный газ с резким запахом;
3 - бесцветный газ с резким запахом, ядовит;
4 - бесцветный газ с резким запахом, ядовит, тяжелее воздуха.
7. Способ собирания аммиака – вытеснение:
1 – воды;
2 – воздуха.
8. Признак, по которому обнаруживают аммиак:
1 – запах;
2 – запах, посинение лакмуса;
3 - запах, посинение лакмуса, белый дым с HClконц;
4 - запах, посинение лакмуса, белый дым с HClконц, обесцвечивание фенолфталеина.
9. Установите правильную последовательность.
Водородная связь -
1 – и атомами
2 – между
3 – элементов
4 – связь
5 – сильно электроотрицательных
6 – атомами водорода
Установите соответствие (2 балла за каждый правильный ответ).
10. Определяемый ион: Реактив, содержащий ион:
1. NH4+ а) OH-;
2. CO32- б) Ag+;
в) H+;
г) SO42-
11. Сокращенное ионное уравнение:
1. 2H+ + CO32- = CO2↑ + H2O;
2. NH4+ + OH- = NH3↑ + H2O
Молекулярное уравнение реакции:
а) (NH4)2SO4 + BaCl2 = BaSO4↓ + 2NH4Cl;
б) NH4Cl + NaOH = NaCl + NH3↑ + H2O;
в) (NH4)2CO3 + 2HCl = 2NH4Cl + CO2↑ + H2O;
г) NH4NO3 + NaOH = NaNO3 + NH3↑ + H2O.
Выпишите номер правильного ответа
12. Качественная реакция на соли аммония:
1 – взаимодействие со щелочами;
2 - взаимодействие со щелочами, разложение при нагревании;
3 - взаимодействие со щелочами, разложение при нагревании, реакции по анионам
13. Области применения солей аммония:
1 – сельское хозяйство;
2 - сельское хозяйство, производство взрывчатых веществ;
3 - сельское хозяйство, производство взрывчатых веществ, кондитерское дело;
4 - сельское хозяйство, производство взрывчатых веществ, кондитерское дело, паяние.
14. Пара металлов, которые не пассивирует концентрированная азотная кислота:
1 – медь и цинк;
2 – цинк и алюминий;
3 – алюминий и железо;
4 – железо и медь.
15. Установите соответствие.
Схема реакции: Продукты реакции:
1. Cu + HNO3 конц → а) Сu(NO3)2 + H2↑;
2. Fe + HNO3 конц → б) Сu(NO3)2 + NO2↑ + H2O;
в) реакция не идет;
г) Сu(NO3)2 + NO↑ + H2O;
д) Fe(NO3)2 + N2O + H2O.
16. Дополните (полный ответ 3 балла).
Масса азотной кислоты, полученной из оксида азота (IV) массой 23 кг при массовой доле выхода 0,95, равна … кг.
Установите соответствие.
17. Аллотропная модификация фосфора:
Белый
Красный
строение и свойства:
а) молекулярная кристаллическая решетка, ядовит;
б) не растворяется в воде и сероуглероде;
в) атомная кристаллическая решетка, не ядовит;
г) светится в темноте.
18. Продукты реакции: Исходные вещества:
1. Ag3PO4↓; а) Ag+ и H2PO4-;
2. 2PH3 + 3Mg2+ б) 3Ag+ и PO43-;
в) P2O5 и Mg(OH)2;
г) Mg3P2 и 6H+
Решить задачи (3 балла за каждую задачу).
19. Масса 80%-й фосфорной кислоты, полученной из фосфора массой 62 кг, равна … .
20. Масса хлорида аммония, полученного при взаимодействии аммиака массой 34 т с раствором, содержащим 36,5 т хлороводорода, равна .. т.
Контрольная работа №4: Подгруппа азота.
Вариант 2
Выпишите номер правильного ответа (1 балл за каждый правильный ответ).
1. Роль азота в реакциях с металлами:
1 – окислитель;
2 – восстановитель.
2. Лабораторный способ получения азота:
1 – разложение оксида ртути;
2 – перегонка жидкого воздуха;
3 – разложение бертолетовой соли;
4 – разложение нитрита аммония.
3. Условия, смещающие равновесие в системе:
2NO + O2 ↔ 2NO2 + Q вправо:
1 – повышение давления и повышение температуры;
2 - повышение давления и понижение температуры;
3 – понижение давления и повышение температуры;
4 – понижение давления и понижение температуры.
4. Формула соединения, массовая доля азота в котором минимальна:
1 – NO;
2 – NO2;
3 – N2O3;
4 – N2O5
5. Дополните. Коэффициент перед формулой окислителя в реакции, схема которой Li + N2 → , равен … .
Выпишите номер правильного ответа.
6. Реагенты для аммиака:
1 – вода;
2 – вода, кислоты;
3 – вода, кислоты, кислород;
4 - вода, кислоты, кислород, щелочь
7. Направление дна сосуда для собирания аммиака
1 – вниз;
2 – вверх
8. Влияние водородной связи на физические свойства веществ:
1 – повышение температуры кипения и повышение температуры плавления;
2 - повышение температуры кипения и понижение температуры плавления;
3 – понижение температуры кипения и повышение температуры плавления;
4 - понижение температуры кипения и понижение температуры плавления.
9. Установите правильную последовательность.
Донорно – акцепторный механизм образования ковалентной связи –
1 – свободной
2 – образование
3 – из атомов
4 – за счет
5 – имеющейся
6 – связи
7 – электронной пары
8 – у одного
Установите соответствие (2 балла за каждый правильный ответ).
10. Определяемый ион: Реактив, содержащий ион:
1. Cl- а) OH-;
2. NH+ б) Ag+;
в) H+;
г) SO42-
11. Сокращенное ионное уравнение:
1. NH4+ + OH- = NH3↑ + H2O;
2. Ba2+ + SO42- = BaSO4↓
Молекулярное уравнение реакции:
а) (NH4)2SO4 + BaCl2 = BaSO4↓ + 2NH4Cl;
б) NH4Cl + NaOH = NaCl + NH3↑ + H2O;
в) (NH4)2CO3 + 2HCl = 2NH4Cl + CO2↑ + H2O;
г) NH4NO3 + NaOH = NaNO3 + NH3↑ + H2O.
12. Выпишите номер правильного ответа.
Химические свойства солей аммония:
1 – разложение при нагревании;
2 - разложение при нагревании, взаимодействие со щелочами;
3 - разложение при нагревании, взаимодействие со щелочами, реакции на анионы.
13. Установите соответствие.
Формула соли: Область применения:
1. NH4NO3 а) кондитерское дело;
2. NH4Cl б) сельское хозяйство;
3. (NH4)2CO3 в) производство взрывчатых веществ;
г) паяние.
14. Пара металлов, которые пассивирует концентрированная азотная кислота:
1 – медь и цинк;
2 – цинк и алюминий;
3 – алюминий и железо;
4 – железо и медь.
15. Установите соответствие.
Схема реакции: Продукты реакции:
1. Al + HNO3 конц → а) Сu(NO3)2 + H2↑;
2. Cu + HNO3 конц → б) Сu(NO3)2 + NO2↑ + H2O;
в) реакция не идет;
г) Сu(NO3)2 + NO↑ + H2O;
д) Al(NO3)3 + N2 + H2O.
16. Дополните (полный ответ 3 балла).
Масса азотной кислоты, полученной из оксида азота (IV) массой 92 кг при массовой доле выхода 0,90, равна … кг.
17. Выпишите номер правильного ответа.
Строение и свойства красного фосфора:
1 - молекулярная кристаллическая решетка, ядовит;
2 - не растворяется в воде и сероуглероде;
3 - атомная кристаллическая решетка, не ядовит;
4 - светится в темноте.
18. Установите соответствие.
Продукты реакции: Исходные вещества:
1. = H2O а) H+ и OH- =;
2. = 2PO43- 3H2O б) O2 и 2H+ =;
в) P2O5 и 6OH- =;
г) P2O3 и 6OH- =.
Решить задачи (3 балла за каждую задачу).
19. Масса 70%-й фосфорной кислоты, полученной из фосфора массой 124 кг, равна …кг.
20. Масса хлорида аммония, полученного при взаимодействии аммиака массой 17 т с раствором, содержащим 73 т хлороводорода, равна .. т.
Контрольная работа №4: Подгруппа азота.
Ответы
Вариант 1
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 2 балла |
| 3 | 2 | 3 | 3 | 1 | 3 | 2 | 3 | 5247163 | 1а 2в |
| 11 2 балла | 12 | 13 | 14 | 15 2 балла | 16 3 балла | 17 2 балла | 18 2 балла | 19 3 балла | 20 3 балла |
| 1в 2бг | 1 | 4 | 1 | 1б 2в | 29,9 кг | 1аг 2бв | 1б 2г | 157 кг | 53,5 |
Вариант 2
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 2 балла |
| 1 | 4 | 2 | 4 | 1 | 3 | 2 | 1 | 41836257 | 1б 2а |
| 11 2 балла | 12 | 13 | 14 | 15 2 балла | 16 3 балла | 17 2 балла | 18 2 балла | 19 3 балла | 20 3 балла |
| 1бг 2а | 3 | 1бв 2г 3а | 3 | 1в 2б | 113,4 кг | 3 | 1а 2в | 274 кг | 53,5 |
Максимальное количество баллов – 31
«5» более 26 баллов
«4» 21 – 25 баллов
«3» 13 – 20 баллов
Итоговая контрольная работа: Химия - 9
На выполнение работы отводится 2 часа (120 минут). Работа состоит из 3 частей и включает 25 заданий.
Часть 1 включает 19 заданий (А1 – А19). К каждому заданию дается 4 варианта ответа, из которых только один правильный. Внимательно прочитайте каждое задание и проанализируйте все варианты предложенных ответов.
Часть 2 состоит из 4 заданий (В1 – В4), на которые нужно дать краткий ответ в виде набора цифр.
Часть 3 включает 2 задания (С1 и С2), выполнение которых предполагает формулирование учащимся полного, развернутого ответа, содержащего необходимые уравнения реакций и расчеты, отражающие ход решения задачи.
Постарайтесь выполнять задания в том порядке, в котором они даны. Для экономии времени пропускайте задание, которое не удается выполнить сразу. Если останется время, вернитесь к пропущенным заданиям.
При выполнении работы вы можете пользоваться периодической системой химических элементов Д.И. Менделеева и таблицей растворимости солей, кислот и оснований в воде.
За выполнение различных по сложности заданий дается один или более баллов. Баллы, полученные вами за выполненные задания, суммируются. Постарайтесь выполнить больше заданий и набрать наибольшее количество баллов.
Часть 1
При выполнении заданий с выбором ответа этой части отметьте Х номер правильного ответа в экзаменационной работе.
А1. Атомы химических элементов бора и алюминия имеют одинаковое число
| 1) | заполненных электронных слоев |
| 2) | протонов |
| 3) | электронов во внешнем электронном слое |
| 4) | нейтронов |
А2. Изменение свойств от металлических к неметаллическим происходит в ряду
| 1) | Ba → Mg → Ca |
| 2) | C → B → Li |
| 3) | Mg → Al → Si |
| 4) | Р → Si → Al |
А3. Ионная связь характерна для
| 1) | оксида кремния |
| 2) | магния |
| 3) | бромида калия |
| 4) | сероводорода |
А4. В каком соединении степени окисления химических элементов равны
– 3 и + 1?
| 1) NF3 | 2) N2O3 | 3) PH3 | 4) AlCl3 |
А5. К кислотным оксидам относится
| 1) | оксид натрия |
| 2) | оксид цинка |
| 3) | оксид углерода (II) |
| 4) | оксид фосфора (V) |
А6. Сумма коэффициентов в уравнении реакции между оксидом натрия и оксидом фосфора (V) равна
А7. Окислительно-восстановительной является реакция, уравнение которой
| 1) | 2Fe(OH)3 = Fe2O3 + 3H2O |
| 2) | CaO + H2O = Ca(OH)2 |
| 3) | 2Al + 3S = Al2S3 |
| 4) | NaOH + HI = NaI + H2O |
А8. С образованием катионов металла и анионов кислотного остатка диссоциирует
| 1) | оксид натрия |
| 2) | гидроксид натрия |
| 3) | азотная кислота |
| 4) | бромид алюминия |
А9. Какое сокращенное ионное уравнение соответствует реакции между нитратом бария и серной кислотой?
| 1) | H+ + NO3- = HNO3 |
| 2) | H+ + OH- = H2O |
| 3) | Ba2+ + SO42- = BaSO4 |
| 4) | Ba2+ + 2NO3- = Ba(NO3)2 |
А10. Оксид меди (II) взаимодействует с
| 1) HNO3 | 2) K2CO3 | 3) Na2O | 4) H2SiO3 |
А11. С гидроксидом калия реагирует каждое из двух веществ
| 1) | оксид серы (VI) и угольная кислота |
| 2) | оксид магния и гидроксид цинка |
| 3) | сероводород и барий |
| 4) | хлороводородная кислота и водород |
А12. С каждым из двух веществ, формулы которых BaCl2 и Cu(OH)2, будет взаимодействовать
| 1) | соляная кислота |
| 2) | фосфорная кислота |
| 3) | азотная кислота |
| 4) | кремниевая кислота |
А13. С раствором нитратом меди (II) может взаимодействовать
| 1) | цинк |
| 2) | гидроксид железа (III) |
| 3) | оксид углерода (IV) |
| 4) | углерод |
А14. Амфотерные свойства проявляют кислородные соединения
| 1) | бериллия |
| 2) | магния |
| 3) | кальция |
| 4) | бария |
А15. Верны ли следующие суждения о чистых веществах и смесях?
А. Молоко является чистым веществом.
Б. Гранит является смесью веществ.
| 1) | верно только А |
| 2) | верно только Б |
| 3) | верны оба суждения |
| 4) | оба суждения неверны |
А16. С помощью фенолфталеина можно распознать
| 1) | хлорид серебра |
| 2) | водород |
| 3) | гидроксид лития |
4) азотную кислоту
А17. Массовая доля кислорода в силикате магния равна
| 1) | 16% 2) 24% 3) 48% 4) 36% |
Часть 2
При выполнении заданий В1 – В4 обведите кружком те варианты ответов, которые вы выбрали как правильные. В ответе запишите последовательность цифр, соответствующих правильным ответам.
В1. В ряду химических элементов Na - Mg - Al:
| 1) | уменьшаются заряды ядер атомов |
| 2) | увеличивается число электронов во внешнем электронном слое |
| 3) | уменьшается радиус атомов |
| 4) | уменьшается электроотрицательность |
| 5) | усиливаются металлические свойства |
Ответ: ________________ .
(Запишите соответствующие цифры в порядке возрастания.)
В2. С оксидом алюминия могут взаимодействовать:
| 1) | серная кислота |
| 2) | хлорид меди (II) |
| 3) | гидроксид железа (III) |
| 4) | медь |
| 5) | оксид углерода (II) |
Ответ: ________________ .
(Запишите соответствующие цифры в порядке возрастания.)
В3. С сульфатом меди (II) реагируют:
| 1) | соляная кислота |
| 2) | водород |
| 3) | свинец |
| 4) | гидроксид бария |
| 5) | оксид кремния |
Ответ: ________________ .
(Запишите соответствующие цифры в порядке возрастания.)
В4. В каких из представленных схем реакций сера является восстановителем?
| 1) | S + O2 → SO2 |
| 2) | S + Cа → CаS |
| 3) | SO3 + Na2O → Na2SO4 |
| 4) | H2S + O2 → SO2 + H2O |
| 5) | H2SO4 + C → SO2 + CO2 + H2O |
Ответ: ________________
Часть 3.
Для ответов на задания этой части используйте специальный бланк ответов №2. Запишите сначала номер задания (С1 и С2), а затем ответ к нему. При выполнении заданий записывайте все уравнения реакций и этапы решения задачи.
C1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Fe2O3 → Fe → X 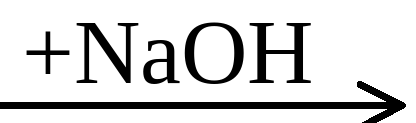 Fe(OH)3
Fe(OH)3
C2. К 200 г 12,25%-ного раствора серной кислоты прилили избыток раствора нитрата бария. Определите массу выпавшего осадка.
Инструкция по проверке и оценке работ учащихся по химии
Часть 1
Задание с выбором ответа считается выполненным верно, если учащийся указал номер правильного ответа. Во всех остальных случаях (выбран другой ответ, выбрано два или больше ответов, среди которых может быть и правильный, ответ на вопрос отсутствует) задание считается невыполненным.
| № задания | Ответ | № задания | Ответ |
| А1 | 3 | А11 | 2 |
| А2 | 2 | А12 | 3 |
| А3 | 2 | А13 | 2 |
| А4 | 2 | А14 | 4 |
| А5 | 4 | А15 | 1 |
| А6 | 1 | А16 | 4 |
| А7 | 4 | А17 | 2 |
| А8 | 2 | А18 | 3 |
| А9 | 3 | А19 | 4 |
| А10 | 1 |
|
Часть 2
Задание с кратким ответом считается выполненным верно, если правильно выбраны два варианта ответа. За полный правильный ответ на задания В1 – В4 ставится 2 балла, за неполный (правильно названы 1 из 2 ответов) – 1 балл, за неверный ответ (или при его отсутствии) – 0 баллов.
| № задания | Ответ | № задания | Ответ |
| В1 | 24 | В3 | 34 |
| В2 | 15 | В4 | 15 |
Часть 3
С1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Fe2O3 → Fe → X 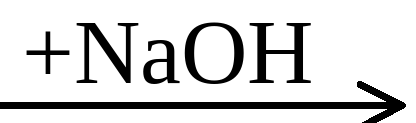 Fe(OH)3
Fe(OH)3
Ответ:
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
| Элементы ответа: Написаны уравнения реакций, соответствующие схеме превращений: 1) Fe2O3 + 3H2 = 2Fe + 3H2O (В качестве восстановителя могут быть использованы CO, Al и др.) 2) 2Fe + 3Cl2 = 2FeCl3 3) FeCl3 + 3NaOH = Fe(OH)3 + 3NaCl |
|
| Ответ правильный и полный, включает все названные выше элементы | 3 |
| Правильно записаны 2 уравнения реакций | 2 |
| Правильно записано одно уравнение реакции | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
С2. К 200 г 12,25%-ного раствора серной кислоты прилили избыток раствора нитрата бария. Определите массу выпавшего осадка.
Ответ:
| Содержание верного ответа и указания по оцениванию (допускаются иные формулировки ответа, не искажающие его смысла) | Баллы |
| Элементы ответа: 1) Составлено уравнение реакции: H2SO4 + Ba(NO3)2 = BaSO4↓+ 2HNO3
2) Рассчитана масса и количество вещества серной кислоты, содержащейся в растворе: m (H2SO4) = 200 ∙ 0,1225 = 24,5 г. n(H2SO4) = 24,5/ 98 = 0,25 моль
3) Определена масса вещества, выпавшего в осадок: по уравнению реакции n(BaSO4) = n(H2SO4) = 0,25 моль. m(BaSO4) = 0,25 ∙ 233 = 58,25 г. |
|
| Ответ правильный и полный, включает все названные выше элементы | 3 |
| Правильно записаны 2 первых элемента из названных выше | 2 |
| Правильно записан один из названных выше элементов (1-й или 2-й) | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 3 |
1
















