Контрольная работа «Металлы и их соединения» 2 вариант
Часть А.
1. Изобразите строение атома калия в виде электронной и электронно-графической формы
2. С растворами гидроксида натрия и соляной кислоты взаимодействует
1) Ag
2) Al
3) Fe
4) Mg
5) Zn
3.В каком ряду химических элементов усиливаются металлические свойства соответствующих им простых веществ? Выберите 2 правильных ответа
1) кислород → фтор → неон
2) натрий→калий→рубидий
3) кремний → сера → хлор
4) селен → сера → кислород
5) алюминий → магний → натрий
4. С каждым из веществ, формулы которых H2O, H2SO4, KOH будет взаимодействовать:
1. Ртуть
2. Алюминий
3. Литий
4. Углерод
5. Цинк
5. С медью не реагирует
1) хлорид железа(II) (р-р)
2) серная кислота (конц.)
3) кислород
4) хлор 5)серная кислота(разб)
6.Алюминий образует сульфат и сульфит алюминия при взаимодействии с
1) серой
2) серной кислотой
3) сернистой кислотой
4) сероводородом
5) соляной кислотой
Контрольная работа «Металлы и их соединения» 1 вариант
Часть А.
1. Изобразите строение атома магния в виде электронной и электронно-графической формы
2. Какой из указанных металлов вступает в реакцию с соляной кислотой?
1) серебро 4) медь
2) золото 5) магний
3) алюминий
3. В каком ряду химических элементов усиливаются металлические свойства соответствующих им простых веществ?
1) калий → натрий → литий 4) алюминий → кремний → углерод
2) сурьма → мышьяк → фосфор 5) кремний→алюминий→магний
3) углерод → кремний → германий
4. С каждым из веществ: H2O, Fe2O3, H2SO4 — будет взаимодействовать Выберите 2 правильных ответа
1) натрий 4) серебро
2) ртуть 5) магний
3) медь
.
5. Железо реагирует с раствором
1) NaCl 4) BaCl2
2) CuCl2 5) PbCl2
3) CaCl2
Часть В.
1. Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВА
А) Fe+HCl
Б) Fe2O3+H2SO4
В) Cu+HNO3(k)
ПРОДУКТЫ РЕАКЦИИ
1) FeCl2+H2
2) FeCl3+H2
3) Fe2(SO4)3+H2O
4) Cu(NO3)2+H2
5) Cu(NO3)2+NO2+H2O
2. Используя метод электронного баланса, составьте уравнение реакции. Определите окислитель и восстановитель. 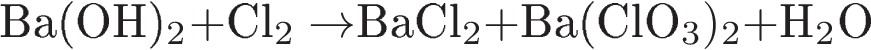
3. Рассчитайте массу осадка, который выпадет при взаимодействии избытка карбоната калия с 17,4 г раствора нитрата бария
6. И железо, и цинк при комнатной температуре реагируют с
1) соляной кислотой
2) оксидом углерода(II)
3) cульфатом меди(II)
4) водой
5) гидроксидом магния
Часть В.
1. Установите соответствие между веществами, вступающими в реакцию и продуктами их взаимодействия
РЕАГИРУЮЩИЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) Na + H2O 1) Fe(OH)2+ NaCl
Б) Na2O + H2O 2) NaOH + H2
В) NaOH+ SO3 3) NaOH
Г) NaOH + FeCl2 4) Fe(OH)3+ NaCl
5) Na2SO3 + H2O
6) Na2SO4 + H2O
2. Используя метод электронного баланса, составьте уравнение реакции. Определите окислитель и восстановитель.
Cu+ H2SO4 = CuSO4+ H2O+ SO2
3. Решите задачу. К раствору силиката калия массой 20,53 г прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка.

























