Просмотр содержимого документа
«Ковалентная химическая связь.»

1 вариант:
1.По данным о распределении валентных электронов назовите элемент:
а ) 2s 1 б ) 2s 2 2p 4
в ) 3s 2 3p 6 г ) 3d 10 4s 1
2.Изобразите строение атома азота, серы.
2 вариант:
1.По данным о распределении валентных электронов найдите элемент:
а ) 4s 2 4p 5 б ) 2s 2 2p 6
в ) 3s 2 3p 4 г ) 4s 2 4p 3
2.Изобразите строение атома кислорода, неона.

Ковалентная химическая связь.


- Химическая связь – это силы взаимодействия, которые соединяют отдельные атомы в молекулы, ионы, кристаллы.
- Способность атома элемента образовывать различное число химических связей с другими атомами называется валентностью.


Ковалентная связь – это химическая связь между атомами, осуществляемая с помощью общих электронных пар.

Джильбер Льюис
Теория ковалентной
связи
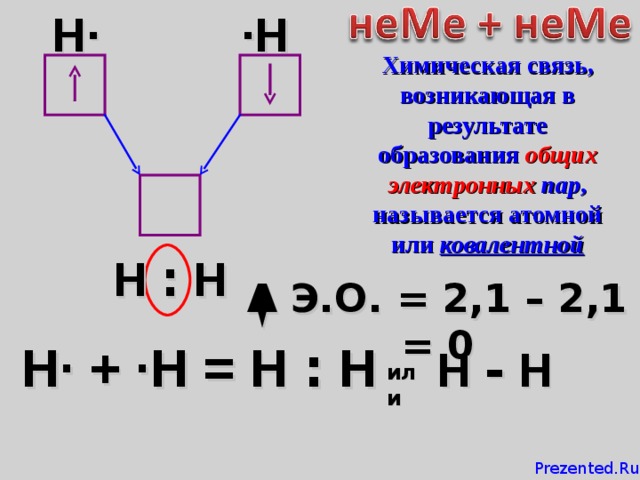
H·
·H
Химическая связь, возникающая в результате образования общих электронных пар , называется атомной или ковалентной
Н : Н
Δ Э.О. = 2,1 – 2,1 = 0
H· + · Н = Н : Н
Н - Н
или
Prezented.Ru



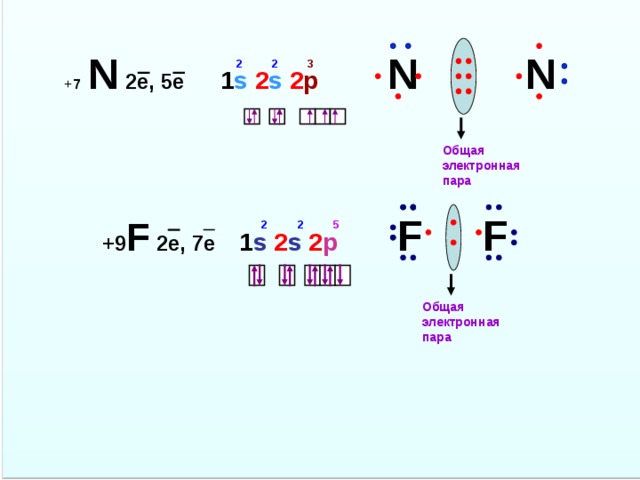
+ 7 N 2е, 5е 1 s 2 s 2 p N N
2 2 3
Общая электронная пара
+ 9 F 2е, 7е 1 s 2 s 2 p F F
2 2 5
Общая электронная пара
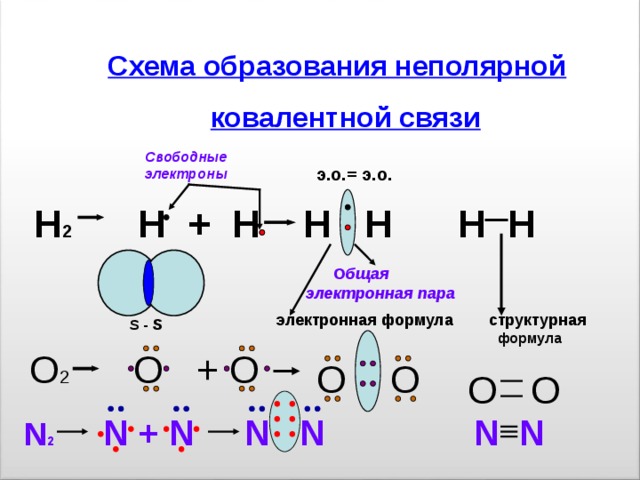
Схема образования неполярной
ковалентной связи
Свободные электроны
э.о.= э.о.
Н 2 Н + Н Н Н Н Н
электронная формула структурная
О бщая электронная пара
S - S
формула
О 2 О + О
О О
О О
N 2 N + N N N N N
15

А как же образуются молекулы из атомов разных неметаллов (сложных веществ):
H С l , HF , Н₂О , Н₂ S, N Н₃… ?

Способность атомов химических элементов оттягивать к себе общие электронные пары, называется электроотрицательностью (ЭО)
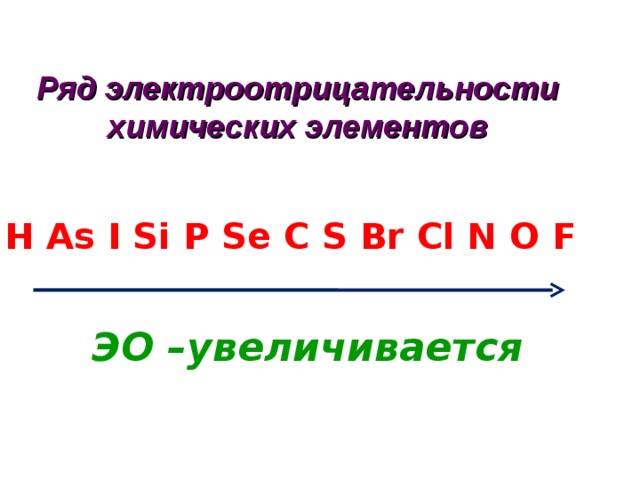
Ряд электроотрицательности химических элементов
H As I Si P Se C S Br Cl N O F
ЭО –увеличивается
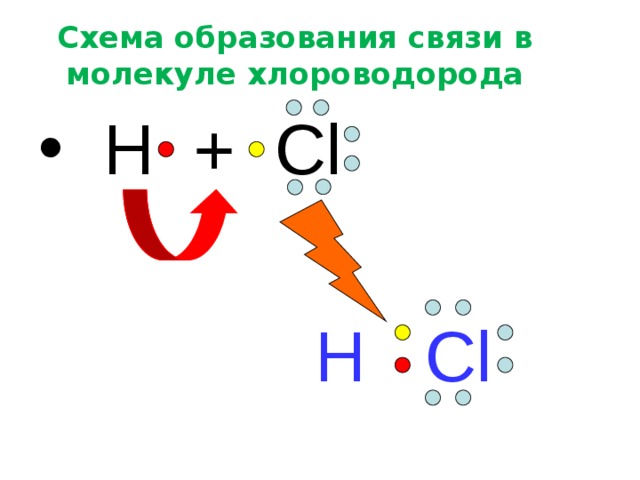
Схема образования связи в молекуле хлороводорода
H Cl
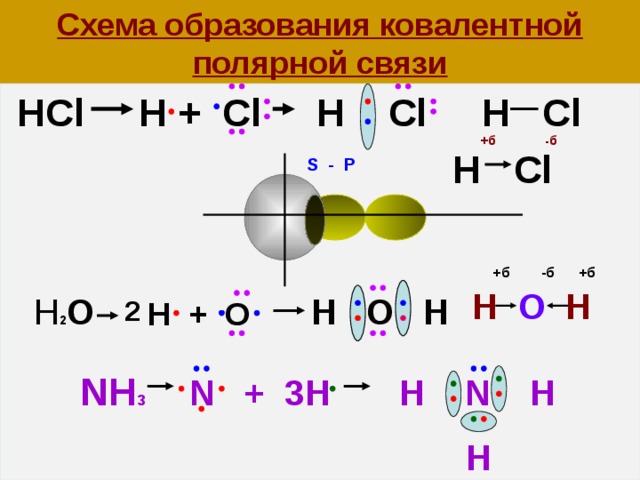
Схема образования ковалентной полярной связи
HCl H + Cl H Cl H Cl
H Cl
+б -б
S - P
2
+ б -б +б
Н О Н
H O H
H 2 O
H + O
NH 3 N + 3H H N H
H

Изобразить схему образования связи в молекуле хлороводорода HCl ;
•• ••
H• + • Cl ׃ = H ( ׃ ) Cl ׃
•• ••
что произошло с электронными слоями у водорода и хлора в результате образования ковалентной связи?

Разумеется, атомы менее ЭО будут иметь избыточный положительный заряд , т.е. будут представлять собой как бы положительный полюс молекулы с зарядом δ +, а более ЭО полюс с зарядом δ -.
Вот вам и стало понятно название этой разновидности ковалентной связи – полярная .
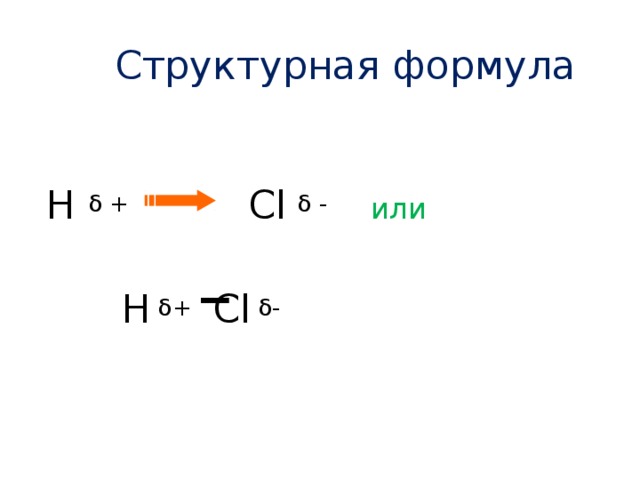
Структурная формула
H δ + С l δ - или
H δ + Cl δ -

Выводы:
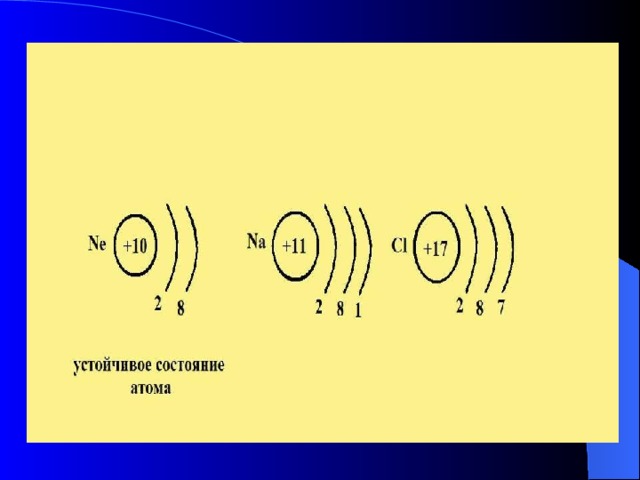
- - Атомы образуют химические связи, чтобы приобрести устойчивую 8-электронную конфигурацию внешнего энергетического уровня.
- - Возникновение общих электронных пар приводит к образованию ковалентной химической связи между атомами .
- - Состав вещества можно выражать в виде:
- Молекулярной формулы HCl
- Электронной формулы
- Структурной формулы H–Cl

Домашнее задание п. 12 упр. 1-6



















































