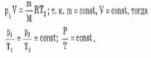Просмотр содержимого документа
«Лабораторная работа изопроцесс»
Лабораторная работа «Изучение изотермического процесса в газе»
ЦЕЛЬ: Обеспечить выполнение обучающимися экспериментальных исследований изопроцессов в газах.
ОБРАЗОВАТЕЛЬНЫЕ ЗАДАЧИ УРОКА:
1) Сделать экспериментальную проверку закона Бойля- Мариотта путем сравнения параметров газа в двух термических состояниях..
2) Продолжить формирование навыков и умений работать с графиками изопроцессов.
3) В результате обсуждения результатов работы доказать справедливость закона Бойля- Мариотта.
РАЗВИВАЮЩИЕ ЗАДАЧИ:
1) Развивать исследовательскую и творческую деятельность обучающихся, которая активизирует познавательные интересы учеников.
ВОСПИТАТЕЛЬНЫЕ ЗАДАЧИ:
1) Добиваться последовательности и аккуратности записи результатов при экспериментальных исследованиях. 2) Формирование навыков работы в команде.
Ход урока
1. Огр момент.
2. Рассаживаются в зависимости от выбранной фигуры. (на столах приготовлен материал для изучения данной группы)
3. Переход учащихся в новую группу по цвету ( выполнение работы лабораторной каждый вносит свой вклад все заносят свои данные в таблицу. Теоретик объясняет теорию , практик выполнят работу, аналитик вычисляет погрешности . Эксперт готовит защиту .) ( Экспертов можно подготовить заранее )
4. Физ минутка
5. Защита
6. Рефлексия эксперты ставят оценку группе и каждый сам оценивает себя в группе ( итоговая оценка выводиться из трех двух эксперта и учителя)
Теория
Изопроцессы
Изопроцессы - это процессы, протекающие при неизменном значении одного из макроскопических параметров (р, V, Т).
Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называют изотермическим.
Изотермический процесс описывает закон Бойля- Мариотта, открытый в 1861 г. английским ученым Р. Бой-лем (1627-1691) и в 1876 г. французским ученым Э. Мари-оттом (1620-1684). При постоянной массе газа pV = const.
Для газа данной массы произведение давления на его объем постоянно, если температура не меняется.
Графики изотермического процесса в координатах р-V; р-Т; V-Т имеют следующий вид (рис. 27):

Процесс изменения состояния термодинамической системы при постоянном давлении называется изобарным. Из уравнения Менделеева-Клапейрона следует, что при
постоянной массе газа 
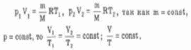
Для данной массы газа отношение объема к температуре постоянно, если давление газа не меняется.
Этот закон был установлен экспериментально в 1802 г. французским ученым Ж. Гей-Люссаком (1778-1850).
Графики изобарического процесса в координатах р-V; V-Т; р-Т имеют следующий вид (рис. 28):
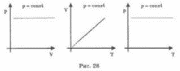
Процесс изменения состояния термодинамической системы при постоянном объеме называется изохорным. Из уравнения Менделеева-Клапейрона можно записать:
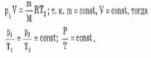

Для данной массы газа отношение давления к температуре постоянно, если его объем не меняется. Графики изохорного процесса в координатах р-V; V-Т; р-Т имеют следующий вид (см. рис. 29). Этот закон был
установлен экспериментально в 1787 г. Ж. Шарлем (1746-1823).


Практическая часть

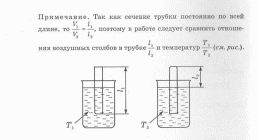


Аналитическая часть