

Мақсаты:
Білімділік: Оқушылардың химиялық байланыс туралы білім алуына жағдай туғызу;
Дамытушылық: Оқушылардың ойлау қабілеті мен дүниетанымдарын кеңейту;
Тәрбиелік: Топпен жұмыс істей білуге тәрбиелеу;
Әдісі: ой қозғау, Венн диаграммасы, есептер шығару;
Көрнекілігі: сызбалар, топшамалар;
Күтілетін нәтиже:
1. Иондық байланыс туралы түсінеді;
2. Тапсырмалар орындай алады.

Қызығушылықты ояту
«Жедел жауап»
Сабаққа психологиялық дайындық
Үй тапсырмасын тексеру
(топшама арқылы)
Топтастыру

Химиялық байланыс
Иондық
Ковалентті
Сутекті
Металдық
полюсті
полюссіз

бейМе
Ковалентті полюссіз байланыс
?
бейМе
?
Ковалентті полюсті байланыс
бейМе
бейМе
?
Ме
Ионды байланыс
бейМе
Ионды байланыс – б ұл иондар арасындағы байланыс.
Металдар мен бейметалдар арасында түзіледі.

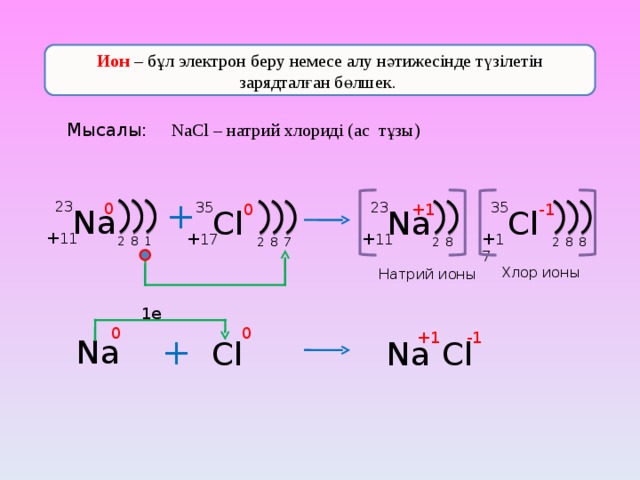
Ион – бұл электрон беру немесе алу нәтижесінде түзілетін зарядталған бөлшек.
Мысалы:
NaCl – натрий хлориді (ас тұзы)
+
23
0
23
35
35
0
+1
-1
Na
Cl
Cl
Na
+ 11
+ 17
+ 17
+ 11
2
8
1
2
2
8
8
7
8
2
8
Хлор ионы
Натрий ионы
1e
Использован слайд из презентации Баженова А.А. «Ионы и ионная связь» в исправленном виде http://www.alekseibazhenov.narod.ru/proektor8chem.html
0
0
-1
+1
+
Na
Cl
Cl
Na
7
7

Электрондарын беретін бөлшек
оң ионға айналады ( катион )
-
+1
0
Na
Na
1e
атом
ион
Электрондарын беретін бөлшек
теріс ионға (анион) айналады .
Использован слайд из презентации Баженова А.А. «Ионы и ионная связь» в исправленном виде http://www.alekseibazhenov.narod.ru/proektor8chem.html
0
+
-1
Cl
Cl
1e
атом
ион
8
8

Na 0 + F 0 → Na + F -
Na 0 + Cl 0 2 → Na + + Cl -
K 0 + Cl 2 0 → K + Cl -
Zn 0 + S 0 → Zn + S -
Қарама-қарсы зарядталған иондар арасындағы байланысты иондық байланыс деп атайды. 1916 жылы неміс ғалымы Коссель ұсынды. Өзінің сыртқы валенттік электрондарына сай электрон бұлтын берген атомдар оң зарядты катиондарға , ал осы электрондарға сай бұлтты қосып алған атомдар терісзарядты анионындарға айналады.Түзілген иондар біріне-бірі Кулон заңы бойынша тартылысып.иондық байланыс түзіледі

Химиялық пирамиданың шыңына шығу жолы – қосылыстардағы ионды химиялық байланыс. Осы заттардағы байланыстың түзілу сызбасын сызыңдар.
Са Cl 2
KCl
H 2
H 2 O
NaF
HF
N 2
Cl 2
BaCl 2
F 2

«Крестиктер-ноликтер» ойынын ойнаңдар. Барлығы ионды байланыспен түзілген заттардан тұратын тік, көлденең немесе қиғаш жолақты табыңдар. Осы заттардағы ионды байланыстың түзілу жолын сызыңдар.
Na 2 S
CH 4
Br 2
NH 3
К Br
PH 3
MgO
H 2 O
O 2

Өздік жұмыс
Химиялық байланыс түрлері мен бейорганикалық қосылыстардың кластарына ажыратыңдар:
NO, HF,O 2 , CO 2 , CI 2 , FeCI 3 , NaCI, KBr, CaO, C 3 N, AlCI 3 , NH 3 , CaF 3 , H 2 , CH 4

Өзіңді өзің тексер:
- Электртерістілік - бұл …….
- Ковалентті полюсті байланыс – бұл …..
- Ковалентті полюссіз байланыс – бұл …..
- Электртерістілігі ең жоғары элемент - …….
- Ковалентті байланысы бар заттардың кристалдық торы қандай болады?
- Мына заттардан ковалентті полюсті байланысты заттарды теріп жазыңдар:
HCl, O 2 , H 2 S, SO 2 , OF 2 , Br 2 , H 2 , PCl 3 , CH 4
11.11.18

Толғаныс
Венн диаграммасы: Иондық және ковалентті байланыс
Үйге тапсырма: §64 1-3 жаттығу
Бағалау






























