Решение задач на вывод формул
10- 11 класс.
Необходимо знать наизусть!
1.Массовая доля
ω(Эл) в долях =Аr(Эл)*n/ Mr(в-ва)
Н-р: 1 доля-100%
0.5- ________
_____- 0.25%
2.Нахождение индексов
(число атомов)
СХНу
Х:У =n(С):n(Н)
Х:У =m(С)/Ar(С): m(Н)/Ar(Н)
Х:У = ω(С)/Ar(С): ω(Н)/Ar(Н)
3.количество вещества и плотность
n=m/M
n =V/Vm
n=N/Na
ρ=m/v
ρ= M/Vm (22,4л/моль)
4. Относительная плотность
DH2(в-ва)=М(в-ва)/М(Н2)
DВозд(в-ва)=М(в-ва)/М(возд)
(М (возд)=29г/моль)
5. Продукты сгорания :
С СО2 ; n(C)=n(СО2)
СО2 ; n(C)=n(СО2)
Н Н2О; 2n(Н)=n(Н2О)
Н2О; 2n(Н)=n(Н2О)
S SO2; n(S)=n(SO2)
SO2; n(S)=n(SO2)
P P2O5; 2n(P)=n(P2O5)
P2O5; 2n(P)=n(P2O5)
N a,C Na2CO3; 2n(Na)=n(Na2CO3)
a,C Na2CO3; 2n(Na)=n(Na2CO3)
n(C )=n(Na2CO3)
H ,Cl HCl; n(H)=n(HCl)
,Cl HCl; n(H)=n(HCl)
n(Cl)=n(HCl)
N N2; 2n(N)=n(N2)
N2; 2n(N)=n(N2)
6. Малярная масса(общая формула)
M(CnH2n+2)=Ar(C ) n+Ar(H) (2n+2)=14n+2
Алканы - CnH2n+2
Алкенны и циклоалканы - CnH2n
Алкины и алкадиены - CnH2n-2
Арены - CnH2n-6
Моногалогеналканы - CnH2n+1Г
Дигалогеналканы - CnH2nГ2
Предельные одноатомные спирты –
CnH2n+1ОН, R-OH
Фенолы - CnH2n-7ОН
Альдегиды - CnH2n+1СОН, R-СOH
Предельные карбоновые кислоты – CnH2n+1СООН, R-СOОH
Сложные эфиры – R1-СOО R2
Аминокислоты - CnH2n (NH2)СООН
Первичные амины - CnH2n+1NH2,R- NH2
Вторичные амины – R1- NH- R2
Т![]() ретичные амины - R1- N- R2
ретичные амины - R1- N- R2
R3
Типология задач
I.

%


IV.1 кл. D II.
вещества
D
класс
 IV. 2. вещества
IV. 2. вещества
Сгорание

III.
Через уравнение
(При взаимодействии….)
 IV.3.4.
IV.3.4.
Класс
вещества

Найти М используя
формулы пунктов 3 и 4 теории
Практика решения задач.
I. Вывод формул веществ по массовым долям элементов:
1. Массовая доля азота в оксиде равна 36.84%. Найдите формулу данного оксида.
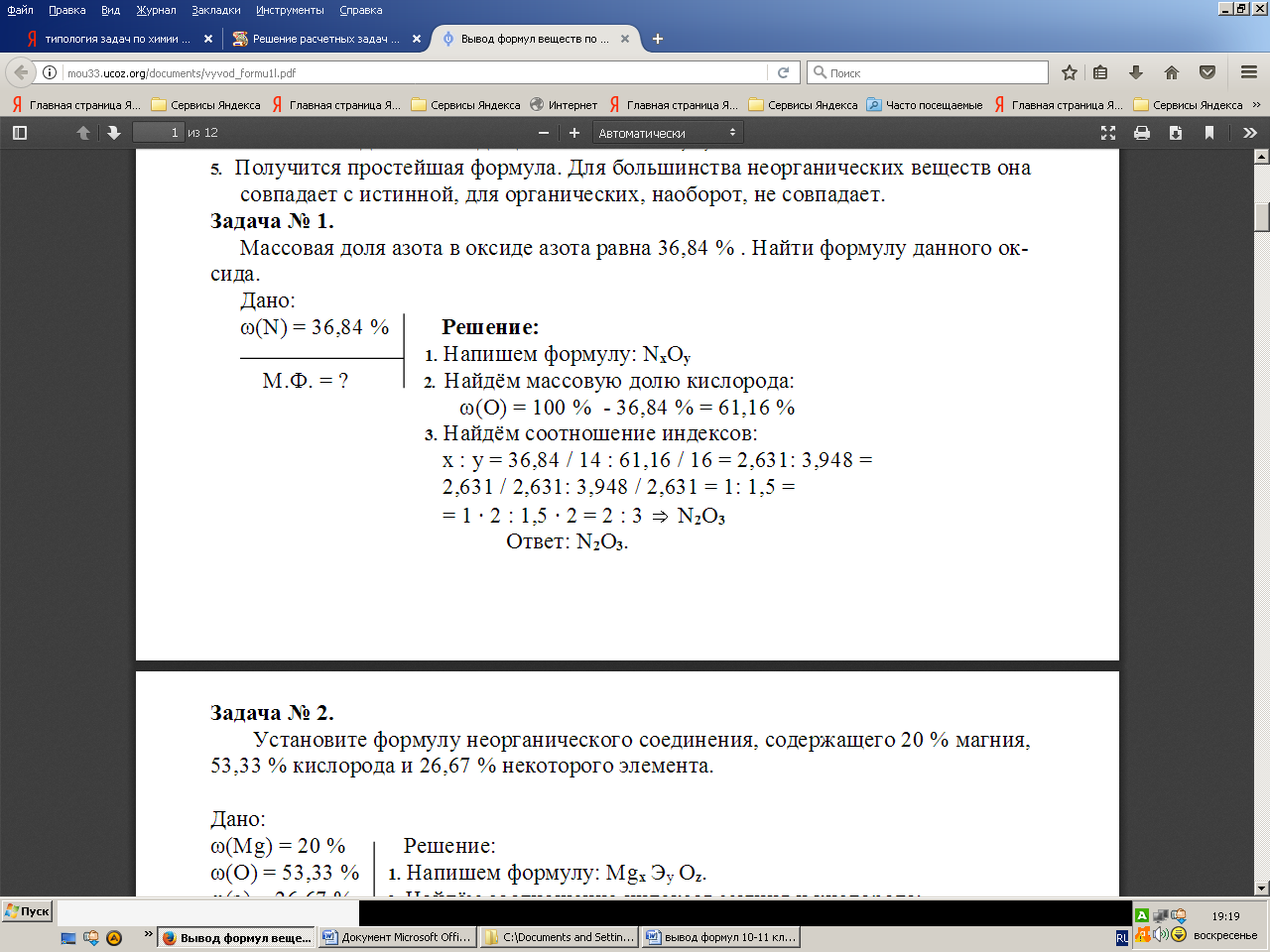
2. Установите формулу неорганического соединения, содержащего 20% магния, 53,33% кислорода и 26.67% некоторого элемента.
3. Массовая доля углерода в углеводороде равна 83.72%. Найти молекулярную формулу углеводорода.
Д\З 4. Массовая доля фосфора в его оксиде равна 43.66%. Какова формула оксида?
II. Вывод формул веществ по массовым долям элементов и данным для нахождения истинной молярной массы.
Найти формулу углеводорода, в котором содержится 14,29% водорода, а его относительная плотность по азоту равна 2.
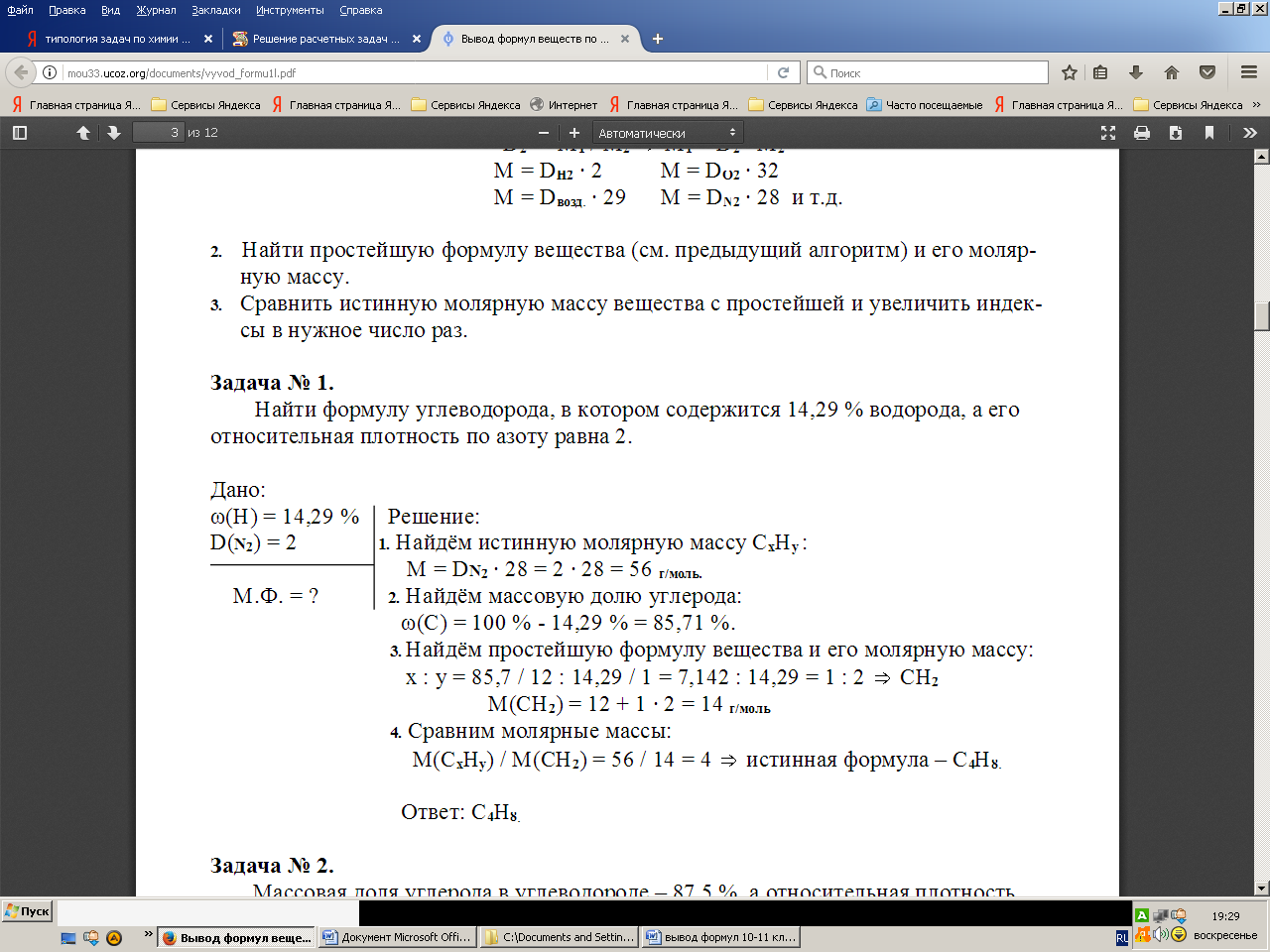
Д\З Относительная плотность углеводорода по воздуху равна3.31, а массовая доля водорода в нем 12.5%. Найдите молекулярную формулу вещества.
III. Вывод формул веществ по продуктам сгорания.
При сгорании 7.2.г вещества образовалось 9.9г углекислого газа и 8.1 г воды. Плотность паров этого вещества по водороду равна 16. Определите формулу вещества.
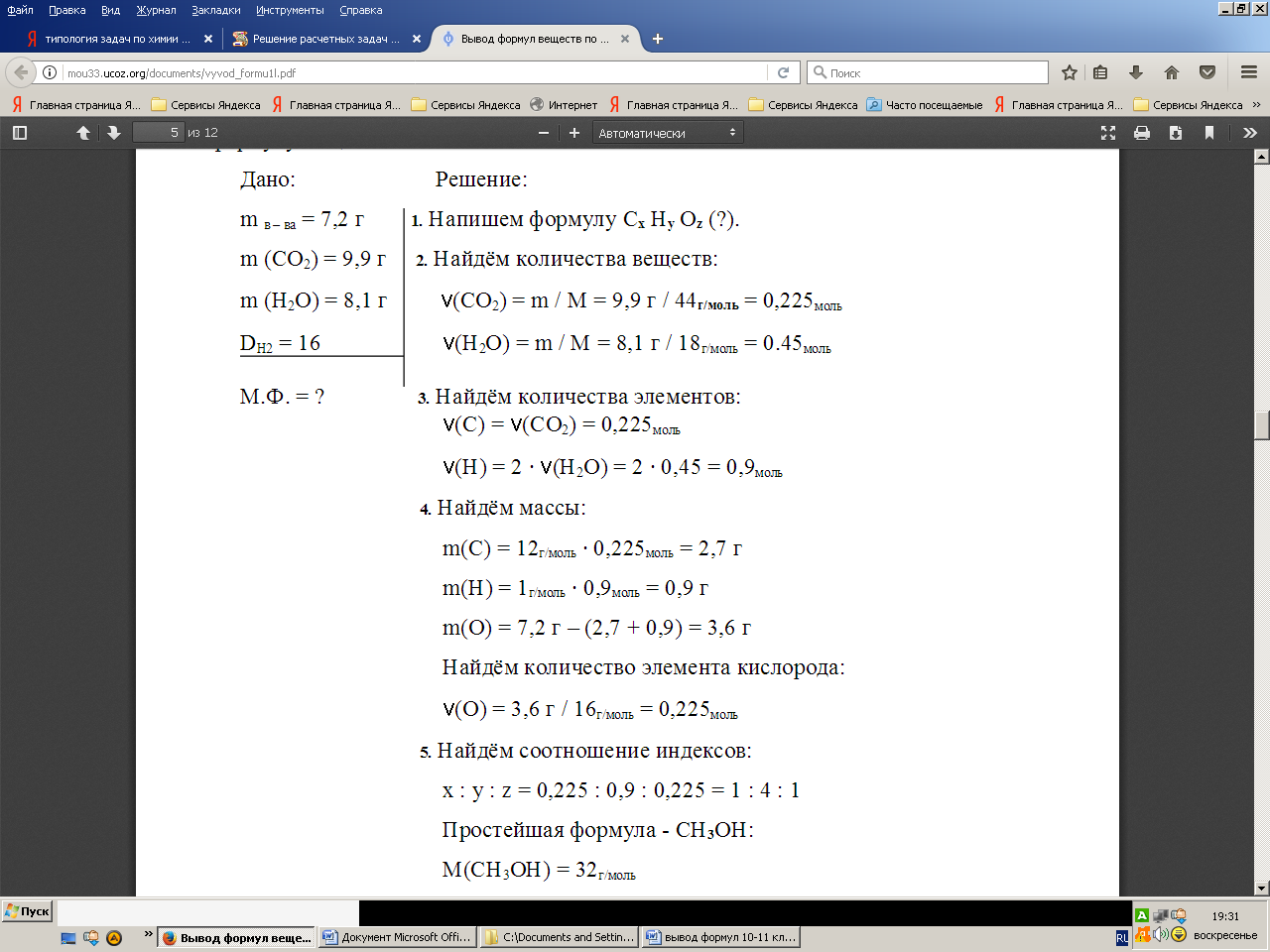

Д\З При сгорании газа, не содержащего кислород, выделилось 2.24л углекислого газа, 1.8 г воды и 3.65 г хлороводорода. Определите формулу сгоревшего вещества.
IV. Вывод формул органических веществ по общим формулам.
Вывод формул по известной массовой доле элемента в веществе.
1. Определить формулу аминокислоты, если известно, что она содержит 15.73% азота.
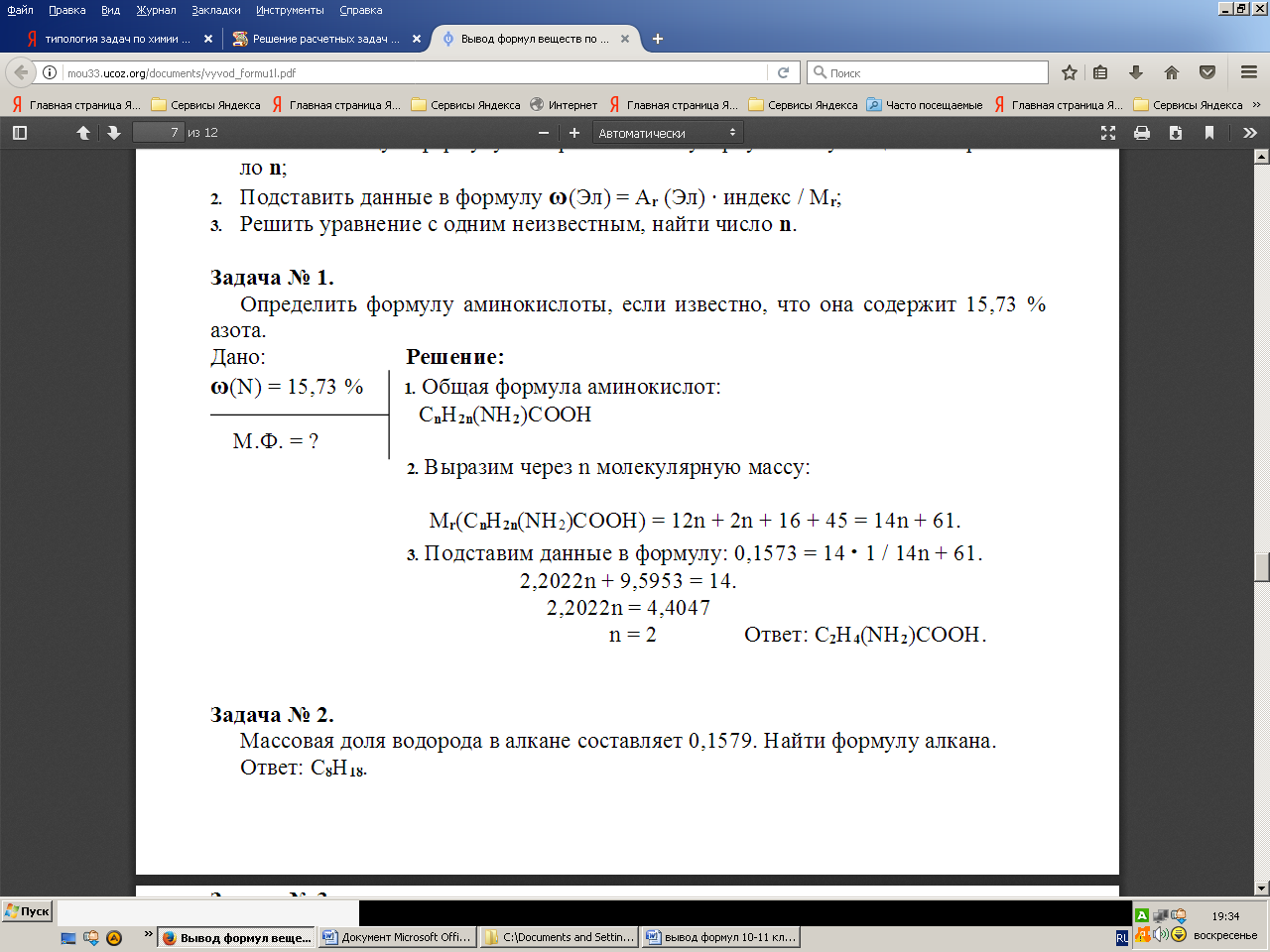
Д/З Массовая доля водорода в алкане составляет 0,1579. Найти формулу алкана.
Вывод формул по известным данным для нахождения истинной молярной массы.
1. Пары одного из монобромалканов в 68.5 раз тяжелее водорода. Найти формулу монобромалкана.
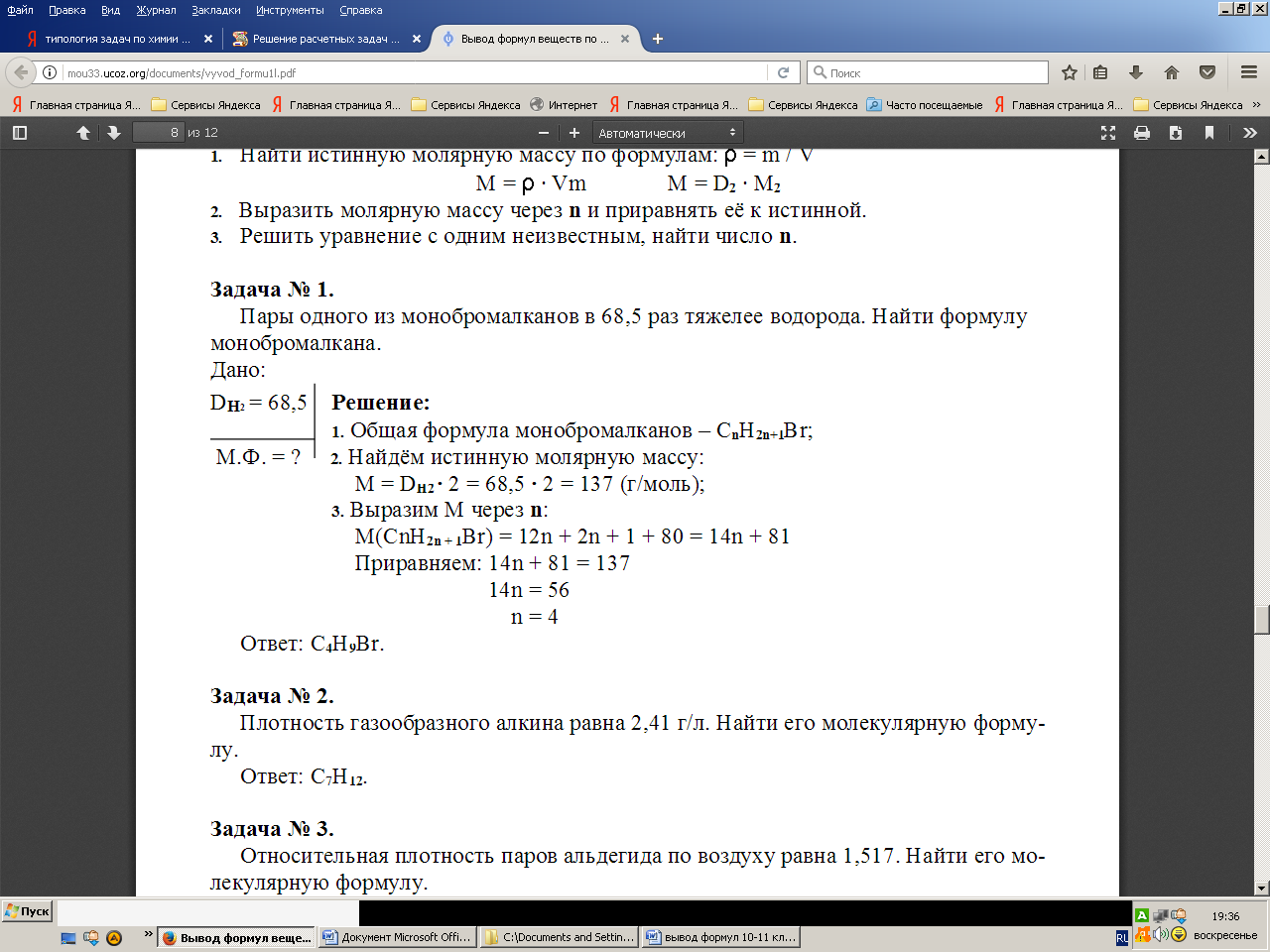
Д\З Плотность газообразного алкина равна 2.41г\л. Найти его молекулярную формулу.
3.Вывод формул по уравнениям реакций в общем виде, если известны данные для двух веществ.
При взаимодействии предельного одноатомного спирта массой 3г с избытком натрия было получено 0.56л водорода. Определите формулу спирта.
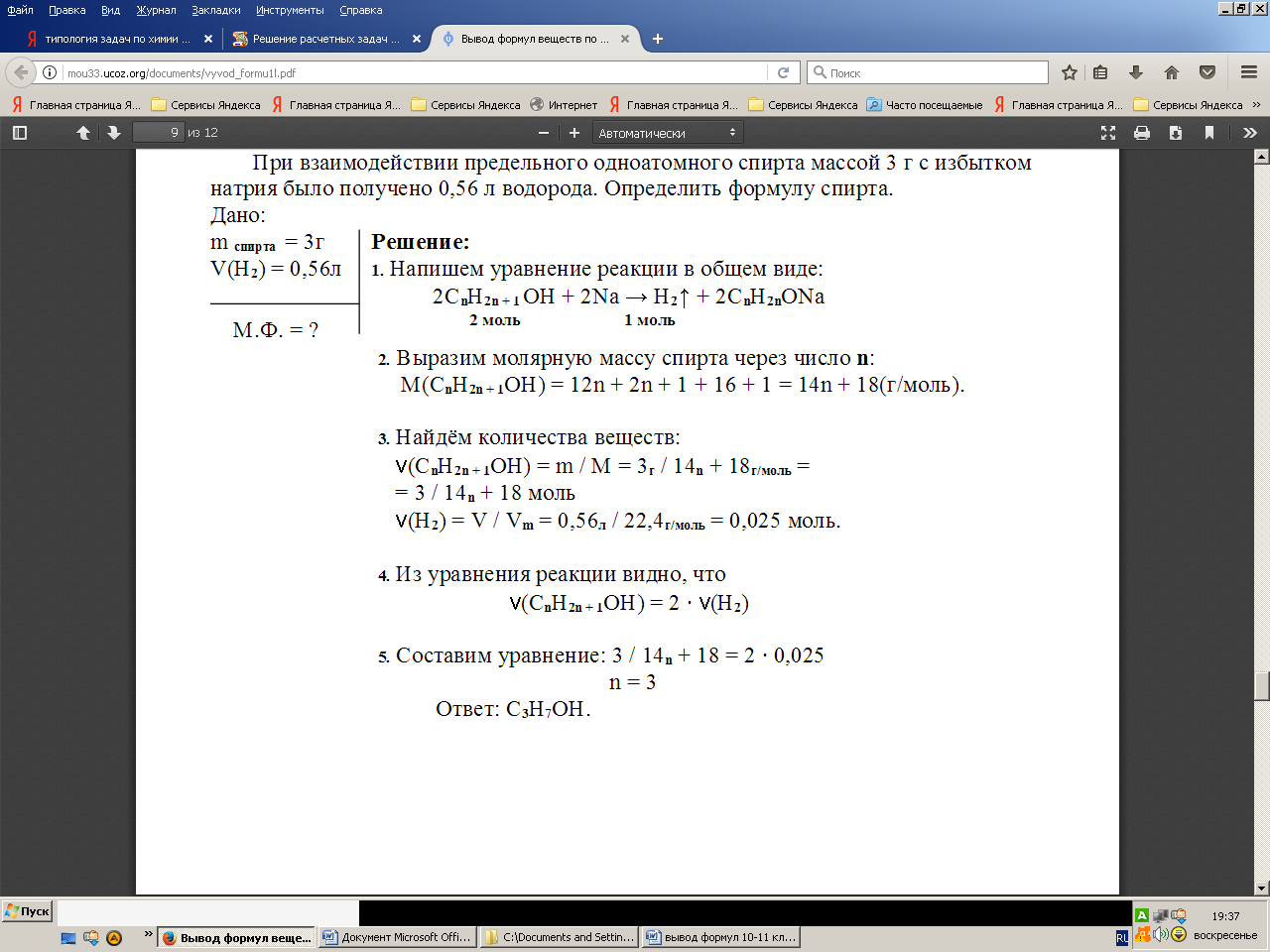
Д\З При сгорании 13.2г алкана образовалось 20.16л углекислого газа. Найдите формулу алкана.
4. Вывод формул по уравнениям реакций в общем виде с применением закона сохранения массы веществ.
Некоторый сложный эфир массой 7.4 г подвергнут щелочному гидролизу. При этом получено 9.8г калиевой соли предельной одноосновной кислоты и 3.2. г спирта. Установите формулу этого эфира.
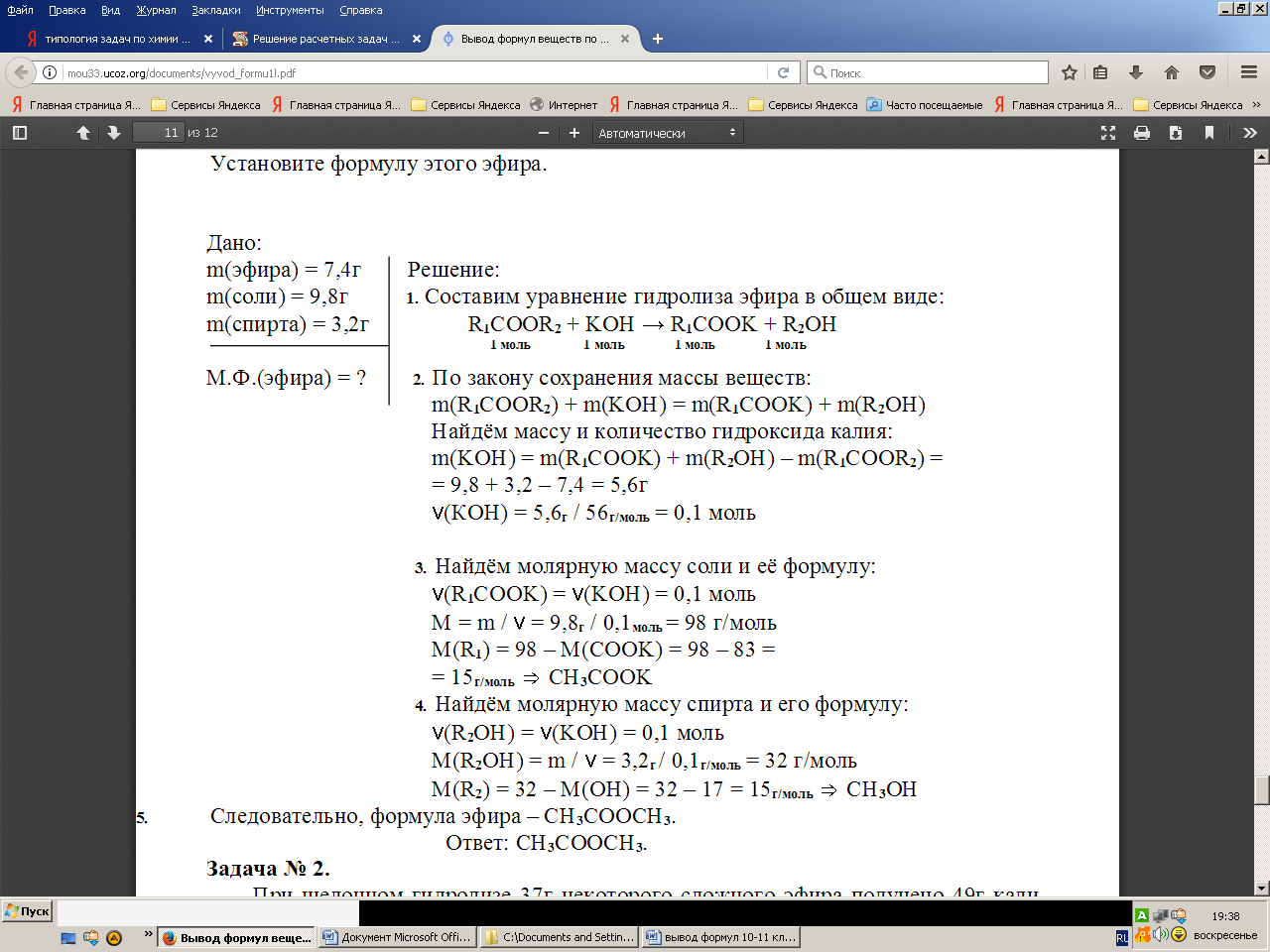
ДЗ При щелочном гидролизе 37г некоторого сложного эфира получено 49г натриевой соли одноосновной карбоновой кислоты и 16г спирта. Установите формулу сложного эфира.







 СО2 ; n(C)=n(СО2)
СО2 ; n(C)=n(СО2)

 IV.1 кл. D II.
IV.1 кл. D II.  IV. 2. вещества
IV. 2. вещества  IV.3.4.
IV.3.4. Найти М используя
Найти М используя 

















