Просмотр содержимого документа
«Олимпиада по химии 10 класс»
ЗАДАНИЯ ШКОЛЬНОГО ЭТАПА ОЛИМПИАДЫ ШКОЛЬНИКОВ ПО ХИМИИ
10 КЛАСС
Часть 1. Тестовые задания.
10 тестовых заданий с одним правильным ответом по 1 баллу каждый
1. Несколько аллотропных модификаций образует каждое вещество в паре:
а) хлор и кислород;
б) азот и углерод;
в) сера и магний;
г) фосфор и сера.
2. Ион, имеющий в своем составе 18 электронов и 16 протонов, обладает зарядом, равным:
а) + 18;
б) - 18;
в) + 2;
г) – 2.
3. Степень окисления хрома в ионе Cr2O72- равна:
а) +2;
б) +4;
в) +6;
г) +7.
4. Прочность связи в ряду молекул F2, O2, N2 увеличивается, потому что:
а) увеличивается валентный угол;
б) увеличивается радиус атомов;
в) увеличивается число связей в молекуле;
г) уменьшается электроотрицательность атомов.
5. Углеводород состава С5Н10 может быть гомологом:
а) этана;
б) пентина-1;
в) 2-метилбутена -2;
г) циклогексана.
6. В соответствии с сокращенным ионным уравнением
Cu2+ + 2OH- =Cu(OH)2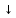 взаимодействуют:
взаимодействуют:
а) CuSO4 и Mg(OH)2;
б) CuSO3 и NaOH;
в) CuSO4 и Ba(OH)2;
г) CuCl2 и Ba(OH)2.
7. В ряду элементов Na Mg А1 Si
а) уменьшается число протонов в ядрах атомов
б) увеличивается число электронных слоев в атомах
в) уменьшается высшая степень окисления атомов
г) уменьшаются радиусы атомов
8. В схеме превращений Fe FeCl3 Fe(OH)3 веществами, с помощью которых можно осуществить превращение, являются соответственно:
а) Сl2 и Сu(ОН)2
б) СuС12 (р-р) и NaOH (p-p)
в) Сl2 и NaOH (p-p)
г) НСl и Н2O
9. В отличие от бутана, бутен вступает в реакцию:
а) замещения
б) отщепления
в) горения
г) присоединения
10. Число структурных изомеров пентана равно:
а) 5
б) 4
в) 3
г) 2
Часть 2. Задачи
В начале ХХ столетия геологи зашифровали на картах места открытия руд ценных металлов при помощи координат химических элементов в Периодической системе. Арабской цифрой указывали номер периода, а римской – номер группы. Кроме того, в записях были еще буквы русского алфавита – А и Б. На одной из старых карт нашли обозначения: 4VIБ, 4VIIIБ2, 6IБ, 6IIБ. Задание: Расшифруйте записи геологов. (2 балла)
При реакции водного раствора щелочи с водным раствором хлорида железа(II) образовалось 9 г осадка, масса которого при стоянии на воздухе увеличилась. Объясните это явление. Рассчитайте прирост массы осадка. (6 баллов)
Напишите уравнения реакций, соответствующие схеме превращений:
Na → NaOH → Na2CO3 → CO2 → CaCO3 → CO2 (6 баллов)
Вычислите в процентах массовую долю кислорода в сульфате железа(II). Запишите число с точностью до целых. (3 балла)
3
























