Михайловский филиал ГАПОУ "Волгоградский медицинский колледж"
МЕТОДИЧЕСКАЯ РАЗРАБОТКА
КОМБИНИРОВАННОГО
ЗАНЯТИЯ
Тема: Спирты, фенолы
Общеобразовательная учебная дисциплина Химия
Курс: 1
Специальность: Сестринское дело
Форма обучения: очная
Количество часов: 2
Разработчик: Анкудинова Н.Н.
Методическая разработка
рассмотрена и одобрена
на заседании УМО
Протокол____от_______
Председатель УМО ________________
Михайловка, 2018
Мотивация изучения темы Спирты как представители кислородосодержащих органических соединений широко применяются в медицине и фармакологии. Спирты и их производные входят в состав лекарственных препаратов, антисептиков. Являются источником получения синтетических волокон, поливиниловых соединений, кетонов, альдегидов, растворителей, применяются в чистом виде.
Цели занятия:
Учебные цели студент должен
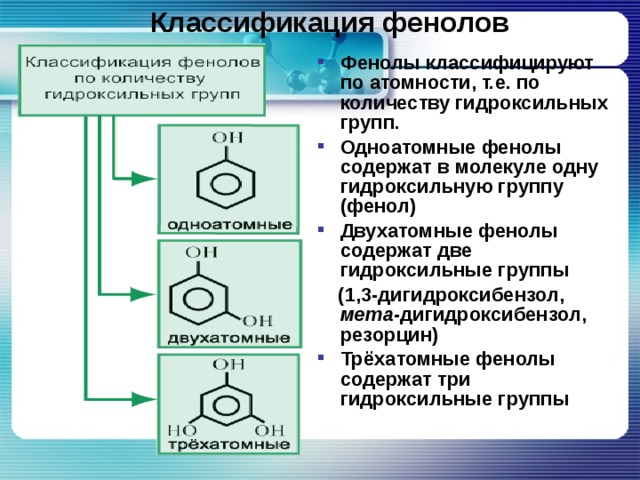
знать номенклатуру, химические свойства, применение в медицине многоатомных спиртов: гликолей, глицерина; классификацию, физические и химические свойства фенолов;
уметь моделировать строение молекул изучаемых веществ, обобщать знания и делать выводы о закономерности в изменении свойств гомологического ряда спиртов, описывать генетические связи между углеводородами, спиртами, альдегидами, владеть основополагающими химическими понятиями, теориями, законами и закономерностями, уверенно пользоваться химической терминологией и символикой.
Преподаватель должен
способствовать формированию представлений о месте химии в современной научной картине мира.
способствовать проявлению студентами логического мышления.
создать условия для понимания роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач.
Развивающие цели
обеспечить развитие познавательных интересов и интеллектуальных способностей в процессе моделирования химического эксперимента, самостоятельного приобретения знаний в соответствии с возникающими жизненными потребностями
способствовать формированию мировоззрения, соответствующего современному уровню развития науки и общественной практики; основ саморазвития, самообразования и самовоспитания
формировать готовность и навыки сотрудничества со сверстниками и взрослыми в образовательной деятельности; умение самостоятельно определять цели деятельности и составлять планы деятельности; готовность и способность к самостоятельной информационно-познавательной деятельности, владение навыками получения необходимой информации
Воспитательные цели
способствовать принятию и реализации ценностей здорового и безопасного образа жизни; бережному, ответственному и компетентному отношению к физическому и психологическому здоровью
формировать умение выбирать успешные стратегии в различных ситуациях; навыки разрешения проблем; критически оценивать и интерпретировать информацию, получаемую из различных источников; умение самостоятельно оценивать и принимать решения, определяющие стратегию поведения, с учетом гражданских и нравственных ценностей;
Формируемые результаты учебной деятельности
сформированность представлений о месте химии в современной научной картине мира; понимание роли химии в формировании кругозора и функциональной грамотности человека для решения практических задач;
владение основополагающими химическими понятиями, теориями, законами и закономерностями; уверенное пользование химической терминологией и символикой;
владение основными методами научного познания, используемыми в химии: наблюдение, описание, измерение, эксперимент; готовность и способность применять методы познания при решении практических задач;
сформированность умения давать количественные оценки и проводить расчеты по химическим формулам и уравнениям;
владение правилами техники безопасности при использовании химических веществ;
сформированность собственной позиции по отношению к химической информации, получаемой из разных источников.
Интеграционные связи внутридисциплинарные «Строение атома», «Основные положения теории химического строения органических соединений», «Предельные углеводороды (алканы)», «Непредельные углеводороды (алкены)»
Формы организации учебной деятельности студентов фронтальная, индивидуальная, коллективная
Применяемые на занятии технологии обучения проблемное обучение, личностноориентированное обучение, деятельностные технологии
Применяемые на занятии методы обучения
по источнику информации: словесные, наглядные
по степени активности обучаемых: действие по образцу, работа в парах, микрогруппах
Оснащение учебник, раздаточный материал, компьютер
Основные этапы занятия с указанием хронометража
Орг.момент 2 минуты
Проверка знаний и умений 16 минут
Объяснение нового материала 27 минут
Закрепление вновь изученного 10 минут
Обобщение изученного материала 30 минут
Подведение итогов занятия 3 минуты
Домашнее задание 2 минуты
Список литературы
Кузменко, Н.Е. Сборник задач и упражнений по химии [Текст] / Н.Е. Кузьменко, В.В. Еремин. - М.: Экзамен, 2002.-544 с.
Пустовалова, Л.М. Общая химия [Текст] / Л.М. Пустовалова, И.Е. Никанорова. – Ростов н/Д : Феникс, 2006. – 478 с.
Ход занятия
| № п/п | Название этапа | Описание этапа | Педагогическая цель этапа | Продолжительность этапа |
|
| Орг. момент | Отмечаются отсутствующие и внешний вид студентов и аудитории, сообщается тема, цели с проведением мотивации, сообщается план проведения занятия | Создание рабочей атмосферы, формирование познавательного интереса к учебной деятельности по данной теме, дисциплинирование обучающихся, мотивация | 2 |
|
| Проверка знаний и умений | а). проверка знаний по теме Предельные одноатомные спирты. Студенты работают с маршрутным листом (Приложение 1). Выполняют задания (Презентация, слайды 1-6). Проводят взаимопроверку, самопроверку, озвучивают результаты работы. б). подведение итогов контроля: Преподаватель обращает внимание на допущенные ошибки, вносит коррективы в ответы, отмечает лучших студентов и дает рекомендации, пояснения тем, кто допустил ошибки. | Определение уровня усвоения изучаемого материала, выявление слабых мест. | 16 |
|
| Объяснение нового материала | Сообщение обучающимся новых знаний с использованием мультимедийной презентации (Презентация, слайды 7-9). Организация самостоятельного изучения нового теоретического материала с использованием учебника, записи в тетрадях по плану маршрутного листа (Приложение 1) | Формирование познавательного интереса к данной теме, побуждение к самостоятельной деятельности, помощь в осмыслении действий. | 27 |
|
| Закрепление | Закрепление пройденного материала; уточнение, обобщение и систематизация полученных знаний. Индивидуальная работы и работа в парах по маршрутному листу (Приложение 1), самоконтроль | Определение уровня усвоения изучаемого материала, выявление слабых мест. Формирование практических умений, необходимых для овладения последующими учебными дисциплинами. Выработка умений самостоятельной работы по данной теме. | 10 |
|
| Обобщение изученного материала | Закрепление и обобщение материала по темам спирты, фенолы. Просмотр презентации о свойствах одноатомных, многоатомных спиртов и фенолов. Заполнение сравнительной таблицы «Одноатомные, многоатомные спирты и фенолы» (Приложение 1) | Обобщение и систематизация знаний. Выработка умений работать в микроруппах. Формирование творческого и логического мышления. |
10
20
|
|
| Подведение итогов занятия | Преподаватель кратко анализирует занятие и дает критическую оценку каждого его этапа, обращает внимание на хорошие результаты и на допущенные ошибки, выделяет лучшие работы и указывает на отставание, недостаточную подготовленность к занятию. Проверяет и оценивает учебные записи студентов, в соответствии с показателями и критериями, указанными в методических рекомендациях по управлению | Побуждение студентов к рефлексии, стимулирование интереса к учебе и ее результатам | 3 |
|
| Задание на дом | Преподаватель дает четкие рекомендации по подготовке к следующему занятию, (учебник Общая химия Л. М. Пустовалова, стр 339-347, Фенолы), акцентируя внимание на главных вопросах | Обеспечение добросовестного и осознанного выполнения домашнего задания. | 2 |
Приложение 1
Маршрутный лист
изучения темы Спирты
1. Проверка знаний по теме «Предельные одноатомные спирты»
Откройте презентацию в папке Спирты.
Внимательно изучите содержание слайда 1,2.
Выполните задания слайдов 3-5.
Осуществите самопроверку и взаимопроверку с помощью слайда 6.
Выполните отметки верно/неверно в тетради
2. Изучение нового материала «Фенолы»
Внимательно изучите содержание слайдов 7-9
Прослушайте комментарии преподавателя
Используя материал учебника выполните записи в тетрадях по плану:
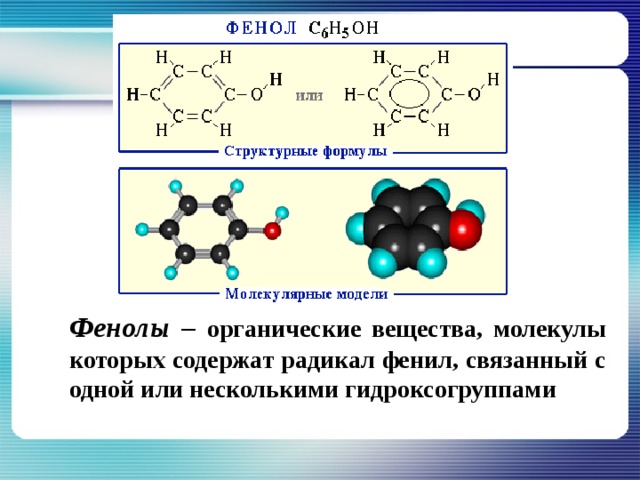
Тема «Фенолы»
Определение и общая формула
Изомерия и номенклатура
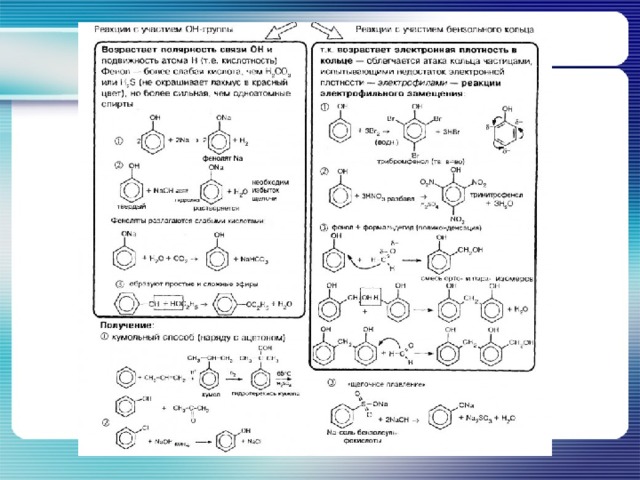
Химические свойства
3. Закрепление изученного материала
Для закрепления изученного материала по теме «Фенолы» выполните задания в тетради:
Определите среди предложенных общую формулу фенолов, запишите ее в тетрадь
CnH2n-2, CnH2n, C6H6-n(OH)n, CnH2n+1(OH), CnH2n-6
Составьте и назовите 3 изомера фенола, содержащего 9 атомов углерода и одну спиртовую группу.
Поменяйтесь работами, оцените результат напарника, отметьте карандашом верные и неверные ответы
4. Обобщение изученного материала
Внимательно изучите содержание слайдов 10-15, прослушайте комментарии преподавателя
Используя знания, полученные ранее и на сегодняшнем занятии, материал учебника, заполните сравнительную таблицу в тетради
|
| Предельные одноатомные спирты | Предельные многоатомные спирты | Фенолы |
| Общая характеристика |
| Общая формула |
|
|
|
| Функциональная группа |
|
|
|
| Радикал |
|
|
|
| Представители |
|
|
|
| Физические свойства |
|
|
|
| Химические свойства |
| Горение |
|
|
|
| Взаимодействие с активными металлами (натрий, калий) |
|
|
|
| Реакция этерификации (взаимодействие с органическими кислотами, на примере уксусной кислоты) |
|
|
|
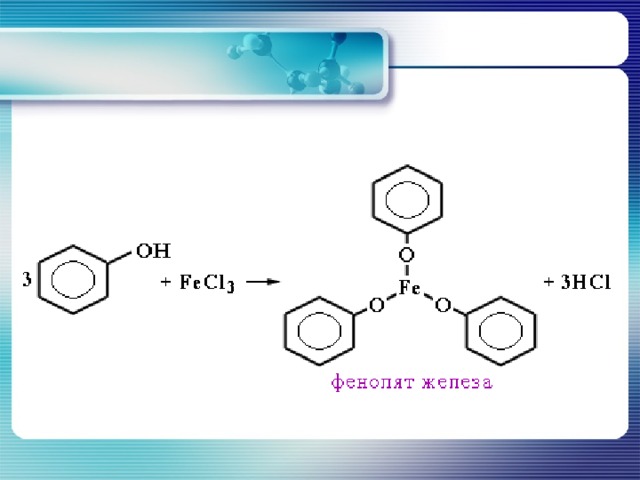
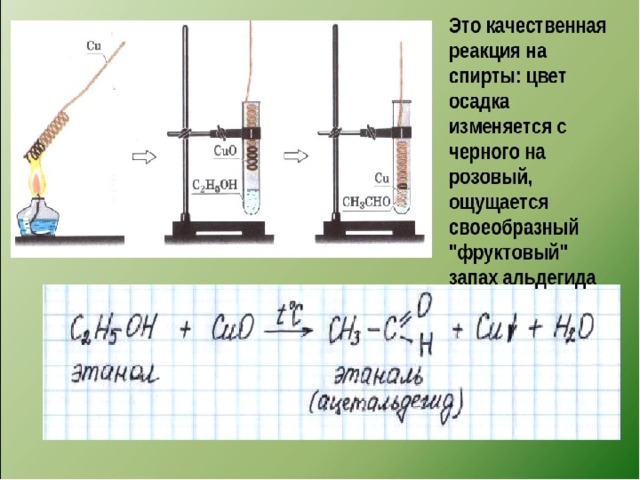
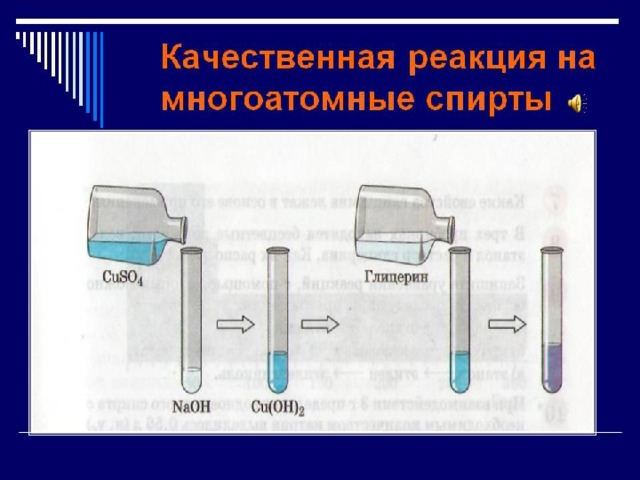
| Качественная реакция |
|
|
|