ПРАКТИЧЕСКАЯ РАБОТА №1.
Название работы: Определение водорода, углерода и хлора в органических веществах.
Цель работы: _____________________________________________________
__________________________________________________________________
С техникой безопасности знаком (а) ___________________________
| Действия | Наблюдения | Уравнения реакций. Выводы |
| Опыт №1. Определение углерода и водорода 


|
| Ca(OH)2 + CO2 →
CuSO4 + 5H2O →
C 16H34 + CuO 16H34 + CuO
|
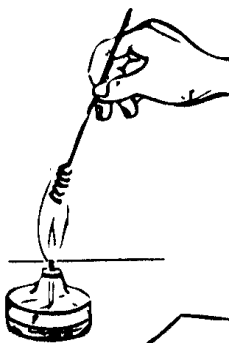
| Опыт №2. Определение хлора  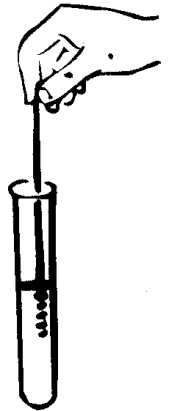
  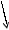
|
|
|
Вывод:___________________________________________________________________________________________________________________________________________________________________________________________________________________
Приведите рабочее место в порядок. Оценка ______________
ИНСТРУКЦИЯ К ПРАКТИЧЕСКОЙ РАБОТЕ № 1
КАЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ УГЛЕРОДА, ВОДОРОДА И ХЛОРА В ОРГАНИЧЕСКИХ ВЕЩЕСТВАХ
ЦЕЛЬ РАБОТЫ:научиться определять углерод, водород и хлор в органических соединениях.
ОБОРУДОВАНИЕ И РЕАКТИВЫ:
лабораторный штатив, нагревательный прибор, простейший прибор для получения газов, держатель, фарфоровая чашка, парафин, оксид меди(II), известковая вода, прокаленный сульфат меди(II), медная проволочка 10 см., раствор тетрахлорметана.
ВИДЕООПЫТ: http://orgchem.ru/chem2/vid/u1_1vid.htm
ИНСТРУКЦИЯ ПО ТЕХНИКЕ БЕЗОПАСНОСТИ:
1.Пробирка закреплена правильно, если она не выпадает из лапки и может быть слегка повернута вокруг своей оси.
2.Нагревайте осторожно сначала всю пробирку, а затем, не вынимая ее из пламени, ту часть, где находится вещество.
3.Направляйте отверстие нагреваемой пробирки в сторону от себя и соседей, избегая выбрасывания жидкости.
4.Не наклоняйтесь над нагреваемой пробиркой.
5.При пользовании нагревательным прибором запрещается:
- передача зажженного нагревательного прибора.
- зажигание одного нагревательного прибора от другого.
6.Гасите, только накрывая пламя колпачком.
7.Выньте газоотводную трубку из пробирки с водой, не прекращая нагревания пробирки с веществом, в противном случае воду из пробирки может перебросить в раскаленную пробирку с веществом!
ХОД РАБОТЫ:
Опыт № 1. Обнаружение углерода и водорода окислением оксидом меди (II)
Соберите прибор, как показано на рисунке.
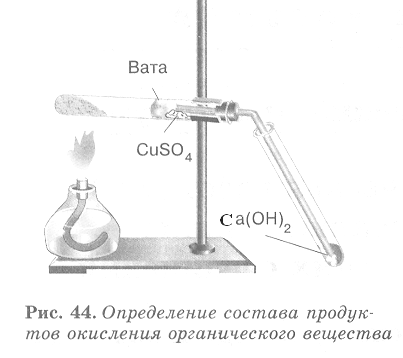 Смесь 1 — 2 г оксида меди (П) и 0,2 г парафина хорошо перемешайте и поместите на дно пробирки. Сверху насыпьте еще немного оксида меди (П). В верхнюю часть пробирки введите в виде пробки небольшой кусочек ваты и насыпьте на нее тонкий слой белого порошка безводного сульфата меди (П). Закройте пробирку пробкой с газоотводной трубкой. При этом конец трубки должен почти упираться в комочек ваты с сульфатом меди (П). Нижний конец газоотводной трубки должен быть погружен в пробирку с свежеприготовленным раствором известковой воды (раствор гидроксида кальция) Нагрейте пробирку в течении 2-3 мин. Если пробка плотно закрывает пробирку, то через несколько секунд из газоотводной трубки начнут выходить пузырьки газа. Как только известковая вода помутнеет, пробирку с ней следует удалить (что и продолжать нагревание, пока пары воды не достигнут белого порошка сульфата меди(П) и не вызовут его посинения.
Смесь 1 — 2 г оксида меди (П) и 0,2 г парафина хорошо перемешайте и поместите на дно пробирки. Сверху насыпьте еще немного оксида меди (П). В верхнюю часть пробирки введите в виде пробки небольшой кусочек ваты и насыпьте на нее тонкий слой белого порошка безводного сульфата меди (П). Закройте пробирку пробкой с газоотводной трубкой. При этом конец трубки должен почти упираться в комочек ваты с сульфатом меди (П). Нижний конец газоотводной трубки должен быть погружен в пробирку с свежеприготовленным раствором известковой воды (раствор гидроксида кальция) Нагрейте пробирку в течении 2-3 мин. Если пробка плотно закрывает пробирку, то через несколько секунд из газоотводной трубки начнут выходить пузырьки газа. Как только известковая вода помутнеет, пробирку с ней следует удалить (что и продолжать нагревание, пока пары воды не достигнут белого порошка сульфата меди(П) и не вызовут его посинения.
После изменения окраски сульфата меди (П) следует прекратить нагревание.
При протекании реакции:
– парафин окисляется в присутствии оксида меди (II). При этом углерод превращается в углекислый газ, а водород – в воду:
– выделяющийся углекислый газ взаимодействует с гидроксидом кальция, что вызывает помутнение известковой воды вследствие образования нерастворимого карбоната кальция:
– сульфат меди (II) приобретает голубую окраску при взаимодействии с водой, в результате чего образуется кристаллогидрат CuSO4 · 5Н2О.
Опыт №2. Качественное определение хлора в молекулах галогенопроизводных углеводородов
Д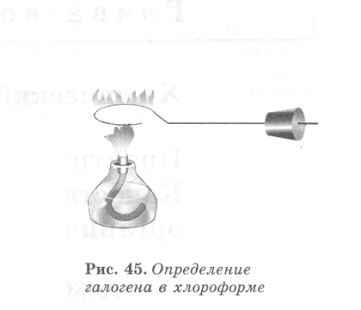 ля проведения опыта требуется медная проволока длиной около 10 см, загнутая на конце петлей и вставленная другим концом в держатель.
ля проведения опыта требуется медная проволока длиной около 10 см, загнутая на конце петлей и вставленная другим концом в держатель.
Прокалите петлю проволоки до исчезновения посторонней окраски пламени. Остывшую петлю, покрывшуюся черным налетом оксида меди (П), опустите в пробирку с хлороформом, затем смоченную веществом петлю вновь внесите в пламя горелки. Немедленно появляется характерная зеленовато-голубая окраска пламени, так как образующиеся при сгорании летучие галогениды меди окрашивают пламя горелки.








 16H34 + CuO
16H34 + CuO



 Смесь 1 — 2 г оксида меди (П) и 0,2 г парафина хорошо перемешайте и поместите на дно пробирки. Сверху насыпьте еще немного оксида меди (П). В верхнюю часть пробирки введите в виде пробки небольшой кусочек ваты и насыпьте на нее тонкий слой белого порошка безводного сульфата меди (П). Закройте пробирку пробкой с газоотводной трубкой. При этом конец трубки должен почти упираться в комочек ваты с сульфатом меди (П). Нижний конец газоотводной трубки должен быть погружен в пробирку с свежеприготовленным раствором известковой воды (раствор гидроксида кальция) Нагрейте пробирку в течении 2-3 мин. Если пробка плотно закрывает пробирку, то через несколько секунд из газоотводной трубки начнут выходить пузырьки газа. Как только известковая вода помутнеет, пробирку с ней следует удалить (что и продолжать нагревание, пока пары воды не достигнут белого порошка сульфата меди(П) и не вызовут его посинения.
Смесь 1 — 2 г оксида меди (П) и 0,2 г парафина хорошо перемешайте и поместите на дно пробирки. Сверху насыпьте еще немного оксида меди (П). В верхнюю часть пробирки введите в виде пробки небольшой кусочек ваты и насыпьте на нее тонкий слой белого порошка безводного сульфата меди (П). Закройте пробирку пробкой с газоотводной трубкой. При этом конец трубки должен почти упираться в комочек ваты с сульфатом меди (П). Нижний конец газоотводной трубки должен быть погружен в пробирку с свежеприготовленным раствором известковой воды (раствор гидроксида кальция) Нагрейте пробирку в течении 2-3 мин. Если пробка плотно закрывает пробирку, то через несколько секунд из газоотводной трубки начнут выходить пузырьки газа. Как только известковая вода помутнеет, пробирку с ней следует удалить (что и продолжать нагревание, пока пары воды не достигнут белого порошка сульфата меди(П) и не вызовут его посинения. ля проведения опыта требуется медная проволока длиной около 10 см, загнутая на конце петлей и вставленная другим концом в держатель.
ля проведения опыта требуется медная проволока длиной около 10 см, загнутая на конце петлей и вставленная другим концом в держатель.









