Практическая работа № 4
Тема: Приготовление растворов с определенной массовой долей растворенного вещества
Цель: Научиться выполнять расчеты массовой доли растворенного вещества в растворе
и готовить растворы с определенной массовой долей растворенного вещества.
Оборудование и реактивы: мерный цилиндр, коническая колба, стеклянная палочка, рычажные весы, разновесы, шпатель, химические стаканы, хлорид натрия, сахар, вода.
Ход работы:
Опыт 1: Приготовление раствора сахара и расчёт его массовой доли в растворе
Отмерьте мерным цилиндром 50 мл дистиллированной воды и влейте её в коническую колбу.
Чайную ложку сахарного песка (или два кусочка) взвесьте на лабораторных весах, затем поместите его в колбу с водой и перемешивайте стеклянной палочкой до полного растворения.
Теперь приступайте к расчётной части. Вначале рассчитайте массовую долю сахара в растворе. Необходимые данные у вас есть: масса сахара, объём воды, плотность воды примите равной 1 г/мл.

m(p-p) = m(cax.) + m(вода),
m(вода) = V(вода) • р(вода).
Вы также сможете рассчитать, сколько молекул сахара содержится в полученном растворе, используя известные вам соотношения:
N(мол. сах.) = NA ∙ n(сах.),
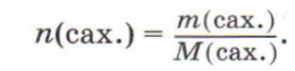
Поскольку сахар состоит на 99,9% из сахарозы, имеющей формулу С12Н22О11, вы легко рассчитаете молярную массу сахара и затем найдёте число молекул сахара в полученном вами растворе.
Опыт 2. Приготовление раствора с заданной массовой долей растворённого вещества.
В кулинарных книгах и пособиях по домашнему консервированию нередко предлагается приготовить раствор с заданной массовой долей растворенного вещества. Как это сделать?
| Вариант | Растворенное вещество | Раствор 1 | Раствор 2 | Раствор 3 |
| 1 | Хлорид натрия | 50 г 10 % - ный | 6 % - ный | 8 % - ный |
| 2 | Хлорид натрия | 30 г 10 % - ный | 4 % - ный | 7 % - ный |
Приготовление раствора 1: Рассчитайте массу твёрдого вещества и воды, необходимых для приготовления раствора 1. Зная, что плотность воды равна 1 г/мл, рассчитайте объём воды, необходимый для приготовления раствора. Взвесьте твёрдое вещество в соответствии с рассчитанной массой и перенесите в химический стакан. Мерным цилиндром отмерьте вычисленный объём воды и прилейте его к веществу в химическом стакане. Перемешивая содержимое стакана стеклянной палочкой, добейтесь полного растворения вещества в воде. Приготовленный раствор отдайте учителю.
Приготовление раствора 2: Рассчитайте массу воды, которую необходимо добавить к раствору l, чтобы получить раствор 2 меньшей концентрации. Рассчитайте объём воды. Отмерьте воду с помощью мерного цилиндра и добавьте в раствор 1. Какова масса раствора 2?
Приготовление раствора 3: Рассчитайте массу твёрдого вещества, которое следует добавить к раствору 2, чтобы получить раствор З большей концентрации. На весах взвесьте необходимую массу вещества, добавьте его в раствор 2 и перемешайте стеклянной палочкой до полного растворения. Какова масса раствора 3?
Вывод:
Образец расчетов
































