Настоящий материал представляет собой руководство (инструкцию) к практической работе и предназначен для обучающихся девятых классов. Данная инструкция содержит подробное описание (цель работы, оборудование и реактивы, порядок выполнения и оформления работы), что поможет учителю подготовиться к уроку, грамотно организовать работу обучающихся, быстро проверить правильность их записей по имеющимся образцам. Такая структура оформления работы приучает учащихся к аккуратности, четкости и грамотному изложению материала.
Прежде чем приступить к лабораторным и практическим работам, необходимо провести инструктаж по правилам техники безопасности при работе в кабинете химии с целью предотвращения травм и ожогов, а также порчи лабораторного оборудования.
Просмотр содержимого документа
«Практическая работа. Решение экспериментальных задач по теме: "Металлы"»
Практическая работа № 7
Решение экспериментальных задач по теме «Металлы»
Рабочее место № ___
Цель работы: изучить химические свойства амфотерных гидроксидов и научиться составлять уравнения реакций с ними.
Оборудование (проверить наличие): сухие пробирки (5 шт.)
Реактивы (проверить наличие): растворы сульфата алюминия, сульфата меди (II), хлорид железа (III), гидроксида натрия или калия, соляной кислоты, роданида (тиоционата) калия.
| Техника безопасности |
| 
| Едкое вещество! Избегать попадания на кожу рук и одежду! |
| 
| Токсичное вещество! Избегать попадания на кожу рук и внутрь! |
| Избегайте попадания реактивов на рабочие поверхности! |
Ход работы
Задание 1. Получение гидроксида алюминия и изучение его свойств
Используя выданные растворы веществ, получите гидроксид алюминия из сульфата алюминия и изучите его свойства.
.сульфата, пробирку-10
апишите уравнение реакции к данному опыту, отметьте наблюдения.Al2(SO4)3 + NaOH → . . .+ . . .
рис. 1. Образец выполнения опытов
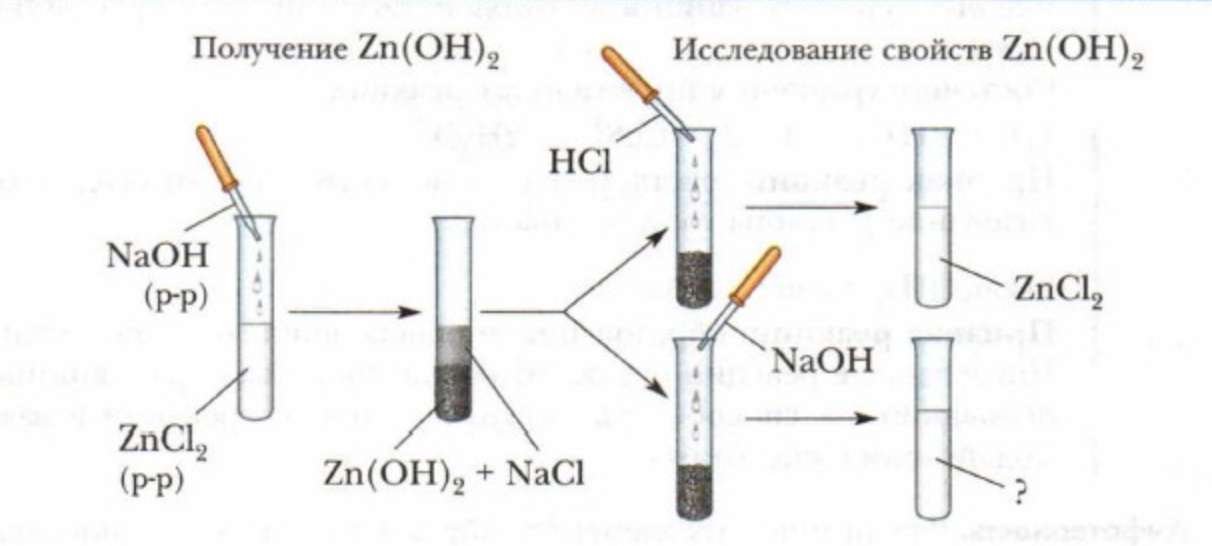 ервойприлейте 1 мл. а
ервойприлейте 1 мл. а
Запишите уравнение реакции к данному опыту, отметьте наблюдения.Al(OH)3 + . . . → . . . + . . .К содержимому второй пробирки прилейте 1 мл. раствора щёлочи (гидроксида натрия или калия). Идёт ли реакция?
Запишите уравнение реакции к данному опыту, отметьте наблюдение.
Al(OH)3 + . . . → (?) . . . + . . .Сделайте вывод о свойствах гидроксида алюминия.Задание 2. Получение гидроксида меди (II) и изучение его свойств
Используя выданные растворы веществ, приготовьте гидроксид меди (II) и исследуйте его свойства (изучите его растворимость в кислотах и щелочах). Проявляет ли он амфотерные свойства?
Запишите уравнения реакций в молекулярном виде. Отметьте наблюдение. Сделайте вывод о свойствах гидроксида меди (II).
Задание 3. Получение соединений железа (III)
Используя необходимые реактивы, выполните следующие превращения:
FeCl3 → Fe(OH)3 → FeCl3 → Fe(SCN)3
Запишите три уравнения реакций в молекулярном виде. Отметьте наблюдения.
FeCl3 + . . . → Fe(OH)3↓ + . . .
Наблюдение: ...
Fe(OH)3 + . . . → FeCl3 + . . .
Наблюдение: ...
FeCl3 + . . . → Fe(SCN)3 + . . .
Наблюдение: ...
После окончания работы помойте посуду, наведите порядок на рабочем месте и сдайте его учителю или лаборанту






 ервойприлейте 1 мл. а
ервойприлейте 1 мл. а









