
Из чего же ,из чего же, из чего же сделаны
автомобили?
Цель работы:
1. Выяснить какие металлы и сплавы стоят на службе самого распространенного транспорта в мире.
2. Исследовать, какие условия способствуют, а какие препятствуют коррозии стали.
Задачи:
1.Изучить литературу, Интернет –ресурсы по вопросам темы исследования.
2. Сформировать знания и представления о металлах, сплавах, ВМС, используемых в автомобилестроении;
3.Узнать каковы перспективы нанотехнологии в автомобильной промышленности.
4. Исследовать зависимость скорости коррозии от присутствия кислорода.
5. Исследовать влияние электролитов на процесс коррозии.
6. Исследовать влияние ингибиторов на процесс коррозии.
Методы исследования: н аучно – поисковый и исследовательский методы, через изучение литературы по данной теме и выполнение экспериментальной части.
Гипотеза: Использование металлов в машиностроении – своеобразна драма: и хорошо , и уж больно велики потери и издержки.
Объект исследования – металлы и сплавы, используемые в автомобилестроении. Коррозия железа.
Предмет исследования – свойства металлов и сплавов. Условия, влияющ ие на скорость коррозии.

Методы исследования: н аучно – поисковый и исследовательский методы, через изучение литературы по данной теме и выполнение экспериментальной части.
Гипотеза: Использование металлов в машиностроении – своеобразная драма: и хорошо , и уж больно велики потери и издержки.
Объект исследования – металлы и сплавы, используемые в автомобилестроении. Коррозия железа.
Предмет исследования – свойства металлов и сплавов. Условия, влияющие на скорость коррозии.

" С давних пор , - писал Д. Гильберт, - никакой другой вопрос так
глубоко не волновал человеческую мысль, как вопрос о бесконечном
Михаил Васильевич Ломоносов (1711 – 1765) – великий русский ученый, химик, физик, художник, историк, поэт ...

Современный толковый словарь русского языка Т.Ф.Ефремовой - "БЕЗДНА"
бездна [бездна] ж. 1) а) Глубина, кажущаяся неизмеримой, не имеющей дна; пропасть. б) Беспредельность неба, вселенной. в) Бесконечность времени. 2) перен. Резко выраженные различия, глубокие расхождения, разделяющие кого-л. 3) перен. разг. Неопределенно большое количество, множество кого-л., чего-л. 4) устар. Ад, преисподняя.
Множество кого - или чего-либо…И сразу всплывают в глубинах подсознания незатейливый мотив:
Автомобили, автомобили
Буквально все заполонили
Там где вековая лежала пыль
Свой след оставил автомобиль ...

1. Вселенная –кузница химических элементов.
Li
C Al
Mg Fe
Au Ir
Au Ir
Pb
Cu
Zn
Sn

Медь и свинец соединились с серой и всплыли на поверхность Земли, а иридий золото и железо опустились в глубины и растворились в ядре.
3 млрд. назад сформировались океаны. Вода растворила остатки железа. Земля осталась практически без золота, иридия и железа.

Но потом появились оксифотобактерии, которые производили кислород в процессе фотосинтеза. А кислород вступал в реакцию с растворенным железом, на дне формировался осадок, который позже дал начало рудникам.
Жизнь ранних растений подарила нам железо, а их смерть – топливо для машин( бензин).

Кончик свечи зажигания изготовлен из иридия.
Тот иридий, который добывают на поверхности ещё одна загадка Вселенной.

«Никто не должен спешить высмеивать гипотезы. Ведь именно они – единственное, при помощи чего величайшие умы мира смогли совершить открытия» .М.В.Ломоносов
Астероиды – это космическая служба доставки металлов. Многие ученые считают, что рудники – это места падения астероидов. Кто знает, может астероиды ,богатые металлами- это будущее и не такое далёкое
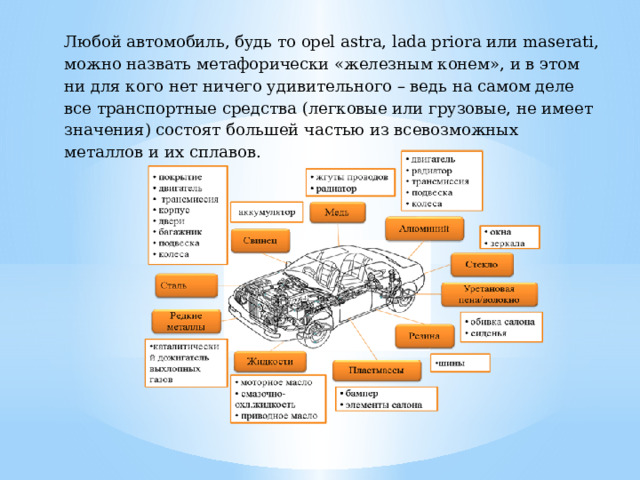
Любой автомобиль, будь то opel astra, lada priora или maserati, можно назвать метафорически «железным конем», и в этом ни для кого нет ничего удивительного – ведь на самом деле все транспортные средства (легковые или грузовые, не имеет значения) состоят большей частью из всевозможных металлов и их сплавов.



. Родий обладает хорошими отражающими свойствами, им покрывают поверхность фар и зеркал. Иридиевые свечи имеют лучшие показатели, чем платиновые
Серебро, палладий и платина используются в производстве автомобильной электроники - выключателей, датчиков давления, сигнализаторов, а так же для пластин аккумуляторов с улучшенными характеристиками. Для прерывателей, регуляторов напряжения, аварийных датчиков, некоторых реле, тахометров помимо серебра используется так же платина и золото, генераторы содержат палладий.

Автопром лидирует в нанореволюции
Спрос потребителей на удобный, экономичный и безопасный автомобиль служит ориентиром для проведения изысканий .

Проблема защиты металлов от коррозии, знакомая человечеству с древних времен, по сей день остается чрезвычайно актуальной

Практическая часть
1. Экспериментальная работа № 1 Роль кислорода в процессе коррозии стали.
В пробирку № 1-ст. гвоздь+вода на половину.
В пробирку № 2-ст. гвоздь+вода полностью.
В пробирку№ 3-ст. гвоздь-вода+масло.
Больше ржавчины образуется в пробирке № 1 — сталь соприкасается и с водой и с кислородом. В пробирке № 2 ржавчины меньше т. к. стали соприкасается только с водой. В пробирке № 3 гвоздь почти не проржавел, кислород не смог пройти через слой масла, а без кислорода коррозия не развивается

2. Экспериментальная работа № 2 .Влияние электролитов на процесс коррозии.
В пробирку № 1-ст. гвоздь + вода.
В пробирку № 2-ст. гвоздь + раствор хлорида натрия.
В пробирку № 3-ст. гвоздь + медь + раствор хлорида натрия.
В пробирку № 4-ст. гвоздь + алюминий + раствор хлорида натрия.
В пробирку №5-ст.гвоздь + припой(олово +свинец)

3. Экспериментальная работа № 3. Влияние ингибиторов на процесс коррозии.
В пробирку № 1 - ст. гвоздь + раствор гидроксида натрия.
В пробирку № 2 - ст. гвоздь + раствор фосфата натрия.
В пробирку № 3 - ст. гвоздь + раствор дихромата натрия.
Коррозия стали в данном случае отсутствует. Следовательно, эти вещества замедляют коррозию, являются ингибиторами.

Опыт №4.
Действие стимулятора коррозии.
Взять две пробирки, в одну налить раствор CuSO4 , в другую – CuCl2. В каждую из пробирок опустить по кусочку алюминия. Алюминий покрыт защитной плёнкой оксида Al2O3 . При разрушении этой плёнки возможно вытеснение меди из раствора её соли более активным металлом (алюминием). Вытеснение меди в первой пробирке идёт очень медленно, во второй – быстро.
CuCl 2 + Al → AlCl 3 + Cu 0
CuSO 4 + Al → Al 2 (SO4) 3 +Cu 0

Опыт 5. Влияние поверхности металла на скорость коррозии.
1) В две пробирки с раствором серной кислоты опустите по одной грануле цинка, взяв одну гладкую (новую), а другую шероховатую (ранее использованную). Убедитесь, что однородность поверхности металла влияет на скорость коррозии.
2) В две пробирки налейте по 1 мл раствора серной кислоты (1:5). Опустите в одну пробирку новую гранулу цинка, в другую – гранулу цинка, смоченную предварительно раствором медного купороса, т.е. загрязненную. Убедитесь, что металлы чистые и загрязненные корродируют с разной скоростью.
Гладкая поверхность и загрязнённая поверхность металла ускоряют коррозию.



































