Просмотр содержимого документа
«Презентация к уроку "Соли"»

В древности она служила деньгами, а в некоторых культурах ею расплачивались вместо золота.


3 марта
Тема: «Соли, их классификация и химические свойства»

Соли – сложные вещества, которые состоят из атомов металла и кислотного остатка

Классификация солей
Основные
Средние или нормальные
Кислые
(CuOH) 2 CO 3
ZnOHCl
NaHCO 3 Ca(H 2 PO 4 ) 2
NaCl CaCO 3 K 2 SiO 3 Ba(NO 3 ) 2 NH 4 Cl

NaHCO₃
CaCO₃
Mg(OH)Cl

Образование названий солей
Номенклатура средних солей:
Пример
NaCl - хлорид натрия
CaCO 3 – карбонат кальция
CuSO 4 - cульфат меди (II)

Соли назвать
KCI
CaCl 2
BaCO 3

Номенклатура основных солей
Название соли
Валентность металла
(если переменная)
Гидроксо Дигидроксо
Название металла в родительном падеже
Название кислотного остатка


NaHCO₃
CaCO₃
Mg(OH)Cl

BaSO4
KCl
MgHPO4

Химические свойства
1. Взаимодействие с кислотами
Na₂CO₃ + 2HCl 2NaCl + CO 2 + H 2 O
BaCl 2 + H 2 SO 4 BaSO 4 + 2HCl
2. Взаимодействие со щелочами
CuSO₄ + 2NaOH Cu(OH) 2 + Na 2 SO 4

Химические свойства
3. Взаимодействие с металлами
CuSO₄+Fe Cu + FeSO₄
4 . Взаимодействие с растворами других солей
(признак реакции-выпадение осадка)
NaCl + AgNO ₃ NaNO 3 + AgCl
К 3 PO 4 + 3AgNO₃ 3КNO ₃ + Ag 3 PO 4
NaI + AgNO₃ NaNO 3 + AgI


Задача
Физиологический раствор представляет собой смесь хлорида натрия (NaCl) и воды и имеет ряд применений в медицине. Он используется для очистки ран, снятия и хранения контактных линз, а также помогает при сухости глаз.
Как приготовить 200г 15% - ного раствора поваренной соли ?

Дано: Решение:
m(р-ра)=200 г Формула для расчета массовой доли вещества в растворе:
ω= 15% ω (в-ва)= (m вещества / m раствора) * 100%
Находим массу соли:
m(в-ва)-? m(в-ва) = (ω(в-ва) * m(раствора)) / 100% ( Массу соли) m(в-ва) = (15% * 200 г) / 100% m(в-ва) = 30 г.
Находим массу воды: Раствор состоит из соли и воды. Поэтому: m(воды) = m(раствора) - m(в-ва) m(воды) = 200 г - 30 г m(воды) = 170 г.

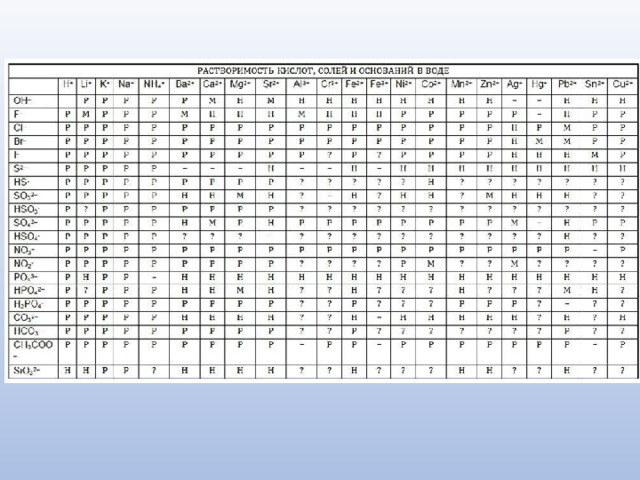
Зеленый — растворимые соли (всё прозрачно и понятно).
Желтый — малорастворимые или цветные соли (есть нюансы)
Красный — нерастворимые соли (выпал в осадок, ничего не усвоил).

Домашнее задание: 1. Дома на кухне или в аптечке найти соли: - Изучить состав на упаковке и найти знакомые химические формулы.
-К лассифицировать соль (средняя, кислая, основная), написать формулу
- Можно сделать фото и показать на следующем уроке.
2. № 4 стр. 115





































