
Доброе утро!

Строение атома. Состав атомных ядер. Изотопы

Цели урока: 1. Узнать из каких частиц состоит атом ? 2.Как определять состав атомных ядер? 3.В чем отличие строения атомов и изотопов.

Атомистические представления
Атом ( atomos – неделимый )
Демокрит , Эпикур 2500 лет назад
начало 19 века
- Все вещества состоят из атомов
- Атомы отличаются друг от друга массой и размерами
- Атомы соединяются в молекулы
Джон Дальтон

АТОМ-
Наименьшая частица химического элемента, являющаяся носителем его свойств.
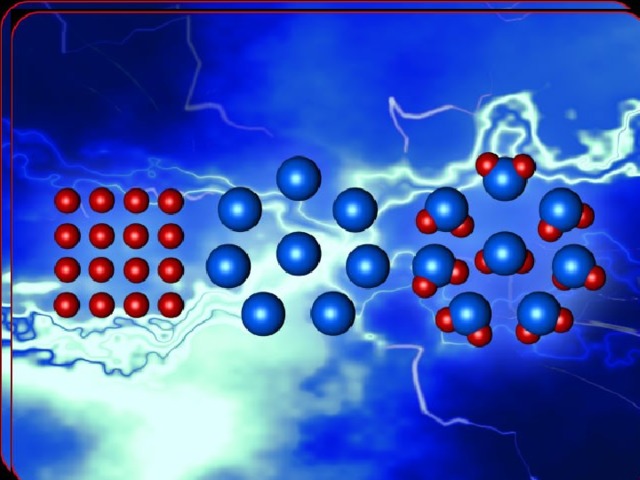
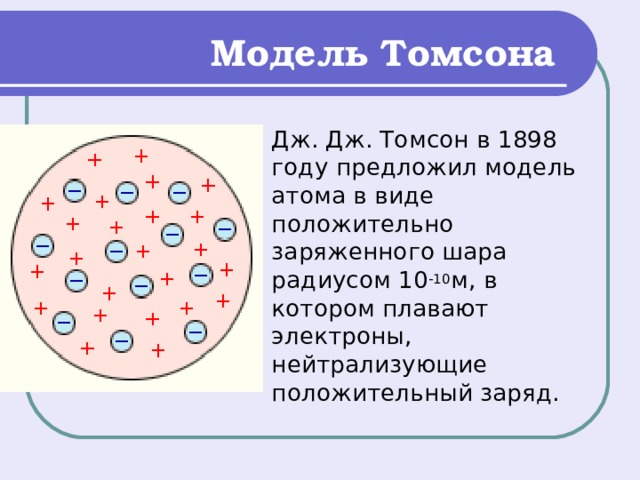
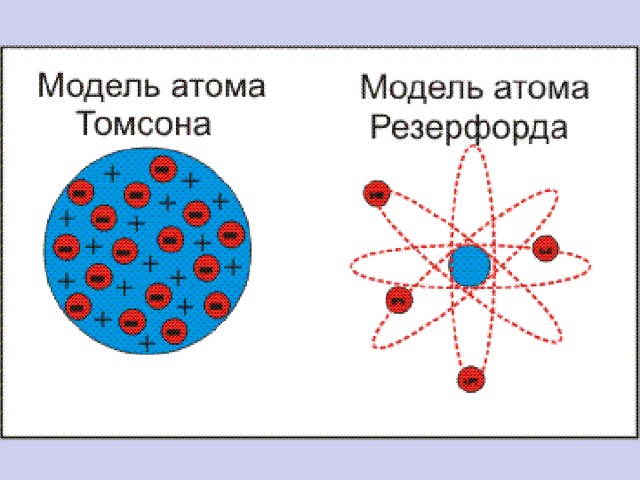
Модель Томсона
Дж. Дж. Томсон в 1898 году предложил модель атома в виде положительно заряженного шара радиусом 10 -10 м, в котором плавают электроны, нейтрализующие положительный заряд.

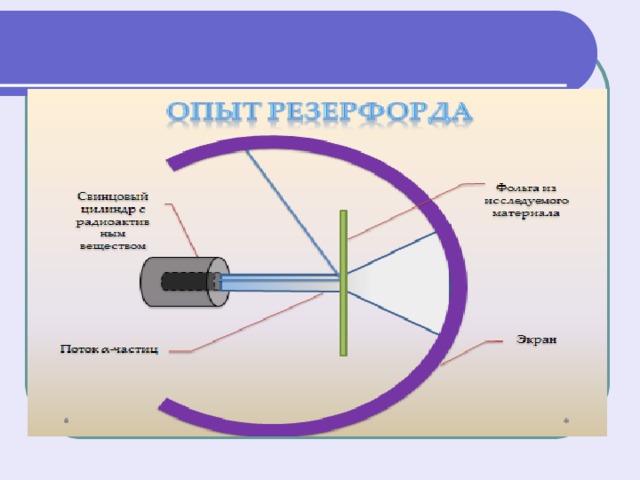
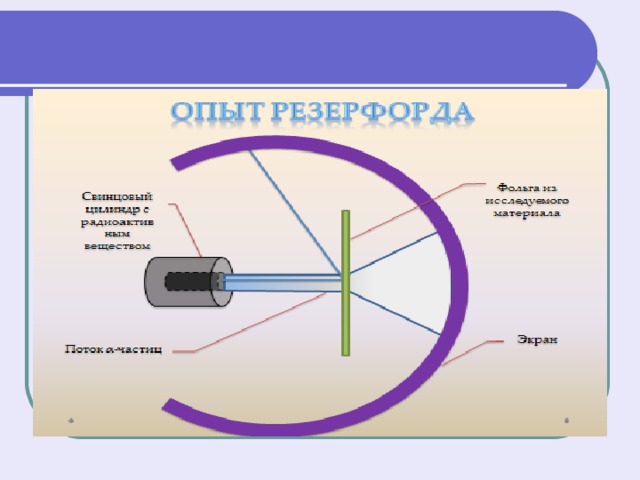
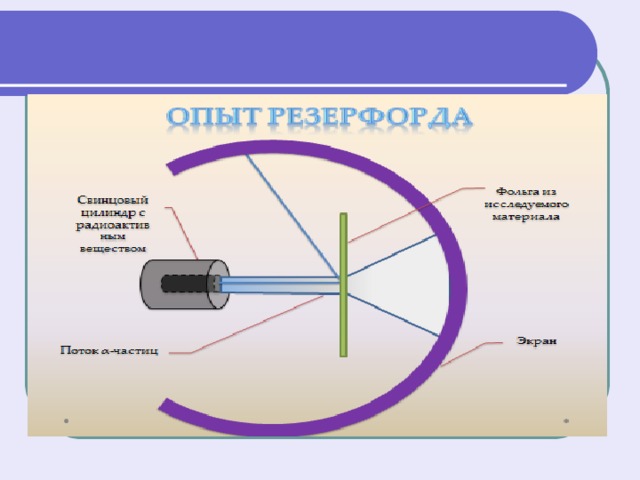
Модель Резерфорда ядерная (планетарная) модель
- Атом имеет ядро, размеры которого малы по сравнению с размерами самого атома.
- В ядре сконцентрирована почти вся масса атома.
- Отрицательный заряд всех электронов распределен по всему объему атома.


АТОМ
Состоит из ядра
Вокруг ядра вращаются электроны
В ядре находятся
Протоны
p
Нейтроны
n
+
не имеют заряда
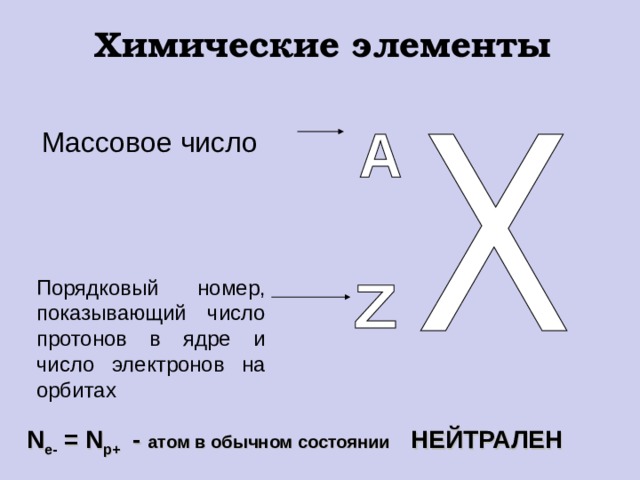
Химические элементы
Массовое число
Порядковый номер, показывающий число протонов в ядре и число электронов на орбитах
N e- = N p+ - атом в обычном состоянии НЕЙТРАЛЕН

Z - заряд ядра = порядковому номеру
химического элемента .
А –массовое число.
А= Z+N
полное число протонов и нейтронов в ядре
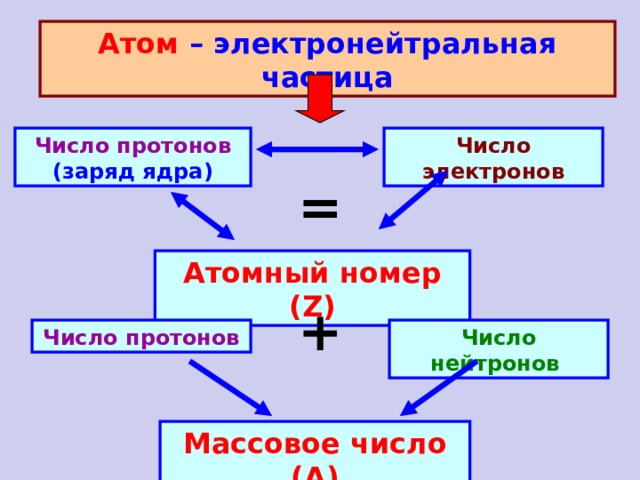
Атом – электронейтральная частица
Число протонов (заряд ядра)
Число электронов
=
Атомный номер ( Z )
+
Число нейтронов
Число протонов
Массовое число (А)
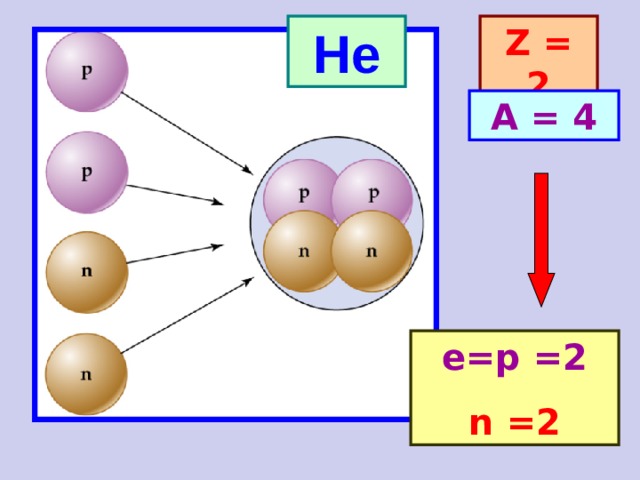
He
Z = 2
A = 4
е= p = 2
n = 2
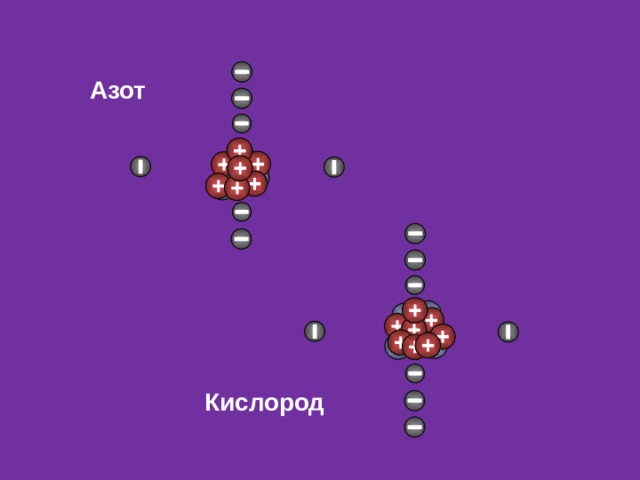
Азот
Кислород
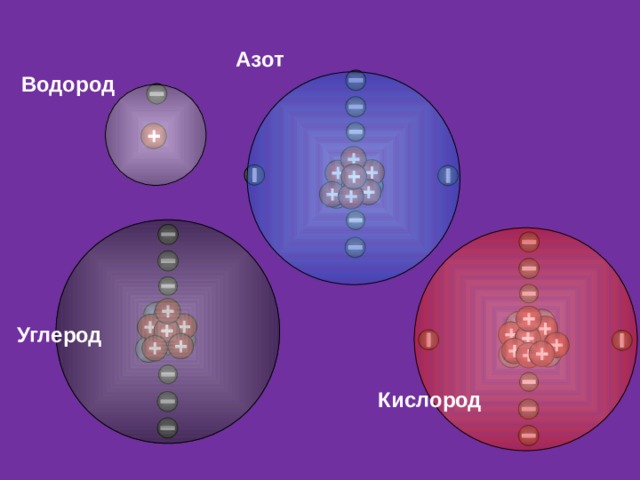
Азот
Водород
Углерод
Кислород

- N → см ПСХЭ
- N = Z = число 1 1 P
- Число 1 0 n = Ar - 1 1 P
Используя алгоритм, выполните задания

Определите состав атомных ядер у элементов с порядковым номером
16, 35, 40, 18.

Какой состав имеют атомные ядра?
1 1 H, 2 1 H, 3 1 H
число нейтронов
число протонов и заряд ядра

Изотопы – это РАЗНОВИДНОСТЬ АТОМОВ , которые имеют одинаковый порядковый номер, но разную атомную массу.

Из смеси выпишите изотопы хлора и
меди:
28 14 Si , 64 29 Cu , 18 8 O ,
23 11 Na , 11 5 B , 37 17 Cl , 27 14 Si , 26 14 Si
16 8 O , 63 29 Cu , 35 17 Cl , 17 8 O , 22 11 Na

Собрать, сколько надо, частиц всех
сортов, И атом - пожалуйста - вот он, готов! Но в общее дело их вклады неравны... Так кто же из этих частиц самый главный Пузатый протон, флегматичный нейтрон, А может быть, юркий малец электрон?
Итак, какие частицы в атоме главные ?

Что узнали?
АТОМ
↙ ↘
ЯДРО ЭЛЕКТРОН
↓ ↓ ( m=0 g=-1)
Протон Нейтрон)
m =1 m =1
g =+1 g =0
N – порядковый номер см.в ПСХЭ
N = Z = число протонов 1 1 р
Число 1 0 n = Ar – 1 1 p
ИЗОТОП → Разновидность атомов химических
элементов
↓ ↓
А r – (разная) Z (одинаковый)

Домашнее задание 1. Используя изученные на уроке термины: атом, ядро, оболочка, протон, нейтрон, электрон; фамилии ученых: Томсон, Резерфорд, составить кроссворд. 2. Сочинить историю в любом жанре (сказка, басня, детектив и т.д.): на что по-вашему похож атом? 3. Н а рабочих листах ответить на вопрос: Если бы не было открыто строение атома, то……………






















































