
КИСЛОРОД
ИДРИСОВА ХАДИШАТ АЛЬХАЗУРОВНА УЧИТЕЛЬ ХИМИИ МБОУ «СОШ № 1 С.П. НАДТЕРЕЧНОЕ НАДТЕРЕЧНОГО МУНИЦИПАЛЬНОГО РАЙОНА ЧР»

1. РАСПРОСТРАНЕНИЕ КИСЛОРОДА В ПРИРОДЕ
Первое место по распространенности в земной коре, т.е. литосфере , занимает кислород – 49%, далее следуют: кремний 26%, алюминий 7%, железо 5%, кальций 4%, натрий, калий и магний по 2%, водород 1%.
В биосфере около 65% от массы живых организмов приходится на кислород .
В гидросфере на его долю приходится 89% .

В атмосфере 23% по массе и 21% по объему .

Без этого элемента вы не проживете и десяти минут.

Оно нам хорошо известно:
Газообразный кислород ,
Которым дышат, если честно,
И человек, и бегемот.
Из элемента кислорода
(Обозначают буквой О)
Ёще придумала природа
Одно простое вещество,
Которое зовут озоном .
И в этом есть большой резон:
В грозу запахнет над газоном –
От слова «пахнущий» - озон.
Как по составу различают
Два аллотропных вещества?
О 3 озон обозначают,
А кислород – всего О 2 .

2. ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТА «КИСЛОРОД»
- Химический знак О
- Положение в ПСХЭ период II , группа VI А, порядковый номер 8
- Относительная атомная масса А r (O)=16
- Химическая формула вещества О 2
- Относительная молекулярная масса M r (O 2 )= 32
- Валентность II

Джозеф Пристли (английский ученый) в 1774 году разложением оксида ртути (II) открыл кислород и изучил его свойства.

Карл Вильгельм Шееле (шведский химик) в 1772 году получил и детально исследовал «огненный воздух», в котором горит свеча.

Антуан Лавуазье в 1774 году провел эксперимент и доказал, что воздух состоит на 1/5 часть из кислорода и 4/5 части азота. Он опроверг теорию «флогистона».

3. СПОСОБЫ ПОЛУЧЕНИЯ КИСЛОРОДА
1. В промышленности кислород получают из воздуха. Воздух представляет собой смесь различных газов, основные компоненты в нем – азот и кислород. Для получения кислорода воздух под давлением сжижают. Так как температура кипения жидкого азота (-196 ° С ) ниже температуры кипения жидкого кислорода (-183 °C ), то азот испаряется раньше кислорода. Жидкий кислород отделяют от испарившегося азота и хранят в стальных баллонах под давлением 15 МПа.

а) электролиз воды
2H 2 O = 2H 2 ↑ + O 2 ↑
б) разложение пероксида водорода
2H 2 O 2 = 2H 2 O + O 2 ↑
в) разложение хлората калия
2KClO 3 = 2KCl + 3O 2 ↑
г) разложение оксида ртути (II)
2HgO = 2Hg + O 2 ↑
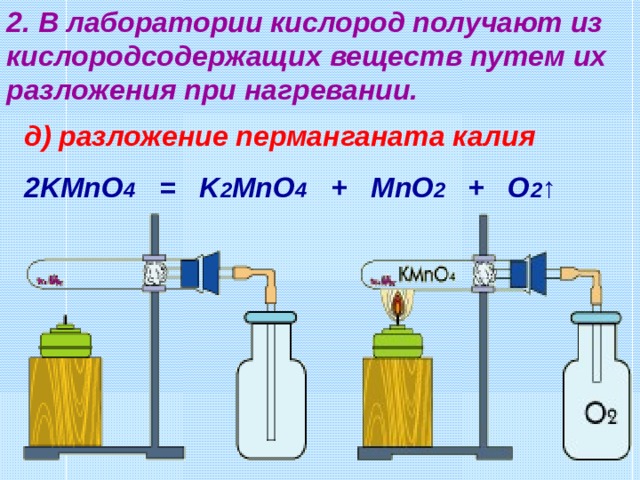
2. В лаборатории кислород получают из кислородсодержащих веществ путем их разложения при нагревании.
д) разложение перманганата калия
2KMnO 4 = K 2 MnO 4 + MnO 2 + O 2 ↑

4. ФИЗИЧЕСКИЕ СВОЙСТВА КИСЛОРОДА
Кислород – газ, без цвета и запаха, мало
растворим в воде (в 100 объемах воды
при 20 °C растворяется 3,1 объема
кислорода), кислород немного
тяжелее воздуха (1 л О 2 при нормальных
условиях (н.у.) весит 1,43 г; 1 л воздуха
при н.у.-1,29 г),температура кипения
кислорода -183 °C , температура
плавления -219 ° .

5. ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОРОДА

6. ПРИМЕНЕНИЕ КИСЛОРОДА ЧЕЛОВЕКОМ

Домашнее задание : параграфы 18-21, вопросы 1-3, задача 1, стр. 59-60
Домашнее задание : параграфы 18-21, вопросы 1-3, задача 1, стр. 59-60

































