Просмотр содержимого документа
«Презентация " Кислород, его общая характеристика, нахождение в природе и получение"»

Он без запаха, без цвета,
С углеродом даст он дым,
Им окутана планета –
Без него не быть живым.
Для дыхания он нужен,
В нем сгорают вещества.
В океане он и в луже,
Там, где зелень и листва.
Кто сейчас его узнает?
И при всех здесь назовет?
Тот, конечно, точно знает
Газ известный – кислород.

Кислород, его общая характеристика, нахождение в природе и получение.
Презентацию подготовил учитель МБОУ «Усть-Бакчарская СОШ»
Ковалёва Ю.Д.


Общая характеристика элемента КИСЛОРОД
Химический знак О
Латинское название оксигениум
Относительная атомная масса
Аr(O)=16
Химическая формула вещества О2
Относительная молекулярная масса Mr(O2)=32
Валентность II
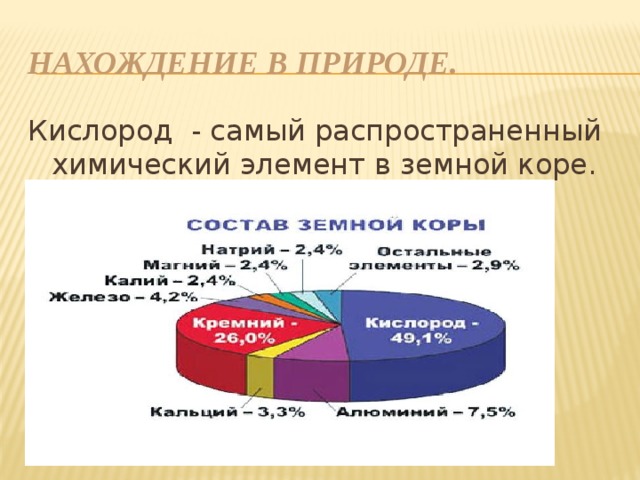
Нахождение в природе.
Кислород - самый распространенный химический элемент в земной коре.

Воздух содержит 0, 209 объёмной доли, или 21% газа кислорода, что приблизительно 1/5 по объему, или 23% по массе.

Открытие кислорода
Первым этот газ получил шведский химик Карл Вильгельм Шееле в 1772 году.

Открытие кислорода
А через два года, в 1774, не зная об опытах предшественника, - английский химик Джозеф Пристли.

Вот история простая:
Джозеф Пристли как-то раз,
Окись ртути нагревая,
Обнаружил странный газ.
Газ без цвета, без названья,
Ярче в нем горит свеча.
А не вреден для дыханья?
Не узнаешь от врача.
Новый газ из колбы вышел.
Никому он не знаком.
Этим газом дышат мыши
Под стеклянным колпаком,
Человек им тоже дышит...
Джозеф Пристли быстро пишет:
Кошка греется на крыше,
Солнца луч в окошко бьет,
Джозеф Пристли, с ним две мыши,
Открывает кислород.


2HgO = 2Hg + O₂
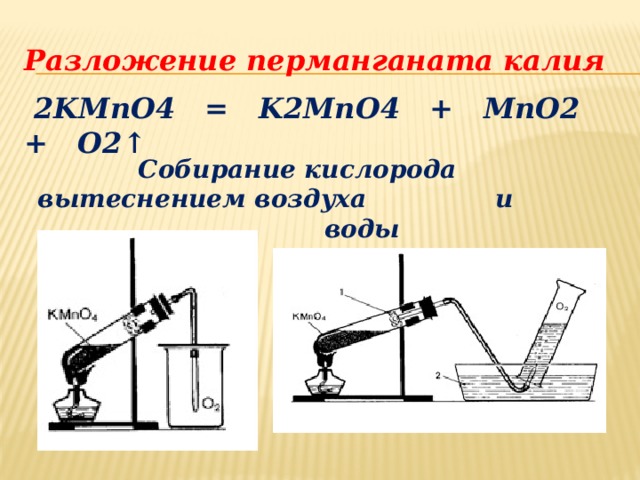
Разложение перманганата калия
2KMnO4 = K2MnO4 + MnO2 + O2 ↑
Собирание кислорода вытеснением воздуха и воды

Получение кислорода в лаборатории
Разложение пероксида водорода
MnO2
2H 2 O 2 2H 2 O + O 2 ↑
Разложение бертолетовой соли
MnO2, t
2KClO 3 2KCl + 3O 2 ↑

Получение кислорода в промышленности
В промышленности кислород получают из воздуха. Воздух представляет собой смесь различных газов, основные компоненты в нем – азот и кислород. Для получения кислорода воздух под давлением сжижают. Так как температура кипения жидкого азота (-196 °С) ниже температуры кипения жидкого кислорода (-183°C), то азот испаряется раньше кислорода. Жидкий кислород отделяют от испарившегося азота и хранят в стальных баллонах под давлением 15 МПа.































