Просмотр содержимого документа
«Презентация "Кислоты"»

Кислоты

- Кислоты – это сложные вещества, в состав молекул которых входят атомы водорода, способные замещаться или обмениваться на атомы металла.

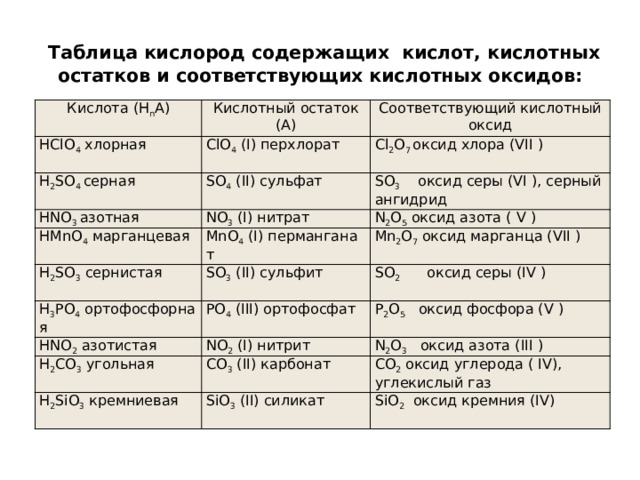
Таблица кислород содержащих кислот, кислотных остатков и соответствующих кислотных оксидов:
Кислота (Н n А)
Кислотный остаток (А)
HClO 4 хлорная
Соответствующий кислотный оксид
ClO 4 (I) перхлорат
H 2 SO 4 серная
HNO 3 азотная
SO 4 (II) сульфат
Cl 2 O 7 оксид хлора (VII )
SO 3 оксид серы (VI ), серный ангидрид
NO 3 (I) нитрат
HMnO 4 марганцевая
N 2 O 5 оксид азота ( V )
MnO 4 (I) перманганат
H 2 SO 3 сернистая
H 3 PO 4 ортофосфорная
Mn 2 O 7 оксид марганца (VII )
SO 3 (II) сульфит
SO 2 оксид серы (IV )
PO 4 (III) ортофосфат
HNO 2 азотистая
P 2 O 5 оксид фосфора (V )
NO 2 (I) нитрит
H 2 CO 3 угольная
N 2 O 3 оксид азота (III )
CO 3 (II) карбонат
H 2 SiO 3 кремниевая
CO 2 оксид углерода ( IV), углекислый газ
SiO 3 (II) силикат
SiO 2 оксид кремния (IV)
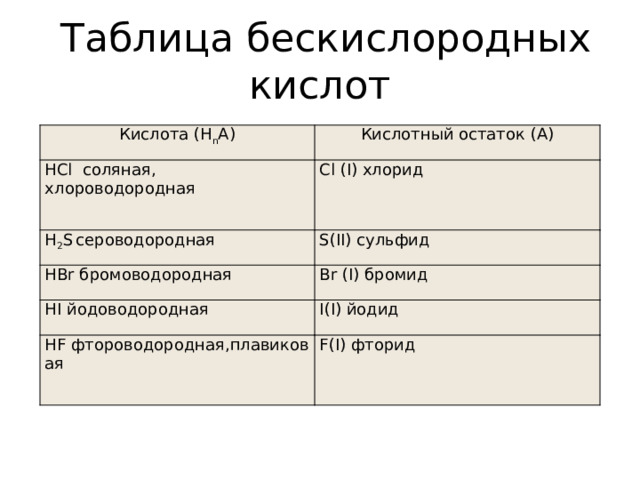
Таблица бескислородных кислот
Кислота (Н n А)
Кислотный остаток (А)
HCl соляная, хлороводородная
Cl (I) хлорид
H 2 S сероводородная
S(II) сульфид
HBr бромоводородная
Br (I) бромид
HI йодоводородная
I(I) йодид
HF фтороводородная,плавиковая
F(I) фторид

Физические свойства кислот
- Многие кислоты, например серная, азотная, соляная – это бесцветные жидкости.
- твёрдые кислоты: ортофосфорная, метафосфорная HPO 3 , борная H 3 BO 3 .
- Почти все кислоты растворимы в воде. Пример нерастворимой кислоты – кремниевая H 2 SiO 3 .
- Растворы кислот имеют кислый вкус.

Способы получения кислот
бескислородные
кислородсодержащие
HCl, HBr, HI, HF, H 2 S
HNO 3 , H 2 SO 4 и другие
ПОЛУЧЕНИЕ
1. Прямое взаимодействие неметаллов
H 2 + Cl 2 = 2 HCl
1. Кислотный оксид + вода = кислота
2. Реакция обмена между солью и менее летучей кислотой
SO 3 + H 2 O = H 2 SO 4
2 NaCl (тв.) + H 2 SO 4 (конц.) = Na 2 SO 4 + 2HCl
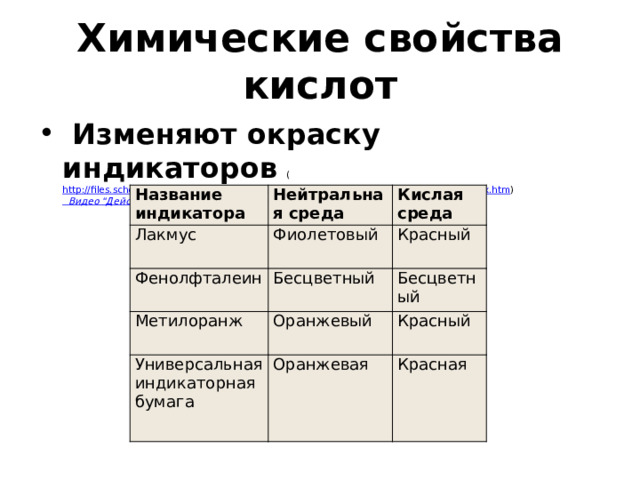
Химические свойства кислот
- Изменяют окраску индикаторов ( http://files.school-collection.edu.ru/dlrstore/273e6145-6cc8-fe8a-376e-9765c4e8a054/index.htm ) Видео "Действие кислот на индикаторы"
Название индикатора
Нейтральная среда
Лакмус
Кислая среда
Фиолетовый
Фенолфталеин
Бесцветный
Метилоранж
Красный
Бесцветный
Оранжевый
Универсальная индикаторная бумага
Оранжевая
Красный
Красная

- 2.Реагируют с металлами в ряду активности до H 2 (искл. HNO 3 –азотная кислота)
- http://files.school-collection.edu.ru/dlrstore/432f464f-1f22-5224-e016-91243ab1f09c/index.htm
- Видео "Взаимодействие кислот с металлами«
- Ме + КИСЛОТА =СОЛЬ + H 2 ↑ (р. замещения)
- Zn + 2 HCl = ZnCl 2 + H 2
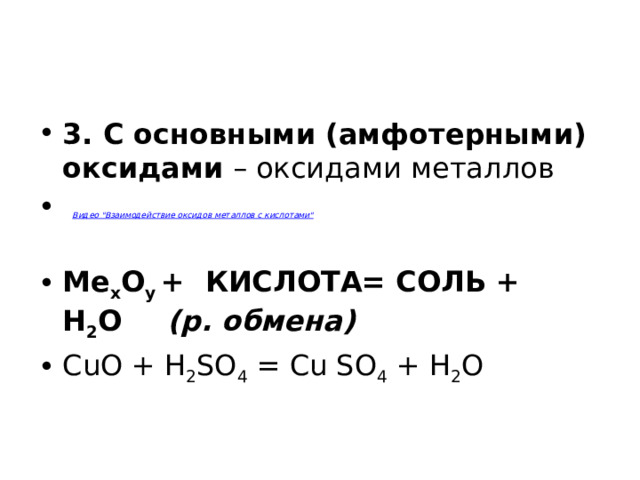
- 3. С основными (амфотерными) оксидами – оксидами металлов
- Видео "Взаимодействие оксидов металлов с кислотами"
- Ме х О у + КИСЛОТА= СОЛЬ + Н 2 О (р. обмена)
- CuO + H 2 SO 4 = Cu SO 4 + H 2 O

- 4. Реагируют с основаниями – реакция нейтрализации
-
- КИСЛОТА + ОСНОВАНИЕ= СОЛЬ+ H 2 O ( р. обмена)
- H 3 PO 4 + 3NaOH = Na 3 PO 4 + 3H 2 O

- 5. Реагируют с солями слабых, летучих кислот - если образуется кислота, выпадающая в осадок или выделяется газ:
Видео "Взаимодействие кислот с солями"
- 2 NaCl (тв.) + H 2 SO 4 (конц.) = Na 2 SO 4 + 2HCl↑ ( р. обмена)
 HClO 4 HBr HCl H 2 SO 4 HNO 3 HMnO 4 H 2 SO 3 H 3 PO 4 HF HNO 2 H 2 CO 3 H 2 S H 2 SiO 3 . Каждая предыдущая кислота может вытеснить из соли последующую " width="640"
HClO 4 HBr HCl H 2 SO 4 HNO 3 HMnO 4 H 2 SO 3 H 3 PO 4 HF HNO 2 H 2 CO 3 H 2 S H 2 SiO 3 . Каждая предыдущая кислота может вытеснить из соли последующую " width="640"
Сила кислот убывает в ряду:
HI HClO 4 HBr HCl H 2 SO 4 HNO 3 HMnO 4 H 2 SO 3 H 3 PO 4 HF HNO 2 H 2 CO 3 H 2 S H 2 SiO 3 .
Каждая предыдущая кислота может вытеснить из соли последующую

- 6. Разложение кислородсодержащих кислот при нагревании
- ( искл. H 2 SO 4 ; H 3 PO 4 )
-
- КИСЛОТА = КИСЛОТНЫЙ ОКСИД + ВОДА (р. разложения )
-
- Запомните! Неустойчивые кислоты (угольная и сернистая) – разлагаются на газ и воду :
- H 2 CO 3 ↔ H 2 O + CO 2 ↑
- H 2 SO 3 ↔ H 2 O + SO 2 ↑
- Сероводородная кислота в продуктах выделяется в виде газа:
- СаS + 2HCl = H 2 S↑ + CaCl 2
- Видео "Химические свойства соляной кислоты"

- ЗАДАНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ
- № 1. Распределите химические формулы кислот в таблицу. Дайте им названия:
- LiOH, Mn 2 O 7 , CaO, Na 3 PO 4 , H 2 S, MnO, Fe(OH) 3 , Cr 2 O 3 , HI , HClO 4 ,HBr , CaCl 2 , Na 2 O, HCl , H 2 SO 4 , HNO 3 , HMnO 4 , Ca(OH) 2 , SiO 2 , H 2 SO 3 , Zn(OH) 2 , H 3 PO 4 , HF , HNO 2 ,H 2 CO 3 , N 2 O, NaNO 3 ,H 2 S , H 2 SiO 3
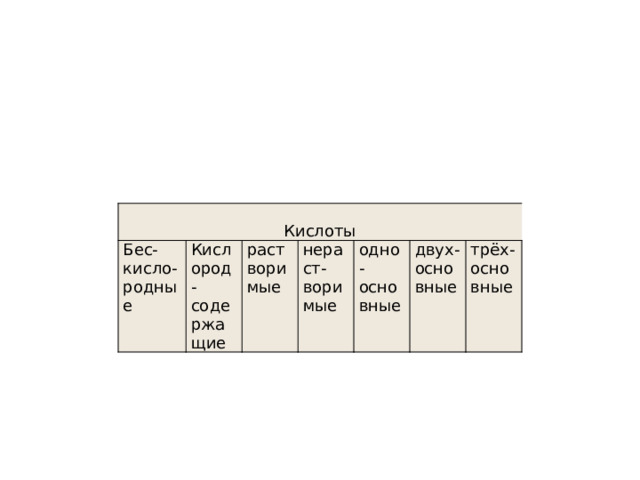
Бес-кисло-
Кислоты
родные
Кислород- содержащие
растворимые
нераст-воримые
одно-
основные
двух-основные
трёх-основные

- https://sites.google.com/site/himulacom/zvonok-na-urok/8-klass/urok-no36-kisloty-klassifikacia-nomenklatura-fiziceskie-i-himiceskie-svojstva


















 HClO 4 HBr HCl H 2 SO 4 HNO 3 HMnO 4 H 2 SO 3 H 3 PO 4 HF HNO 2 H 2 CO 3 H 2 S H 2 SiO 3 . Каждая предыдущая кислота может вытеснить из соли последующую " width="640"
HClO 4 HBr HCl H 2 SO 4 HNO 3 HMnO 4 H 2 SO 3 H 3 PO 4 HF HNO 2 H 2 CO 3 H 2 S H 2 SiO 3 . Каждая предыдущая кислота может вытеснить из соли последующую " width="640"














