
Количество вещества
и
молярный объем газов

Количество вещества —
физическая величина, характеризующая количество однотипных структурных единиц, которые содержатся в веществе .
Под структурными единицами понимаются любые частицы,
из которых состоит вещество
( атомы , молекулы , ионы
или любые другие частицы).
Единицей измерения количества вещества в СИ служит моль .

Моль – это такое количество вещества,
в котором содержится 6*10 23 молекул
(или других структурных частиц) этого вещества.

МАССА 1 МОЛЬ
ВЕЩЕСТВА НАЗЫВАЕТСЯ ЕГО
МОЛЯРНОЙ МАССОЙ ,
обозначается М
и измеряется в г/моль .
![Молярная масса - это масса одного моля вещества . М=[г/моль] ( молярная масса численно равна молекулярной массе М=Мr ) отсюда](https://fsd.multiurok.ru/html/2019/01/04/s_5c2f4558c6a91/img4.jpg)
Молярная масса
- это масса одного моля вещества .
М=[г/моль]
( молярная масса численно равна молекулярной массе М=Мr )
отсюда
![[ М] – г/моль, [ m] – г, кг/кмоль, кг, мг/ммоль. мг. [ n] –моль, кмоль, ммоль. Единицы измерения](https://fsd.multiurok.ru/html/2019/01/04/s_5c2f4558c6a91/img5.jpg)
[ М] – г/моль, [ m] – г,
кг/кмоль, кг,
мг/ммоль. мг.
[ n] –моль,
кмоль,
ммоль.
Единицы измерения

Например ,
1 моль воды имеет массу,
равную 18 грамм ,
так как Мr(Н 2 О)= 18 .
Тогда: 1 моль кислорода
имеет массу - …,
5 моль алюминия - ….,
0,1 моль натрия - ….. .
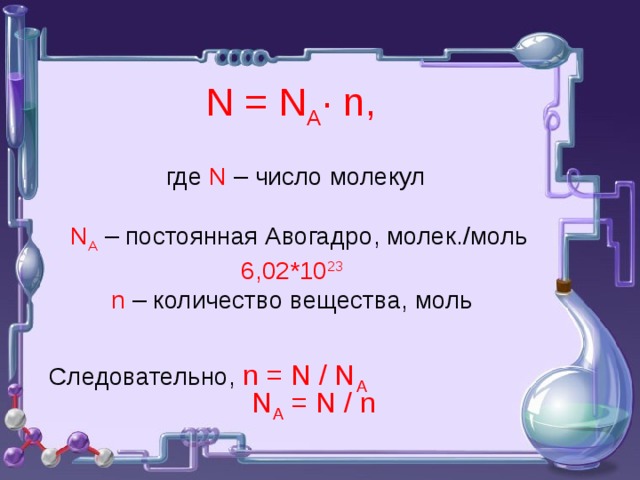
N = N A ∙ n, где N – число молекул N A – постоянная Авогадро, молек./моль
6,02*10 23
n – количество вещества, моль
Следовательно, n = N / N A
N A = N / n

Некоторое представление о величине числа Авогадро даёт следующий пример.
Количество воды, которое низвергается с ниагарского водопада (США) –
при длине 1279 м и высоте 40 м - составляет 6500 м 3 / с.
В капле воды содержится больше молекул, чем капель, упавших с Ниагарского водопада за 400 лет при условии постоянного полноводья.

Закон объемных отношений
Измеряя объемы, и объемы газов, в результате реакции Ж.Л. Гей-Люссак
открыл закон газовых (объемных) отношений:
«При постоянном давлении и температуре объемы
вступающих в реакцию газов относятся друг к другу
как небольшие простые
целые числа»
Ж.Л. Гей-Люссак
1808

Например
Химическая реакция
Отношение объемов газов
Н 2 +Cl 2 2HCl
1:1:2
2CH 4 C 2 H 2 +3H 2
2:1:3
2C+O 2 2CO
1:2
Химическая реакция
Отношение объемов газов
Н 2 +F 2 2HF
1:1:2
2CH 4 C 2 H 2 +3H 2
2:1:3
2C +O 2 2CO
1:2

Закон объёмных отношений позволил итальянскому учёному А. Авогадро предположить, что молекулы простых газов состоят из двух одинаковых атомов (Н 2 , N 2 , Cl 2 ,О 2 , F 2 … )
Всего лишь восемь элементов в природе существуют в виде двухатомных молекул:
H 2 ; N 2 ; O 2 .
И все галогены: F 2 ; Cl 2 ; Br 2 ; I 2 ; At 2.

А. Авогадро
1811
о
Итальянский ученый Амадео Авогадро сформулировал закон (для газов) :
в равных объемах различных газов при одинаковых условиях содержится одинаковое число молекул

Следствия (для газов)
- Отношение массы определённого объёма одного газа к массе такого же объёма другого газа, взятого при тех же условиях, называется плотностью первого газа по второму:
- Одно и то же число молекул различных газов при одинаковых условиях занимает одинаковые объемы.

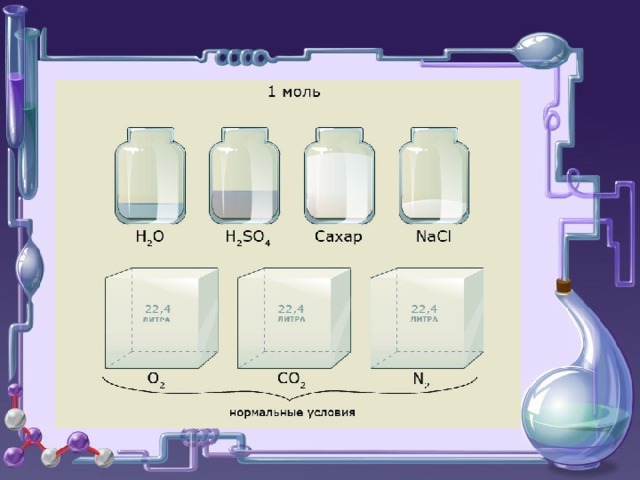
- 1 моль любого газа при н.у. занимает объем 22,4 л.
- Объем 1 моль вещества – это молярный объем ( V m )

Уравнение связи
Где n- количество вещества (моль)

Решение задач
Найдите массу 2 моль кислорода.
Дано: Решение:
n (О 2 )= 2 моль 1. n = m/ М
2. m = n х М , М=Мr
3. М (О 2 ) = 16х2=32 (г/ моль)
Найти: 4. m (О 2 ) = 32х2=64 (г)
m (О 2 ) - ?
Ответ: m (О 2 ) = 64 г

- Найдите массу 3 моль углекислого газа (СО 2 ).
- Рассчитайте массу 112 л водорода (н.у.)
- Что тяжелее: 2 моль СО 2 или 2 моль
СаО ?
- Найдите количество вещества серной кислоты (H 2 SO 4 ) массой 4,9 г
- Какой объем займет сернистый газ (SO 2 ) , масса которого равна 3,2 г?
- Найдите число молекул в 2 молях
водорода.
Задачи (закрепление)











![Молярная масса - это масса одного моля вещества . М=[г/моль] ( молярная масса численно равна молекулярной массе М=Мr ) отсюда](https://fsd.multiurok.ru/html/2019/01/04/s_5c2f4558c6a91/img4.jpg)
![[ М] – г/моль, [ m] – г, кг/кмоль, кг, мг/ммоль. мг. [ n] –моль, кмоль, ммоль. Единицы измерения](https://fsd.multiurok.ru/html/2019/01/04/s_5c2f4558c6a91/img5.jpg)































