
Алкины

Ацетиленовые углеводороды (алкины)
- это непредельные (ненасыщенные) углеводороды, содержащие в молекуле одну тройную связь и имеющие общую формулу C n H 2 n -2
! Первый в гомологическом ряду - ацетилен HC CH

Номенклатура
Названия производят от соответствующего алкана с заменой суффикса –ан на –ин .
1 2 3 4 5
CH 3 – C ≡ C – CH(CH 3 ) – CH 3
4- метилпентин-2

Изомерия
1) изомерия углеродного скелета (начиная с C 5 H 8 )
CH ≡C-CH 2 -CH 2 -CH 3 CH≡C- CH(CH 3 )- CH 3
пентин-1 3-метилбутин-1
2) изомерия положения тройной связи (начиная с C 4 H 6 )
CH ≡C-CH 2 -CH 2 -CH 3 CH 3 - C≡C-CH 2 -CH 3
пентин-1 пентин-2
3) межклассовая изомерия (алкадиены). CH ≡C-CH 2 -CH 2 -CH 3 CH 2 =CH-CH=CH-CH 3
пентин-1 пентадиен-1,3

Физические свойства
В обычных условиях
- алкины С 2 –С 3 – газы
- с С 4 -С 16 – жидкости
- высшие алкины – твердые вещества.
Наличие тройной связи в цепи приводит к повышению
температуры кипения, плотности и растворимости их
в воде по сравнению с олефинами (алкенами) и парафинами (высшими алканами).
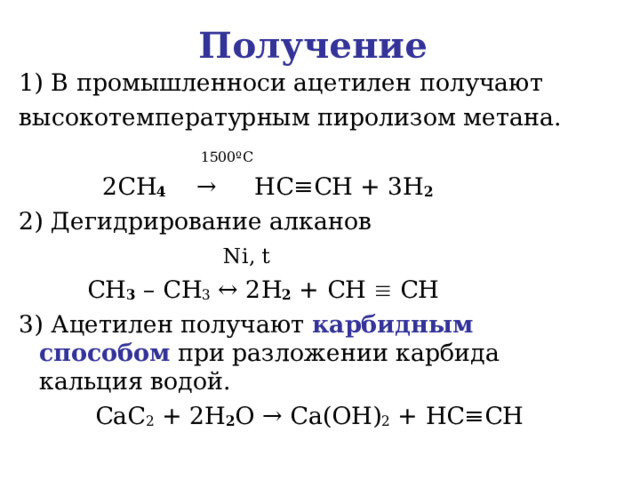
Получение
1) В промышленноси ацетилен получают
высокотемпературным пиролизом метана.
1500 º С
2 CH 4 → HC ≡ CH + 3 H 2
2) Дегидрирование алканов
Ni , t
CH 3 – CH 3 ↔ 2 H 2 + CH CH
3) Ацетилен получают карбидным способом при разложении карбида кальция водой.
CaC 2 + 2 H 2 O → Ca ( OH ) 2 + HC ≡ CH

4) Алкины можно получить
дегидрогалогенированием,
дигалогенопроизводных алканов.
С H 3 – CH ( Br )– CH 2 ( Br ) + 2 KOH → CH 3 – C ≡ CH +
+ 2 KBr + 2 H 2 O спирт. р-р
CH 3 – C ( Br 2 )– CH 2 – CH 3 +2 KOH → CH 3 – C ≡ C – CH 3 +
+ 2 KBr + 2 H 2 O спирт. р-р

Строение ацетилена
Углеродные атомы в молекуле ацетилена находятся в состоянии sp -гибридизации. Две негибридные р-орбитали одного атома углерода образуют 2 -связи с двумя р-орбиталями другого.

Химические свойства
1) Гидрирование осуществляется при нагревании с теми же металлическими катализаторами ( Ni , Pd или Pt ), что и в случае алкенов, но с меньшей скоростью.
CH 3 – C ≡ CH + H 2 → CH 3 – CH = CH 2
CH 3 – CH = CH 2 + H 2 → CH 3 – CH 2 – CH 3

2) Галогенирование. Алкины обесцвечивают бромную воду ( качественная реакция на тройную связь ). Реакция галогенирования алкинов протекает медленнее, чем алкенов.
HC ≡ CH + Br 2 → CHBr = CHBr
CHBr = CHBr + Br 2 → CHBr 2 – CHBr 2
3) Гидрогалогенирование. Образующиеся продукты определяются правилом Марковникова.
CH 3 – C ≡ CH + HBr → CH 3 – CBr = CH 2
CH 3 – CBr = CH 2 + HBr → CH 3 – CBr 2 – CH 3

- Правило В.В.Марковникова:
водород присоединяется к наиболее гидрогенизированному атому углерода при двойной связи, то есть к атому углерода с наибольшим числом водородных атомов .

4) Гидратация (реакция Кучерова). Присоединение воды осуществляется в присутствии сульфата ртути. Эту реакцию открыл и исследовал в 1881 году М.Г.Кучеров.
HgSO 4
C 2 H 5 –C ≡ CH + H 2 O → C 2 H 5 – C – CH 3
||
O

5) Полимеризация. Алкины ввиду наличия тройной связи склонны к реакциям полимеризации, которые могут протекать в нескольких направлениях:
a) Под воздействием комплексных солей меди происходит димеризация
kat HC ≡ CH + HC ≡ CH → CH 2 = CH – C ≡ CH
б) Тримеризация (для ацетилена)
C акт. , t
3С H ≡ CH → С 6 Н 6 ( бензол)

6) Водородные атомы ацетилена способны замещаться металлами с образованием ацетиленидов.
HC ≡ CH + 2 Na → NaC ≡ CNa + H 2
HC ≡ CH + Ag 2 O → AgC ≡ CAg ↓ + H 2 O
( аммиачный р-р )
HC ≡ CH + CuCl 2 → CuC ≡ CCu ↓ + 2HCl
( аммиачный р-р )

7 ) Горение ( t = 2500 ºC )
2СН СН + 4 O 2 → CO 2 + 2 H 2 O + 3 C ↓
2C 2 H 2 + 5O 2 → 4CO 2 + 2H 2 O +Q
8 ) В присутствии перманганата калия ацетилен легко окисляется в до щавелевой кислоты (обесцвечивание раствора KMnO 4 является качественной реакцией на наличие тройной связи).
3 C 2 H 2 + 8 KMnO 4 + 4 H 2 O → 3 HOOC - COOH + +8 MnO 2 + 8 KOH

Применение
При горении ацетилена в кислороде температура пламени достигает 3150 °C , поэтому ацетилен используют для резки и сварки металлов . Кроме того, ацетилен широко используется в органическом синтезе разнообразных веществ - например, уксусной кислоты,
1,1,2,2- тетрахлорэтана и др. Он является одним из исходных веществ при производстве синтетических каучуков, поливинилхлорида и других полимеров.

1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
CH 4 → C 2 H 2 → C 2 H 4 → C 2 H 5 Cl → C 2 H 4 → C 2 H 4 Cl 2
В уравнениях укажите структурные формулы органических веществ.
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
С 2 Н 6 → С 2 Н 4 → С 2 H 2 → C 2 Н 3 Сl → С 2 Н 5 Сl → С 2 Н 4
В уравнениях укажите структурные формулы органических веществ.

































