Просмотр содержимого документа
«Презентация по химии 8 класс "Типы химических реакций"»


Проверка знаний:
Знаки химических элементов.
- название
- произношение
- - название - произношение
Ba
Zn
Br
Pb
Cu
Al
Si
B
C
Hg
Au
O
Na
F
S
Cl
K
Ag
N
Ca
Fe
I
H

Кислород
Водород
Кальций
Сера
Азот
Алюминий
Цинк
Железо
Серебро
Натрий
Калий
Фосфор
Магний
Ртуть
Барий

H 2 O

5H 2 O

3 Fe 4H 2 O
5N 3N 2
6CO 2 7C
2O 3O 2
SO 2 Zn
4Ag 4H
3S 3H 2
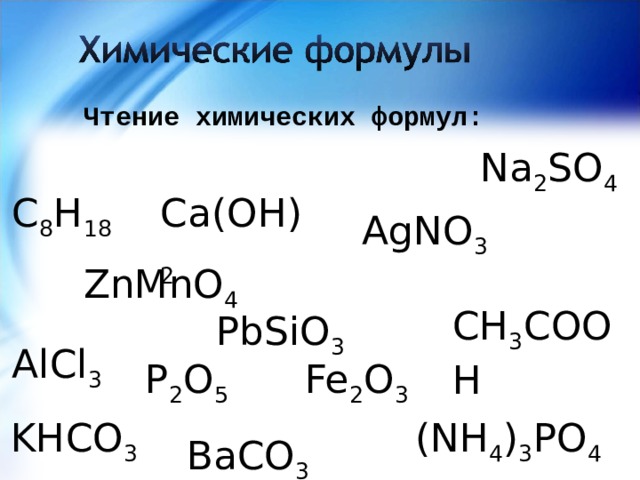
Чтение химических формул:
Na 2 SO 4
Ca(OH) 2
C 8 H 18
AgNO 3
ZnMnO 4
CH 3 COOH
PbSiO 3
AlCl 3
P 2 O 5
Fe 2 O 3
(NH 4 ) 3 PO 4
KHCO 3
BaCO 3

Типы химических реакций
Реакция замещения
Реакция соединения
Реакция разложения
Реакция обмена

Лабораторный опыт
« Прокаливание медной проволоки
в пламени спиртовки»
Cu + O 2 = 2CuO
1) Данная реакция протекает при нагревании.
2) Признаки реакции: изменение цвета.
3) Тип реакции: реакция соединения.
Реакция соединения

Реакция соединения-
реакция, в результате которой из двух или нескольких простых или сложных веществ образуется одно более сложное вещество.

Лабораторный опыт
« Взаимодействие цинка с соляной кислотой»
Zn + 2HCl = ZnCl 2 + H 2 ↑
1) Данная реакция протекает при соприкосновении веществ.
2) Признаки реакции: выделение газа
3) Тип реакции: реакция замещения.
Реакция замещения

Лабораторный опыт
« Взаимодействие мела (мрамора) с соляной кислотой»
1) Данная реакция протекает при соприкосновении веществ.
2) Признаки реакции: выделение газа.
3) Тип реакции: реакция обмена.
CaCO 3 + 2HCl = CaCl 2 + CO 2 ↑ + H 2 O
Реакция обмена

Реакция обмена-
реакция между двумя сложными веществами,
в результате которой
они обмениваются своими составными частями.

Реакция разложения-
реакция, в результате которой
из одного сложного вещества образуются два или несколько простых или сложных веществ.
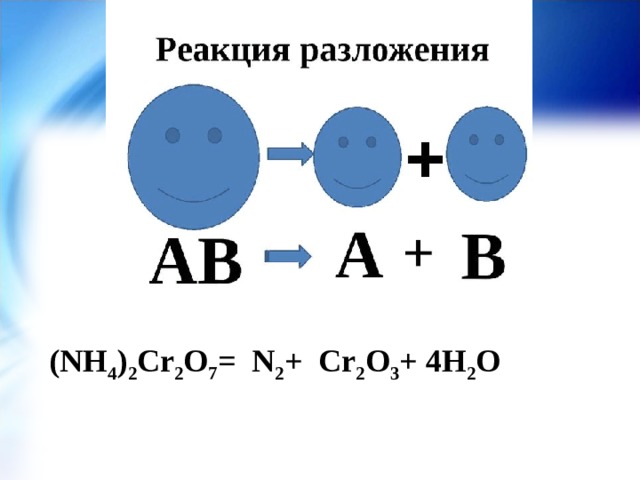
( NH 4 ) 2 Cr 2 O 7 = N 2 + Cr 2 O 3 + 4 H 2 O

Дописать уравнения химических реакций, расставить коэффициенты, определить тип химических реакций
Li+N 2 = …+…
Н 2 О = …+ О 2 ↑
BaCl 2 + Na 2 SO 4 = BaSO 4 ↓ + …
Al + Fe 2 O 3 = Al 2 O 3 + …

Взаимопроверка
6Li+N 2 = 2 Li 3 N – р.с.
2Н 2 О = 2 Н 2 ↑ + О 2 ↑- р.р.
BaCl 2 + Na 2 SO 4 = BaSO 4 ↓ +2 NaCl – р.о.
2Al + Fe 2 O 3 = Al 2 O 3 +2 Fe – р.з.

Домашнее задание
Подготовиться к практической работе №4 с. 207

Рефлексия
Оцените свою работу на уроке с позиции:
1. Я узнал (а) …
2. Мне было легко и понятно
(или сложно понять) …
3. Я научился (ась)…




































