Просмотр содержимого документа
«Презентация по химии : Химическая связь»

Химическая связь
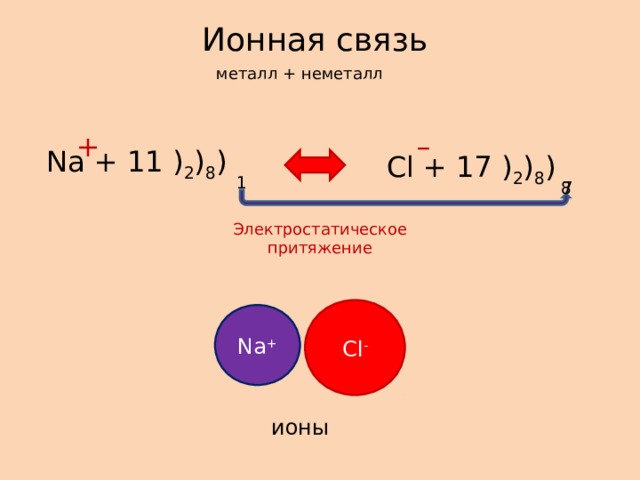
Ионная связь
металл + неметалл
+
–
Na + 11 ) 2 ) 8 )
Cl + 17 ) 2 ) 8 )
1
7
8
Электростатическое притяжение
Cl -
Na +
ионы

Свойства ионной связи
ненаправленная,
так как электромагнитное поле распространяется во все стороны
+
–
ненасыщаемая,
притянется столько ионов, сколько уместится
–
–
+
–

Поэтому все вещества с ионной связью имеют немолекулярное строение
Кристаллическая решетка
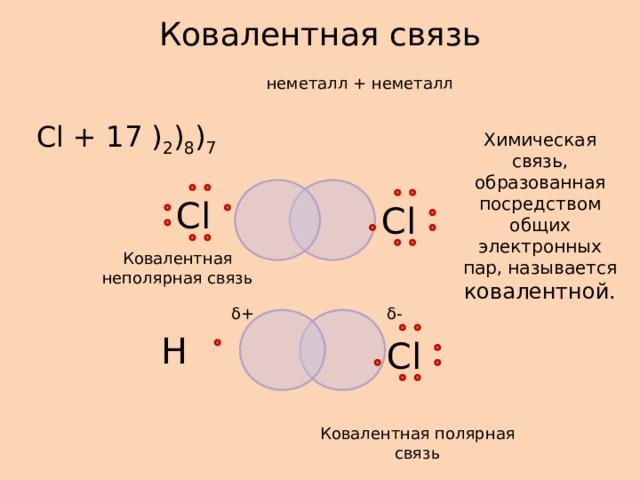
Ковалентная связь
неметалл + неметалл
Cl + 17 ) 2 ) 8 ) 7
Химическая связь, образованная посредством общих электронных пар, называется ковалентной.
С l
С l
Ковалентная неполярная связь
δ -
δ +
Н
С l
Ковалентная полярная связь

Ковалентная связь может быть образована несколькими парами электронов
N
N
N N
Количество связей у атома равно количеству электронов, которых не достает у атома до октета.

Свойства ковалентной связи
направленная,
атомы должны расположиться определенным образом.
104˚
Н
О
Н
насыщаемая,
связывает два атома,
«третий – лишний»
Н:Н
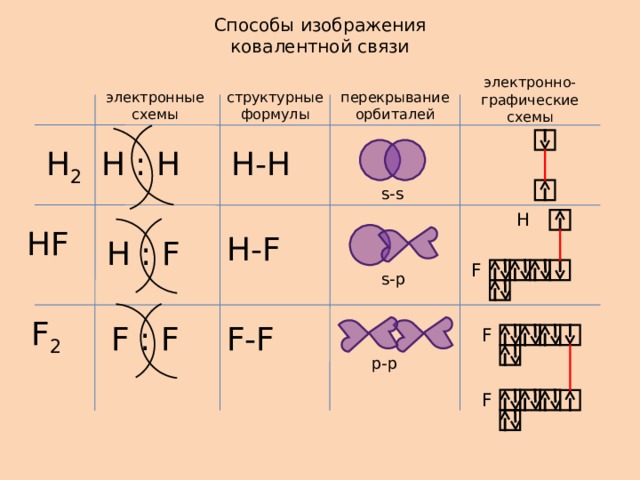
Способы изображения ковалентной связи
электронно-графические схемы
электронные схемы
перекрывание орбиталей
структурные формулы
Н -H
Н 2
Н : Н
s-s
H
Н F
Н -F
Н : F
F
s-p
F 2
F : F
F-F
F
p-p
F

ион-атомы
+
+
+
+
свободные электроны
+
+
+
+
+
+
+
+
+
+
+
+
Металлическая связь

Как определить вид связи в веществе?
Определите природу химических элементов
если
металл и неметалл
только металл
только неметаллы
связь ионная
связь металлическая
связь ковалентная
если
ЭО элементов одинакова
ЭО элементов различна
связь ковалентная полярная
связь ковалентная неполярная

Определите вид связи в следующих веществах:
Н 2 , Na, NaF, H 2 S, NH 3 , O 2 , Zn, CaS, Mg 3 N 2 , CH 4 , Al, F 2 .

Водородная связь – электростатическое притяжение между положительно поляризованным атомом водорода одной молекулы и отрицательно поляризованным атомом О, N или F другой молекулы (или другого фрагмента молекулы).
+
-
+
+
+
+
-
+
-
+
-
+
+
+
-
+
-
+





























