Просмотр содержимого документа
«Презентация по теме "МОНОСАХАРИДЫ"»
Моносахариды
Химия – 10
Автор: Кунова Г.В. учитель химии ЦДО г. Липецк

- Моносахариды – это гетерофункциональные соединения , так как в состав их молекул входит одна карбонильная группа и несколько гидроксильных групп.
- По числу углеродных атомов в молекуле моносахариды делятся на триозы, тетрозы, пентозы, гексозы.
- В природе наиболее распространены моносахариды, в молекулах которых содержится пять углеродных атомов (пентозы) или шесть (гексозы).

Глюкоза – строение молекулы
- Молекулярная формула глюкозы С 6 Н 12 О 6 .
О строении молекулы глюкозы можно судить на основании опытных данных:
- Глюкоза реагирует с карбоновыми кислотами , образуя сложные эфиры , содержащие от 1 до 5 остатков кислоты.
- Если раствор глюкозы прилить к свежеполученному гидроксиду меди (II), то осадок растворяется и образуется ярко-синий раствор соединения меди, т. е. происходит качественная реакция на многоатомные спирты .
- Вывод: глюкоза – многоатомный спирт.
Глюкоза – строение молекулы
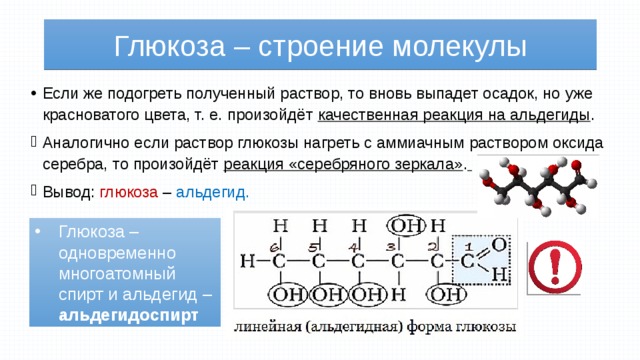
- Если же подогреть полученный раствор, то вновь выпадет осадок, но уже красноватого цвета, т. е. произойдёт качественная реакция на альдегиды .
- Аналогично если раствор глюкозы нагреть с аммиачным раствором оксида серебра, то произойдёт реакция «серебряного зеркала» .
- Вывод: глюкоза – альдегид.
- Глюкоза – одновременно многоатомный спирт и альдегид – альдегидоспирт
Глюкоза – строение молекулы
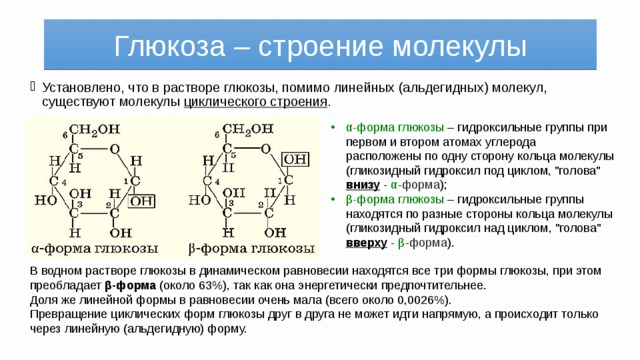
- Установлено, что в растворе глюкозы, помимо линейных (альдегидных) молекул, существуют молекулы циклического строения .
- α-форма глюкозы – гидроксильные группы при первом и втором атомах углерода расположены по одну сторону кольца молекулы (гликозидный гидроксил под циклом, "голова" внизу - α - форма );
- β-форма глюкозы – гидроксильные группы находятся по разные стороны кольца молекулы (гликозидный гидроксил над циклом, "голова" вверху - β - форма ).
В водном растворе глюкозы в динамическом равновесии находятся все три формы глюкозы, при этом преобладает β-форма (около 63%), так как она энергетически предпочтительнее.
Доля же линейной формы в равновесии очень мала (всего около 0,0026%).
Превращение циклических форм глюкозы друг в друга не может идти напрямую, а происходит только через линейную (альдегидную) форму.

Глюкоза – химические свойства
Реакции глюкозы как альдегида
- Окисление альдегидной группы.
Глюкоза способна окисляться в соответствующую (глюконовую) кислоту и давать качественные реакции альдегидов.
1) Реакция «серебряного зеркала»:
Глюкоза – химические свойства
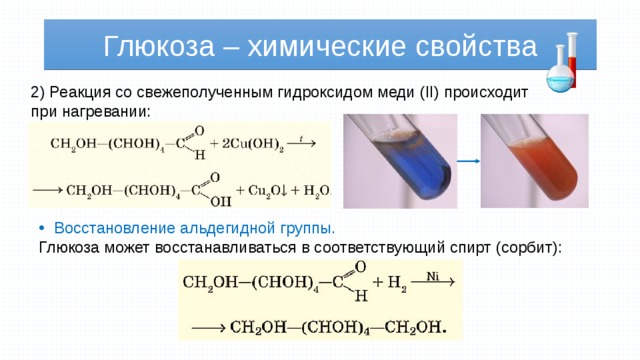
2) Реакция со свежеполученным гидроксидом меди (II) происходит при нагревании:
- Восстановление альдегидной группы.
Глюкоза может восстанавливаться в соответствующий спирт (сорбит):

Глюкоза – химические свойства
Как многоатомные спирты
- Глюкоза взаимодействует со свежеприготовленным гидроксидом меди (II) без нагревания, при этом образуется раствор ярко-синего цвета, а также с кислотами с образованием сложных эфиров.
+ глюкоза
- Реакция с гидроксидом меди (II) является качественной реакцией на глюкозу .

Глюкоза – химические свойства
Реакции брожения
- Эти реакции протекают под действием особых биологических катализаторов белковой природы – ферментов.
1) Спиртовое брожение
Оно издавна применялось человеком для получения этилового спирта и алкогольных напитков:
2) Молочнокислое брожение
Этот вид брожения составляет основу жизнедеятельности молочнокислых бактерий и происходит при скисании молока, квашении капусты и огурцов, силосовании зелёных кормов.

Применение глюкозы
- Глюкоза - основной источник энергии в живой клетке , поэтому она широко применяется в медицине при лечении самых различных заболеваний, особенно при общем истощении организма.
- Полученный восстановлением глюкозы сорбит используется при диабете в качестве заменителя сахара.

Применение глюкозы
- В микробиологической промышленности растворы глюкозы применяют как питательную среду для размножения кормовых дрожжей.

Применение глюкозы
- Спиртовым брожением глюкозы получают пищевой этиловый спирт.
- В кондитерской промышленности глюкоза в составе патоки используется при изготовлении мармелада, карамели, пряников и т. п.

Применение глюкозы
- Реакция «серебряного зеркала» глюкозы применяется при изготовлении зеркал и ёлочных украшений.
- В текстильной промышленности глюкоза используется для отделки тканей.

Фруктоза
- Наиболее важная из кетоз – D-фруктоза.
- Фруктоза широко распространена в растительном мире: содержится во фруктах, в пчелином мёде, входит в состав дисахарида сахарозы.

Фруктоза
Строение молекулы
- Фруктоза изомерна глюкозе и имеет молекулярную формулу
C 6 H 12 O 6
- Как и все моносахариды , фруктоза не подвергается гидролизу.
- Фруктоза (фруктовый сахар) – многоатомный кетоноспирт:
Она представляет собой кетогексозу с карбонильной группой у второго углеродного атома цепи.
1
2
3
6
4
5
Карбонильная группа
Фруктоза
Строение молекулы
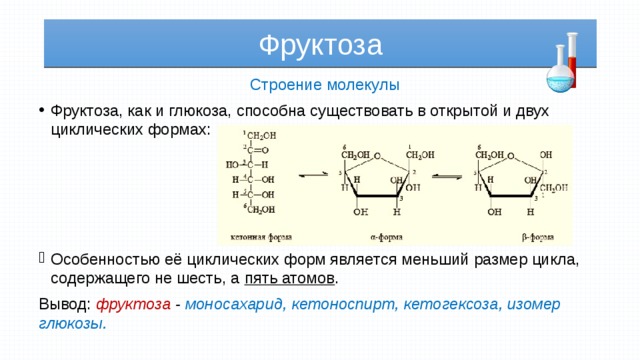
- Фруктоза, как и глюкоза, способна существовать в открытой и двух циклических формах:
- Особенностью её циклических форм является меньший размер цикла, содержащего не шесть, а пять атомов .
Вывод: фруктоза - моносахарид, кетоноспирт, кетогексоза, изомер глюкозы.

Фруктоза
Физические свойства
- По сравнению с глюкозой она имеет более сладкий вкус.
- Фруктоза, как и глюкоза, хорошо растворима в воде.
Химические свойства
- Фруктоза вступает во все реакции многоатомных спиртов :
образует сахараты с нерастворимыми в воде гидроксидами, простые и сложные эфиры.
Однако наличие в молекуле вместо альдегидной группы кетонного фрагмента затрудняет реакции окисления фруктозы.

Источники:
- Интернет-источники: фото и рисунки.



































