
Строение атома

Люди всегда задумывались о строении микромира, но на пороге новой эры так и не пришли к единой точке зрения.
Э. Резерфорд
Н. Бор
А. Беккерель

В 1879 году английский ученый Уильям Крукс открыл катодные лучи - поток быстролетящих отрицательно заряженных частиц, размеры которых были меньше самого маленького атома водорода, по вызываемой ими люминесценции. В 1891г. Д. Стонэй предложил назвать открытые частицы электронами.

В 1895г. немецкий ученый Уильям Конрад Рентген обнаружил новый вид излучения, обладающего большой проникающей способностью, и назвал их X - лучами. Таинственные лучи засвечивали фотопленку, завернутую в черную бумагу. Несколько позднее было установлено, что Х-лучи представляют собой электромагнитные колебания с очень малой длиной волны. В настоящее время рентгеновские лучи широко используются в различных областях науки и техники.
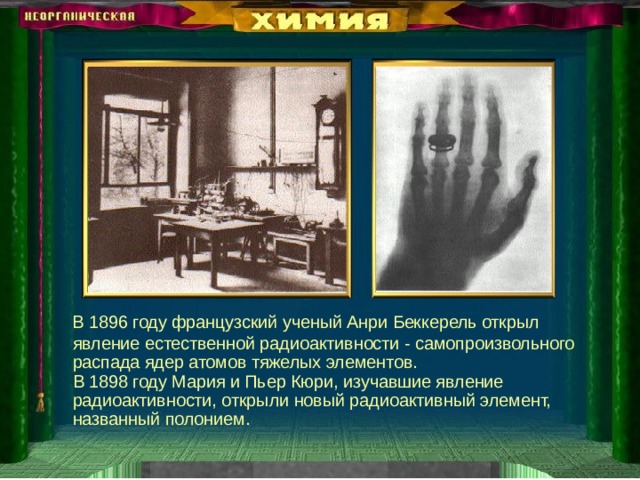
В 1896 году французский ученый Анри Беккерель открыл явление естественной радиоактивности - самопроизвольного распада ядер атомов тяжелых элементов. В 1898 году Мария и Пьер Кюри, изучавшие явление радиоактивности, открыли новый радиоактивный элемент, названный полонием.

Главным итогом совершенных открытий было, ясное осознание того, что атом не является мельчайшей частицей вещества, он имеет сложное строение. Было предложено несколько гипотез - моделей строения атома. Большинство из них основывалось на предположениях, что атом, оставаясь в целом электронейтральным, представляет собой совокупность положительно и отрицательно заряженных частиц.

Первой экспериментально обоснованной моделью строения атома была планетарная модель Эрнеста Резерфорда, создать которую ему помог специально проведенный опыт. Поток α - частиц, излучаемых радиоактивным источником через узкую щель направляется на тонкую золотую фольгу. Регистрация α - частиц проводилась при помощи флюоресцирующего экрана. В отсутствии фольги α - частицы двигались узким пучком, вызывая на экране яркую вспышку.

Когда на их пути помещали фольгу, то происходило в основном их слабое рассеивание. Однако, было обнаружено, что отдельные α - частицы могут отскакивать от фольги, вызывая свечение дополнительных экранов, помещенных в различных участках пространства до основного экрана.

Основываясь на модели Резерфорда можно было объяснить отдельные факты экспериментального поведения атомов. Однако для интерпретации других она была бессильна.
Было предложено еще несколько моделей строения атома, наиболее известными из которых являлись гипотеза Н.Бора и А.Зоммерфельда. Но ни одна из них не дала исчерпывающих объяснений имеющимся экспериментальным сведениям об атоме.

Состав ядра
Ядро - это центральная часть атома, в котором сосредоточена практически вся его масса. Ядро имеет положительный заряд, равный количеству протонов находящихся в нем. Кроме протонов в ядре также находятся нейтроны - частицы, имеющие массу, но не обладающие зарядом .

A r = m p+ + m n
Общее название протонов ( p + ) и нейтронов ( n 0 ) – нуклоны.
Нуклоны имеют следующие характеристики:
масса заряд
p + 1 +1
n 0 1 0
M асса атома складывается из суммы масс протонов и нейтронов .

Изотопы
Атомы одного элемента, имеющие одинаковое число протонов, но разное число нейтронов называются изотопами . Химические свойства таких атомов одинаковы, но они различны по некоторым физическим свойствам.
В 1961 году изотоп 12 С был выбран в качестве международного стандарта атомной массы

Состояние электрона в атоме
Вокруг ярда движутся электроны ( e - ) , образующие электронную оболочку, размеры которой определяют размеры самого атома.
Заряд e - по величине равен заряду p + , но противоположен по знаку.
 90 % , называют электронной орбиталью. " width="640"
90 % , называют электронной орбиталью. " width="640"
Состояние электрона в атоме
Для электрона, движущегося в атоме нельзя с достаточной точностью определить его координаты (то есть точку пространства в которой он находится) и направление его движения. Следствием этого факта является вероятностное описание движения электрона в атоме.
Область пространства, в которой вероятность нахождения электрона 90 % , называют электронной орбиталью.

Вопросы:
- Сколько протонов и нейтронов содержится в ядре атома лития? Каковы массовое и зарядовое числа для этого ядра?
- Какую частицу обозначают символом n? Сравните эту частицу (по массе и заряду) с протоном.
- Сколько протонов и нейтронов содержится в ядре атома кислорода? Каковы массовое и зарядовое числа для этого ядра?
- В ядре атома некоторого химического элемента содержится 13 протонов и 14 нейтронов. Чему равны массовое и зарядовое числа для этого ядра?
- Что называют изотопами?




















 90 % , называют электронной орбиталью. " width="640"
90 % , называют электронной орбиталью. " width="640"











