
МУНИЦИПАЛЬНОЕ БЮДЖЕТНОЕ ОБЩЕОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ОГОРОНСКАЯ СРЕДНЯЯ ОБЩЕОБРАЗОВАТЕЛЬНАЯ ШКОЛА
ЗЕЙСКОГО РАЙОНА АМУРСКОЙ ОБЛАСТИ
ДАМДИНОВА СОЕЛМА ЦЫБЕНОВНА – УЧИТЕЛЬ ХИМИИ
E-mail: damdinovasoelma@yandex.ru
Октябрь, 2021

«УЧЕБНАЯ ПРЕЗЕНТАЦИЯ ПО ТЕМЕ: УГЛЕРОД (9 КЛАСС)»

Этот химический элемент является основой живых организмов. Например, в теле человека массой 70 кг содержится около 13 кг! Это только в одном человеке! А также он содержится во всех растениях и животных. Из этого химического элемента состоят природный газ, нефть, уголь, торф, известняки и многие другие соединения.

ПЛАН ИЗУЧЕНИЯ ТЕМЫ:
1. Строение и свойства углерода по положению в ПСХЭ Д.И.Менделеева
2. Углерод – простое вещество. Аллотропия углерода.
3. Химические свойства углерода. Применение углерода.
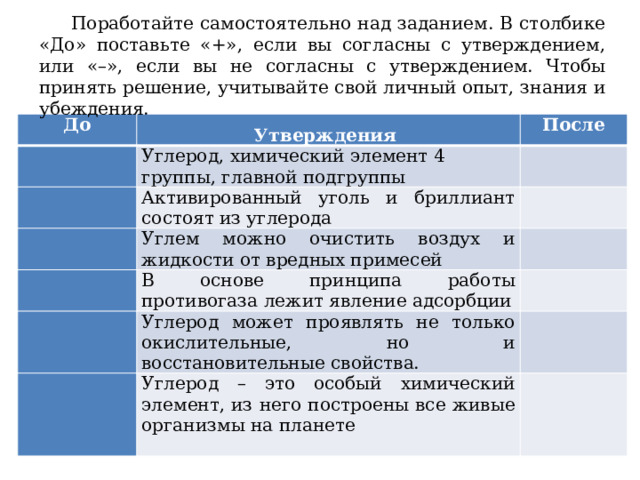
Поработайте самостоятельно над заданием. В столбике «До» поставьте «+», если вы согласны с утверждением, или «–», если вы не согласны с утверждением. Чтобы принять решение, учитывайте свой личный опыт, знания и убеждения.
До
Утверждения
После
Углерод, химический элемент 4 группы, главной подгруппы
Активированный уголь и бриллиант состоят из углерода
Углем можно очистить воздух и жидкости от вредных примесей
В основе принципа работы противогаза лежит явление адсорбции
Углерод может проявлять не только окислительные, но и восстановительные свойства.
Углерод – это особый химический элемент, из него построены все живые организмы на планете

Инструктаж по технике безопасности
1. Во время работы необходимо соблюдать чистоту, тишину, порядок и правила охраны труда, т. к. поспешность, неряшливость часто приводят к несчастным случаям. 2. Категорически запрещается в лаборатории принимать пищу, пить воду, пробовать вещества на вкус. 3. Сосуды с реактивами после употребления необходимо закрывать пробками и ставить на соответствующие места. 4. Нюхать вещества можно лишь осторожно, направляя на себя пары или газы легким движением руки, не наклоняясь к сосуду и не вдыхая полной грудью. 5. При проведении работы пользуйтесь только теми склянками, банками и т. п., на которых имеются четкие надписи на этикетках.
6. Во время нагревания веществ в пробирках и колбах нельзя направлять их отверстия на себя и соседей. Также, нельзя заглядывать в нагреваемые сосуды во избежание возможного поражения при выбросе горячей массы.
7.Необходимо знать месторасположение и уметь пользоваться средствами противопожарной защиты: песком, совком, огнетушителем.

РАБОТА В ГРУППАХ по изучению темы урока: Углерод
Задание для 1 группы
1.Дайте характеристику химическому элементу Углерод по положению в Периодической системе химических элементов Д.И.Менделеева
2.Исследуйте текст «Химическая история углерода» и подготовьте сообщение.
Задание для 2 группы
1.Пользуясь п.29 учебника и текстом с.164-166 опишите физические свойства алмаза и графита и заполните таблицу «Сравнение свойств алмаза и графита»
2. Составьте модели алмаза и графита
3. Лабораторный опыт: «Изучение свойств аморфного углерода»
«Обесцвечивание раствора перманганата калия, медного купороса древесным углём».
Ход работы:
В 2 воронки поместите слой ваты, растёртый карболен (таблетки активированного угля) смешанный с речным песком.
Воронки поставьте в стаканы.
В первую воронку налейте раствор перманганата калия, во вторую пробирку раствор сульфат меди.
Обратите внимание на изменение окраски раствора. Почему раствор обесцветился? Назовите свойство?
Делайте вывод:
восстановитель
окислитель
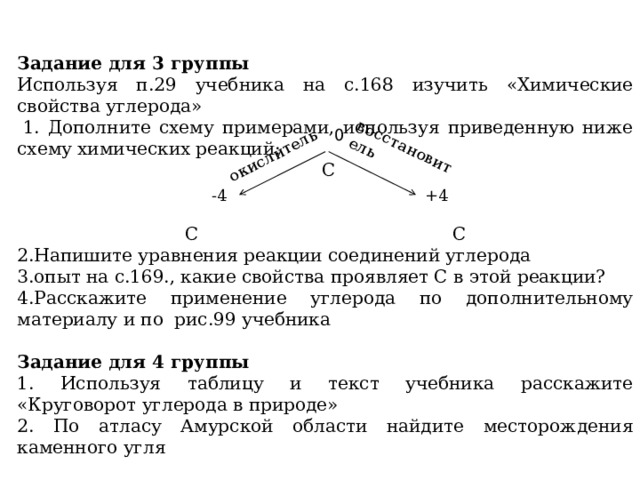
Задание для 3 группы
Используя п.29 учебника на с.168 изучить «Химические свойства углерода»
1. Дополните схему примерами, используя приведенную ниже схему химических реакций:
С
С С
2.Напишите уравнения реакции соединений углерода
3.опыт на с.169., какие свойства проявляет С в этой реакции?
4.Расскажите применение углерода по дополнительному материалу и по рис.99 учебника
Задание для 4 группы
1. Используя таблицу и текст учебника расскажите «Круговорот углерода в природе»
2. По атласу Амурской области найдите месторождения каменного угля
0
+4
-4

СХЕМА СТРОЕНИЯ АТОМА УГЛЕРОДА
«Химическая история углерода»
Углерод является одним из первых химических элементов, который известен человеку. С незапамятных времён человек использовал уголь и сажу. Когда наши предки овладели огнём, а это было около 100 тысяч лет назад, они имели дело с углём и сажей. По всей видимости, люди знакомы очень давно с разновидностями углерода, аллотропными модификациями - алмазом и графитом и каменным углем. Углерод является одним из элементов, имя первооткрывателя которого неизвестно, неизвестно и то, какая из форм элементарного углерода – алмаз или графит – была открыта раньше. И то и другое случилось слишком давно, ещё до возникновения письма.
Сам процесс горения, который является первым химическим процессом, который заинтересовавшим человека. Огонь давал тепло, свет, защищал от хищных животных. Но горение рассматривалось как процесс разложения вещества. Человек замечал, что если взять много топлива, то в результате горения остаётся зола, которой значительно меньше чем сжигаемое топливо. Уголь или углерод не считали элементом. Элементом для древнего человека был огонь. В конце XVIII, начале XIX веков зародилась теория флогистона, в которой говорилось о том, что в любом веществе имеется особое элементарное вещество-флогистон, который улетучивался в результате процесса горения. Небольшое количество золы, образовавшееся в результате горения, давало повод сторонникам данной теории предполагать, что уголь-это почти чистый флогистон. На поздних этапах развития теории флогистона, некоторые учёные стали предполагать, что уголь - есть элементарное вещество.
Впервые название углерод (carbone) в книге Гитона де Морво, Лавуазье, Бертоллеи Фуркруа "Метод химической номенклатуры" (1787) .
В 1791 г. английский химик Теннант первым получил свободный углерод; он пропускал пары фосфора над прокаленным мелом, в результате чего образовывался фосфат кальция и углерод. Международное название Carboneum происходит от лат. carbo (уголь). Слово это древнего происхождения. Со словом "carbo" связаны названия углерода и на других европейских языках (carbon, charbone и др.). Немецкое Kohlenstoff происходит от Kohle - уголь (старогерманское kolo, шведское kylla -- нагревать). Древнерусское угорати, или угарати (обжигать, опалять) имеет корень гар, или гор, с возможным переходом в гол; уголь по-древнерусски югъль, или угъль, того же происхождения. Слово алмаз (Diamante) происходит от древнегреческого - несокрушимый, непреклонный, твердый, а графит от греческого - пишу.
В начале XIX в. старое слово уголь в русской химической литературе иногда заменялось словом "углетвор" (Шерер, 1807; Севергин, 1815); с 1824 г. Соловьев ввел название углерод, которым мы сейчас и пользуемся.

УГЛЕРОД В ПРИРОДЕ
в свободном состоянии
в виде соединений
АЛМАЗ, ГРАФИТ
ПРИРОДНЫЙ ГАЗ, НЕФТЬ,
ГОРЮЧИЕ СЛАНЦЫ, КАРБОНАТНЫЕ МИНЕРАЛЫ,
ОРГАНИЧЕСКИЕ ВЕЩЕСТВА

УГЛЕРОД КАК ПРОСТОЕ ВЕЩЕСТВО.
АЛЛОТРОПНЫЕ МОДИФИКАЦИИ
САЖА
АЛМАЗ
ГРАФИТ
ДРЕВЕСНЫЙ УГОЛЬ
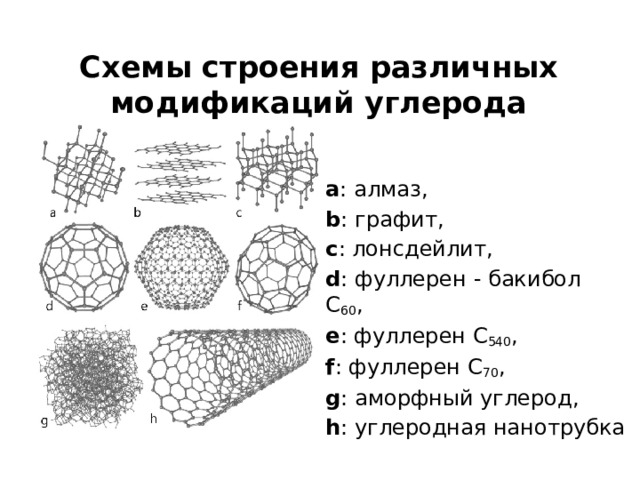
Схемы строения различных модификаций углерода
a : алмаз,
b : графит,
c : лонсдейлит,
d : фуллерен - бакибол C 60 ,
e : фуллерен C 540 ,
f : фуллерен C 70 ,
g : аморфный углерод,
h : углеродная нанотрубка

«Сравнение свойств алмаза и графита»
Признаки сравнения
Тип кристаллической решетки
Алмаз
атомный
Графит
Твердость
Атомно-слоистый
твердый
Прозрачность
Прозрачный минерал
Электропроводность
мягкий
Не имеет прозрачности
Не обладает электропроводностью
Блеск
Обладает электропроводностью
Цвет
Имеет больший показатель преломления
Прозрачный минерал, кристаллы могут быть любого цвета
Имеет металлический блеск
Имеет серый цвет
105 ПА, 1000 С
АЛМАЗ
ГРАФИТ
1010 ПА, 2000 С

ХИМИЧЕСКИЕ СВОЙСТВА УГЛЕРОДА
600-700С
С + О 2 = СО 2
(АЛМАЗ)
ВОССТАНОВИТЕЛЬНЫЕ СВОЙСТВА:
С + 2Н 2 SO 4 = CO 2 +2SO 2 + 2H 2 O
C + ZnO = CO +Zn
ОКИСЛИТЕЛЬНЫЕ СВОЙСТВА
4Al + 3C = Al 4 C 3
Si + C = SiC
C + 2H 2 = CH 4
+3
-4
0
t
0
+4
t
-4
+1
-4
t
ПРИМЕНЕНИЕ УГЛЕРОДА
ХИМИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
СТРОИТЕЛЬСТВО
МЕТАЛЛУРГИЧЕСКАЯ ПРОМЫШЛЕННОСТЬ
МАШИНОСТРОЕНИЕ
С (УГЛЕРОД)
ЮВЕЛИРНОЕ ДЕЛО
РАКЕТОСТРОЕНИЕ
МЕДИЦИНА
СМАЗКИ ДЛЯ ТЕХНИЧЕСКОГО ОБОРУДОВАНИЯ

Возвращаемся к заданию. В столбике «После» поставьте «+», если вы согласны с утверждением, или «–», если вы не согласны с утверждением, учитывая, знания, полученные на уроке.
До
Утверждения
Углерод, химический элемент 4 группы, главной подгруппы
После
Активированный уголь и бриллиант состоят из углерода
Углем можно очистить воздух и жидкости от вредных примесей
В основе принципа работы противогаза лежит явление адсорбции
Углерод может проявлять не только окислительные, но и восстановительные свойства.
Углерод – это особый химический элемент, из него построены все живые организмы на планете

СПИСОК ЛИТЕРАТУРНЫХ ИСТОЧНИКОВ:
- Химия.9 класс : учеб. для общеобразоват.организаций / О.С.Габриелян,
И.Г.Остроумов, С.А.Сладков. – М. : Просвещение, 2019
2. https://www.alto-lab.ru/elements/uglerod



































