Просмотр содержимого документа
«презентация к уроку»

муниципальное казенное общеобразовательное учреждение «Щученская средняя общеобразовательная школа» Лискинского района Воронежской области
Презентация
Урок химии в 11 классе
« Белки»
Подготовила Пащенко Галина Владимировна

1. Определение.
2 . Состав
3 . Структура
4 . Физические свойства
5 . Химические свойства
6 . Функции
7. Содержание в продуктах питания
8. Значение белков


углерод – 54 % ,
кислород – 23%,
азот – 17%,
водород – 6–7%,
а также сера, фосфор, магний, марганец.

Бесконечное разнообразие белков создаётся за счёт различного сочетания всего 20 аминокислот. Белок может состоять и из большего числа аминокислотных остатков, и кроме того, каждая аминокислота может встречаться в белке несколько раз. Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (– NH 2 ) с основными свойствами, другая – карбоксильной группой (– COOH) с кислотными свойствами. Часть молекулы, называемая радикалом ( R) , у разных аминокислот имеет различное строение.

Белки – амфотерные электролиты. При определённом значении pH среды (она называется изоэлектрической точкой) число положительных и отрицательных зарядов в молекуле белка одинаково. Это одно из основных свойств белка. Белки в этой точке электронейтральны, а их растворимость в воде наименьшая. Способность белков снижать растворимость при достижении электронейтральности их молекул используется для выделения их из растворов, например в технологии получения белковых продуктов.

1. Гидролиз
2. Денатурация (необратимое свёртывание белков)
3. Ренатурация (белок + спирт)

1. Горение с запахом жжёного пера.
2. Ксанопротеиновая (желтая):
белок + азотная кислота (конц.) = желтый цвет.
3. Биуретовая реакция: белок + щёлочь + раствор медного купороса = красно-фиолетовый цвет.










- Первичная структура
- Вторичная структура
- Третичная структура
- Четвертичная структура
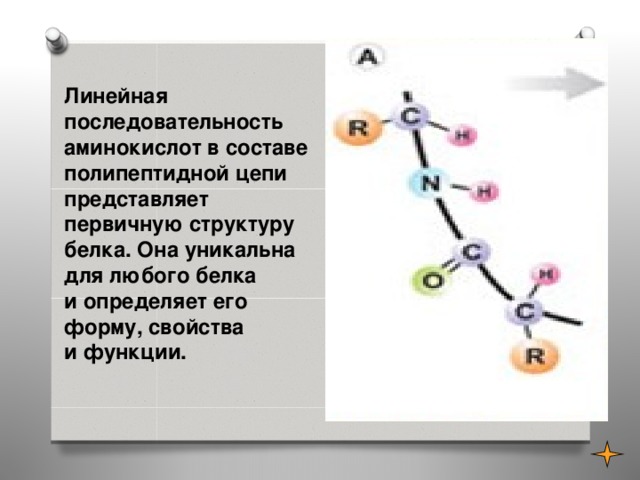
Линейная последовательность аминокислот в составе полипептидной цепи представляет первичную структуру белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
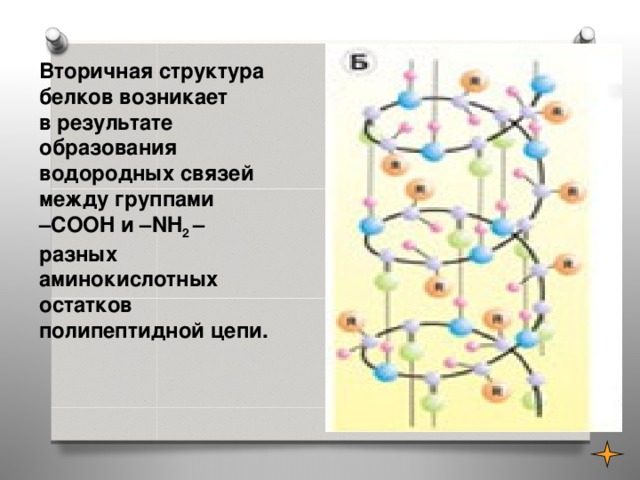
Вторичная структура белков возникает в результате образования водородных связей между группами –COOH и –NH 2 – разных аминокислотных остатков полипептидной цепи.
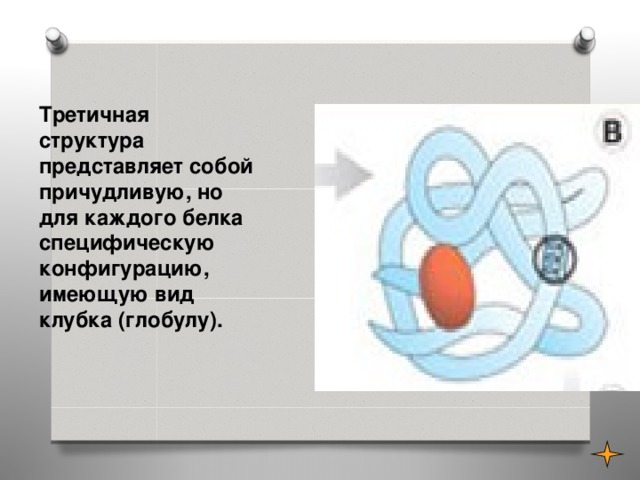
Третичная структура представляет собой причудливую, но для каждого белка специфическую конфигурацию, имеющую вид клубка (глобулу).
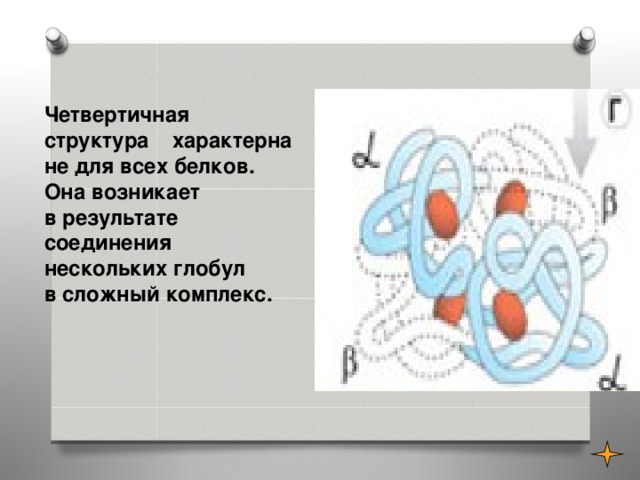
Четвертичная структура характерна не для всех белков. Она возникает в результате соединения нескольких глобул в сложный комплекс.

Название продукта
Содержание белка
Мясо
18–22%
Название продукта
Сыр
Рыба
Содержание белка
Горох
20–36%
17–20%
26%
Яйца
Картофель
Молоко
13%
1,5–2%
Ржаной хлеб
7,8%
3,5%
Яблоки
Рис
Пшено
8%
0,3–0,4%
Капуста
1,6%
10%
Морковь
Свекла
0,8–1%
Макароны
1,6%
9–13%
Гречневая крупа
11%


- В организмах животных и человека под влиянием ферментов ( пепсин, трипсин, эрипсин и т. д.) происходит гидролиз белков. В результате этого образуются аминокислоты, которые всасываются ворсинками кишечника в кровь. При этих процессах в организме выделяется энергия.

БЕЛКИ
Белки составляют примерно 20 % массы
человеческого тела и 50 % сухой массы клетки. В тканях человека белки не откладываются «про запас», поэтому
необходимо ежедневное их поступление с пищей.

Белки являются структурной и функциональной основой жизнедеятельности всех живых организмов, они обеспечивают рост, развитие и нормальное протекание обменных процессов в организме. Это мускулы, кровь, сердце, кожа, кости... В природе существует примерно 10 11 различных белков, обеспечивающих жизнедеятельность организмов всех степеней сложности, от вирусов до человека. Белками являются ферменты, антитела, многие гормоны и другие биологические активные вещества. Необходимость постоянного обновления белков лежит в основе обмена веществ

СПАСИБО ЗА ВНИМАНИЕ !














































