Просмотр содержимого документа
«презентация к уроку»

муниципальное казенное общеобразовательное учреждение «Щученская средняя общеобразовательная школа» Лискинского района Воронежской области
Презентация
Урок химии в 9 классе
« Галогены»
Подготовила Пащенко Галина Владимировна
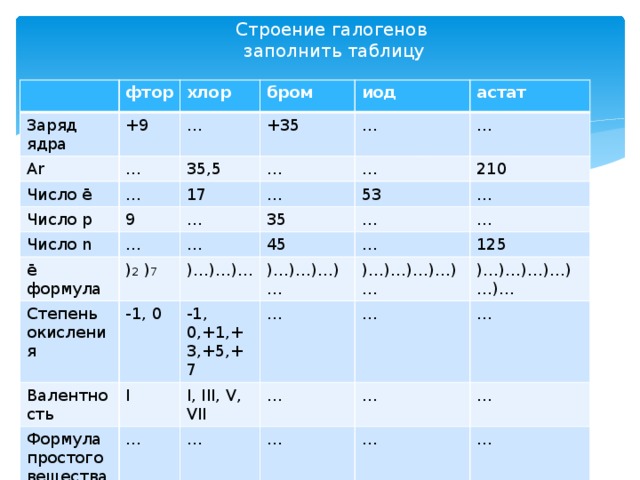
Строение галогенов заполнить таблицу
фтор
Заряд ядра
Аr
хлор
+9
Число ē
…
…
бром
+35
иод
35,5
…
Число p
17
астат
…
…
Число n
9
…
…
…
ē формула
…
…
210
53
35
Степень окисления
…
) 2 ) 7
…
45
)…)…)…
Валентность
…
-1, 0
Формула простого вещества
I
-1, 0,+1,+3,+5,+7
…
)…)…)…)…
…
…
125
I, III, V, VII
)…)…)…)…)…
…
)…)…)…)…)…)…
…
…
…
…
…
…
…
…
…

Физические свойства галогенов (работа по группам)
Фтор
Вид
Хлор
Агр. состояние
Цвет
Бром
Запах
Иод
Т. пл.
Т. кип.

Как переводится название группы «галогены»?
Рождающие соли
Галогены- сильные окислители.
Какие химические свойства проявляют галогены?

Взаимодействие с металлами
С медью: Cu + Г 2 = СuГ 2
С железом : Fe + … = …
C алюминием: … + … = …
Фтор
Медь
Хлор
Железо
Бром
Алюминий
Иод
Цинк
Взаимодействие с неметаллами
Водород
Фтор
Хлор
Бром
Иод

Взаимодействие со сложными веществами
Фтор
Вода
Фториды
Хлор
HF + O 2
Бром
-
Хлориды
-
Бромиды
-
-
Иод
Фториды + Cl 2
-
Фториды + Br 2
Иодиды
-
-
-
Хлориды +Br 2
-
Фториды + I 2
-
-
Хлориды + I 2
-
Бромиды + I 2
-

Какие свойства проявляют галогены в химических реакциях?
Окислительные
Металлические
Восстановительные
Окислительно- восстановительные
Все перечисленное
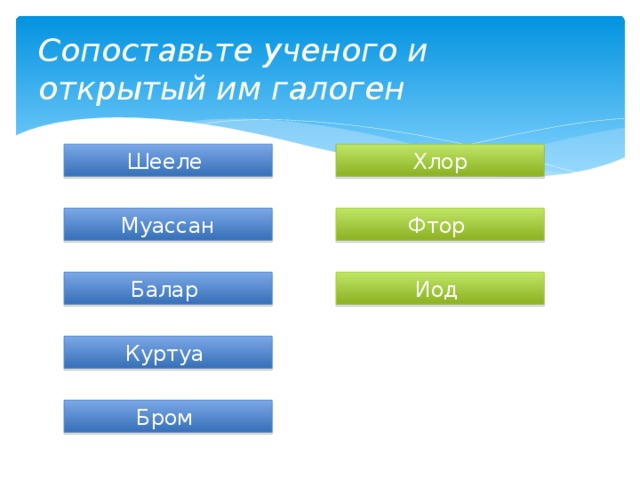
Сопоставьте ученого и открытый им галоген
Шееле
Хлор
Муассан
Фтор
Балар
Иод
Куртуа
Бром

Тест

Какова степень окисления галогена в KClO 4
+7
+5
+3
0
-1

Какова степень окисления галогена в HClO 3
+7
+5
+3
0
-1

Схема процесса окисления в реакции : H 2 + Сl 2 = 2HCl
Э 0 → Э -1
Э -1 → Э 0
Э 0 → Э +1
Э +1 → Э 0
Э 0 → Э +3

Схема процесса восстановления в реакции : 2HBr + Сl 2 = 2HCl +Br 2
Э +1 → Э 0
Э 0 → Э -1
Э 0 → Э +1
Э -1 → Э 0
Э 0 → Э +3
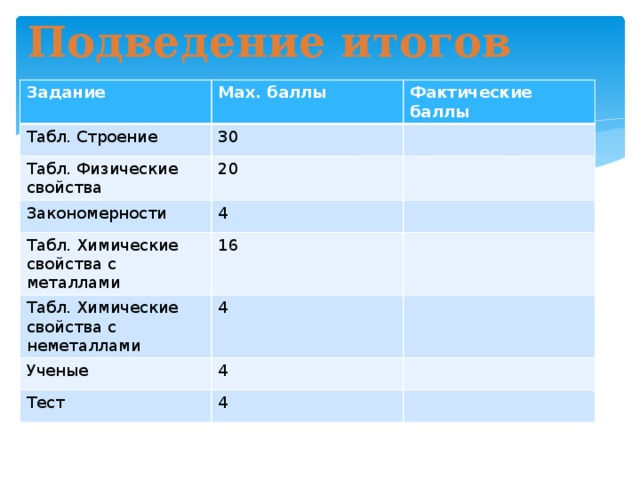
Подведение итогов
Задание
Мах. баллы
Табл. Строение
Фактические баллы
30
Табл. Физические свойства
20
Закономерности
4
Табл. Химические свойства с металлами
16
Табл. Химические свойства с неметаллами
4
Ученые
4
Тест
4

Оценивание
Количество баллов
Уровень
78- 82
Оценка
Высокий
70-77
Повышенный
5
55-69
4
Средний
0-54
Низкий
3
2

СПАСИБО ЗА РАБОТУ !

































