Просмотр содержимого документа
«презентация к уроку»

муниципальное казенное общеобразовательное учреждение «Щученская средняя общеобразовательная школа» Лискинского района Воронежской области
Презентация
Урок химии в 9 классе
«Железо»
Подготовила Пащенко Галина Владимировна

СЕГОДНЯ НА УРОКЕ: - ПОСМОТРИМ НА ЖЕЛЕЗО ГЛАЗАМИ ИСТОРИКА, ГЕОЛОГА, БИОЛОГА, ТЕХНОЛОГА, ЭКОЛОГА, ФИЗИКА, ПРАКТИКА, ХИМИКА; - ПРИЯТНО УДИВИМСЯ: ОКАЗЫВАЕТСЯ, ВЫ ЗНАЕТЕ УЖЕ ТАК МНОГО !

Визитка химического элемента

Охарактеризуйте железо как химический элемент
- Порядковый номер, номер периода , группа, подгруппа
- Порядковый № 26, 4 период , VIII группа, побочная подгруппа
- Заряд ядра, распределение электронов по уровням
- Заряд ядра +26, распределение é 2, 8, 14, 2
- Характерная степень окисления
- 0, +2, + 3

Физическая страница

Выберите правильные ответы:
- Самый тугоплавкий металл
- Температура плавления +1539 о С
- Проводит электрический ток
- Лёгкий металл
- Легко намагничивается и размагничивается
Запишите номера правильных ответов в тетрадь.

Историческая страница

каменный
век
медный
IV- III
век
бронзовый
тысячелетие
век
конец IV –
железный
начало I
до н.э.
век
I
тысячелетия
тысячелетие
до н.э.
до н.э.

Геологическая страница

Нахождение в природе
- В свободном виде в метеоритах
- В живых организмах
- В воде минеральных источников содержится сульфат и гидрокарбонат железа

Биологическая страница
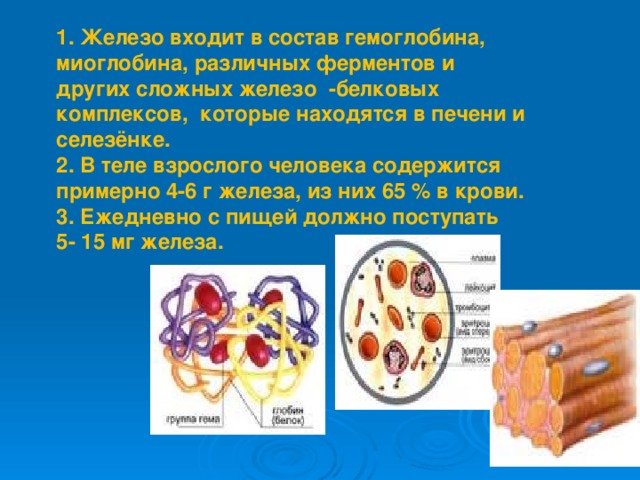
1. Железо входит в состав гемоглобина, миоглобина, различных ферментов и других сложных железо -белковых комплексов, которые находятся в печени и селезёнке.
2. В теле взрослого человека содержится примерно 4-6 г железа, из них 65 % в крови.
3. Ежедневно с пищей должно поступать 5- 15 мг железа.
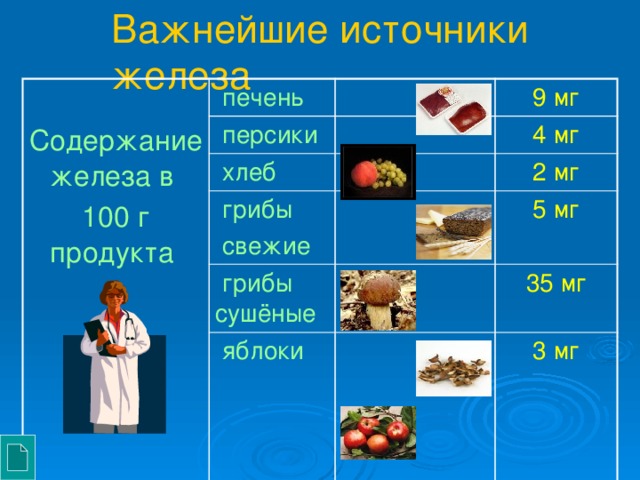
Важнейшие источники железа
Содержание железа в
печень
100 г продукта
персики
9 мг
хлеб
4 мг
грибы
2 мг
свежие
грибы сушёные
яблоки
5 мг
35 мг
3 мг

Технолого –экологическая страница
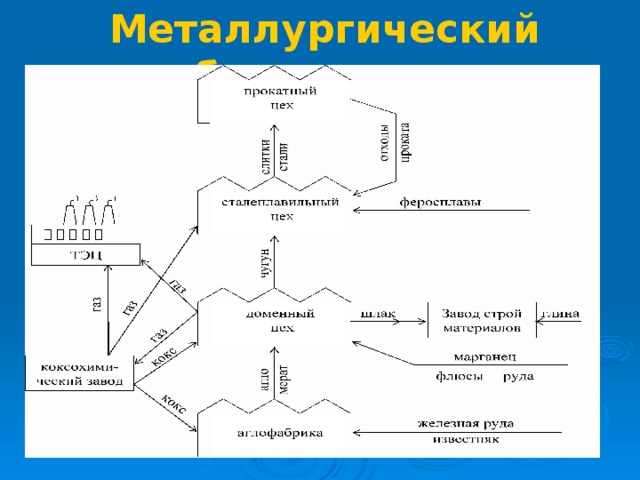
Металлургический комбинат

Загрязнение окружающей среды
- В черной металлургии выплавка чугуна и стали сопровождается образованием большого количества отходов: твердых(шлак, пыль), газообразных(дымовые газы), жидких(сточные воды).
- Из богатых железных руд на 1т чугуна образуется 1 т пустой породы, а из бедных руд – 2 т.

Практическая страница

- Железо - самый употребляемый металл, на него приходится до 90 % мирового производства металлов.
- Чистое железо способно быстро намагничиваться и размагничиваться, поэтому его применяют для изготовления трансформаторов, электромоторов и мембран микрофонов. Основная масса железа на практике используется в виде сплавов – чугуна и стали.

В царстве рыжего дьявола Ржа ест железо. Русская пословица

А.Е.Ферсман (1883г. -1945 г.) – автор «Занимательной минералогии» На поверхности железа под действием кислорода и воды образуется бурый слой ржавчины. Схему этого процесса условно записывают так: 4 Fe +3O 2 +6H 2 O = 4Fe(OH) 3

Химическая страница Расставьте коэффициенты методом электронного баланса
- Fe + S → Fe S
- Fe + O 2 → F 3 O 4
- Fe + Cl 2 → Fe Cl 3
![Лабораторный опыт №13, стр.209 «Качественные реакции на двух- и трехзарядные ионы железа» Оборудование: пробирки, штативы для пробирок. Реактивы: растворы веществ FeSO 4 , NaOH, K 3 [Fe(CN) 6 ], FeCl 3 , K 4 [Fe(CN) 6 ], KCNS. Строго соблюдайте правила техники безопасности!](https://fhd.multiurok.ru/8/4/a/84afb6441ca8b4f3ab1ea9f836da1c5e83a04f38/img21.jpg)
Лабораторный опыт №13, стр.209 «Качественные реакции на двух- и трехзарядные ионы железа»
- Оборудование: пробирки, штативы для пробирок.
- Реактивы: растворы веществ FeSO 4 , NaOH, K 3 [Fe(CN) 6 ], FeCl 3 , K 4 [Fe(CN) 6 ], KCNS.
Строго соблюдайте правила техники безопасности!

Рекомендации по проведению химического эксперимента Строго соблюдайте правила техники безопасности! Опыт №1. В одну пробирку налейте 2-3мл свежеприготовленного раствора соли железа (II), а в другую – столько же соли железа (III). В обе пробирки прилейте по 2-3мл раствора щелочи. Опыт №2. К раствору соли железа (III) прилейте раствор роданида калия.

В земной коре 5,1% железа, 2 место после алюминия
По запасам железных руд Россия занимает 1 место в мире:
- Магнитный железняк ( Fe 3 O 4 )-Урал
- Гематит (Fe 2 O 3 ) - Кривой Рог
- Лимонит (Fe 2 O 3 * n H 2 O) – Керчь, Курск, Кольский п-ов, Сибирь, Дальний Восток
- Пирит ( FeS 2 )- Урал
- Cидерит (FeCO 3 )

Природоохранные меры
- 2. Комплексное использование руд
- 3. Улавливание и использование газообразных выбросов
- 4. Переработка твердых отходов, их использование в качестве вторичного сырья

Способы защиты от коррозии?
скульптура «Рабочий и колхозница»
подземный трубопровод

Метеоритное железо

Плавка железа в Древнем Египте (воздух подаётся мехами, сшитыми из шкур животных)

Глиняные печи - горны

Ковка железа
Куй железо, пока горячо.
Русская пословица.

СПАСИБО ЗА ВНИМАНИЕ !




























![Лабораторный опыт №13, стр.209 «Качественные реакции на двух- и трехзарядные ионы железа» Оборудование: пробирки, штативы для пробирок. Реактивы: растворы веществ FeSO 4 , NaOH, K 3 [Fe(CN) 6 ], FeCl 3 , K 4 [Fe(CN) 6 ], KCNS. Строго соблюдайте правила техники безопасности!](https://fhd.multiurok.ru/8/4/a/84afb6441ca8b4f3ab1ea9f836da1c5e83a04f38/img21.jpg)



















