
Первый закон термодинамики
- это закон сохранения и превращения энергии в применении к тепловым процессам.

Внутренняя энергия тела может изменяться двумя способами:
1. При совершении механической работы
Совершая работу, можно добыть огонь, т. е. нагреть дерево до температуры, превышающей температуру его воспламенения.

В 1798 году Бенджамин Румфорд
(англо-американский учёный и изобретатель):
вода нагревается в процессе совершаемой
при сверлении работы.

В 1847 году Джеймс Джоуль
(английский физик, внесший значительный
вклад в становление термодинамики):
груз заставлял лопасти, погруженные в воду, вращаться, в результате чего вода нагревалась.
1 Дж механической работы ∼ 1 Дж количества теплоты
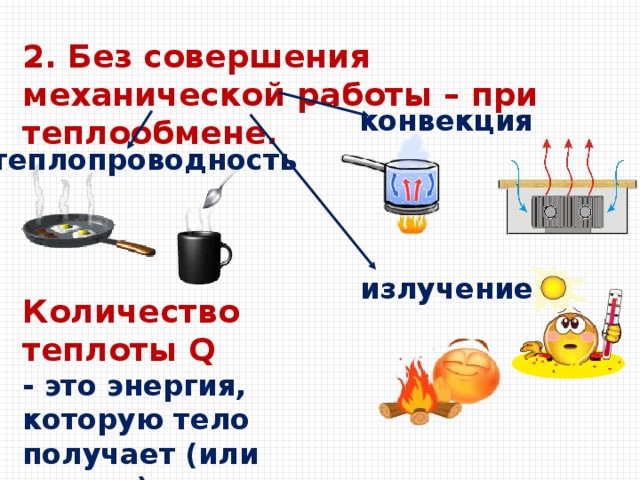
2. Без совершения механической работы – при теплообмене.
конвекция
теплопроводность
излучение
Количество теплоты Q
- это энергия, которую тело получает (или отдает)
при теплообмене.

Первый закон термодинамики
Изменение внутренней энергии ΔU системы
при переходе её из одного состояния в другое равно сумме работы внешних сил А и количества теплоты Q, переданного системе:
𝚫 U = A + Q

Вторая формулировка
первого закона термодинамики
Количество теплоты Q, полученное системой, идёт на изменение её внутренней энергии ΔU и на совершение системой работы над внешними телами:
Q = 𝚫 U + Aʹ
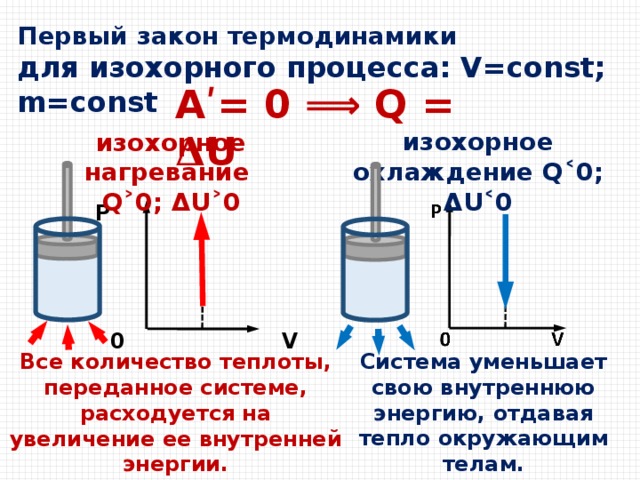
Первый закон термодинамики
для изохорного процесса: V=const; m=const
A ʹ = 0 ⟹ Q = 𝚫U
изохорное охлаждение Q ˂0; 𝝙 U˂0
изохорное нагревание
Q ˃0; 𝝙 U˃0
P
0 V
Система уменьшает свою внутреннюю энергию, отдавая тепло окружающим телам.
Все количество теплоты, переданное системе, расходуется на увеличение ее внутренней энергии.
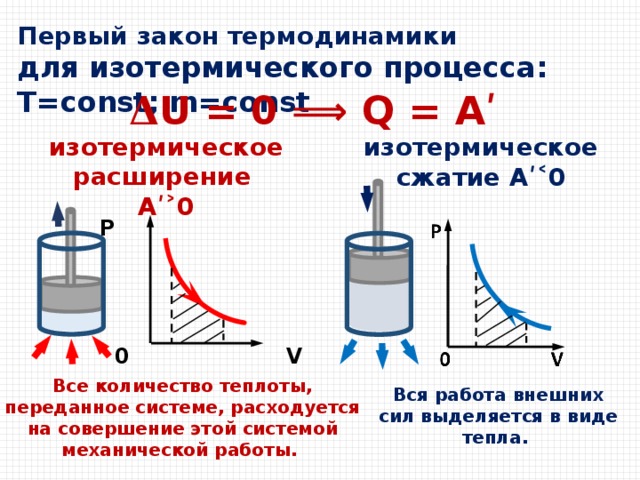
Первый закон термодинамики
для изотермического процесса: T=const; m=const
𝚫 U = 0 ⟹ Q = Аʹ
изотермическое расширение
Аʹ˃0
изотермическое сжатие Аʹ˂0
P
0 V
Все количество теплоты, переданное системе, расходуется на совершение этой системой механической работы.
Вся работа внешних сил выделяется в виде тепла.
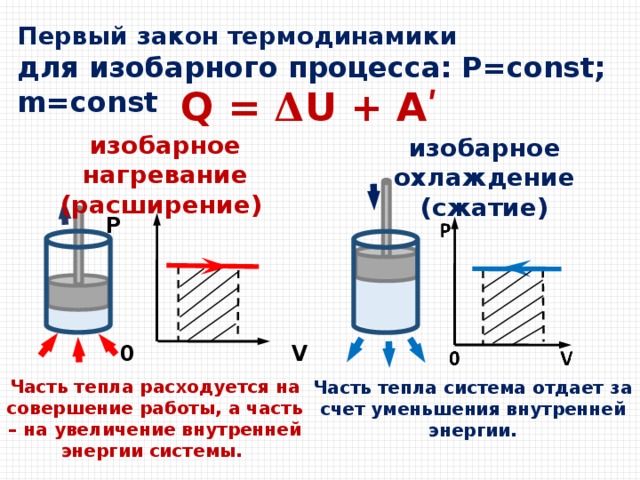
Первый закон термодинамики
для изобарного процесса: Р=const; m=const
Q = 𝚫U + Аʹ
изобарное нагревание (расширение)
изобарное охлаждение (сжатие)
P
0 V
Часть тепла расходуется на совершение работы, а часть – на увеличение внутренней энергии системы.
Часть тепла система отдает за счет уменьшения внутренней энергии.
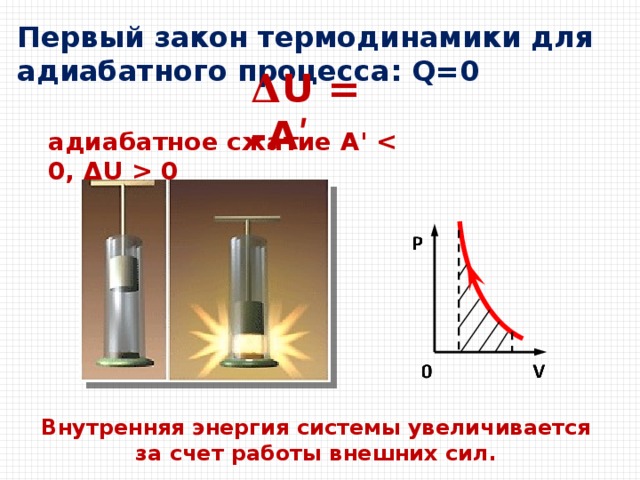
Первый закон термодинамики для адиабатного процесса: Q=0
𝚫 U = -Аʹ
адиабатное сжатие А' 0
Внутренняя энергия системы увеличивается
за счет работы внешних сил.
 0, ΔU Система совершает механическую работу только за счет уменьшения своей внутренней энергии. " width="640"
0, ΔU Система совершает механическую работу только за счет уменьшения своей внутренней энергии. " width="640"
Первый закон термодинамики для адиабатного процесса: Q=0
𝚫 U = -Аʹ
адиабатное расширение А' 0, ΔU
Система совершает механическую работу только за счет уменьшения своей внутренней энергии.
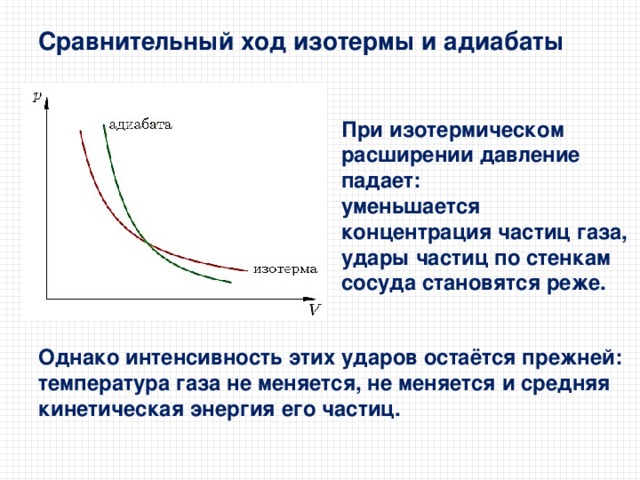
Сравнительный ход изотермы и адиабаты
При изотермическом расширении давление падает:
уменьшается концентрация частиц газа, удары частиц по стенкам сосуда становятся реже.
Однако интенсивность этих ударов остаётся прежней: температура газа не меняется, не меняется и средняя кинетическая энергия его частиц.
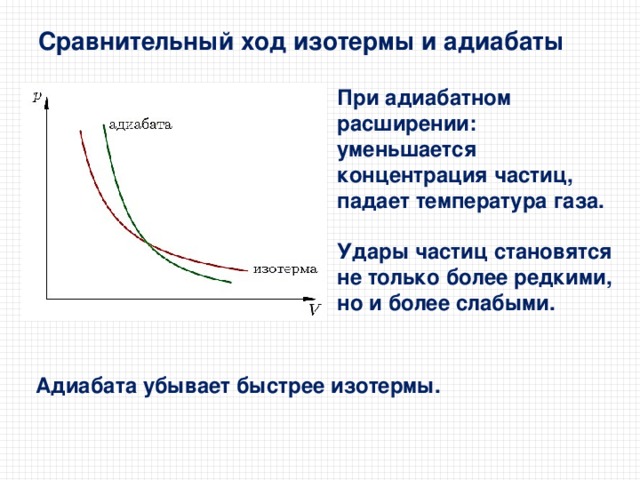
Сравнительный ход изотермы и адиабаты
При адиабатном расширении:
уменьшается концентрация частиц,
падает температура газа.
Удары частиц становятся не только более редкими, но и более слабыми.
Адиабата убывает быстрее изотермы.

Одним из главных процессов, приводящих к образованию облака, является процесс адиабатного расширения воздуха при его подъеме над поверхностью земли.
Нагретый воздух поднимается вверх и расширяется, так как атмосферное давление падает с увеличением высоты. Это расширение сопровождается значительным охлаждением. В результате водяные пары конденсируются и образуются облака.


















 0, ΔU Система совершает механическую работу только за счет уменьшения своей внутренней энергии. " width="640"
0, ΔU Система совершает механическую работу только за счет уменьшения своей внутренней энергии. " width="640"






















