МБОУТР СОШ №1 г. Торопца Тверской области
«Свойства щелочных металлов и их значение»
Скарлыгина Полина
ученица 10 класса
руководитель: Фомина Г.А
учитель химии высшей категории.
2015
Торопец
172840 Тверская обл. г.Торопец ул. Комсомольская, 4
тел.2-19-64
Содержание
1. Введение……………………………………………………………………..3 - 4
Методологические характеристики:
-актуальность темы
-гипотеза
-цель работы
-задачи
-объект исследования
-методы исследования
2. Основная часть…………………………………………………………….5 - 18
Вступление (актуальность темы, значение науки химии на современном уровне)
1)Общая характеристика щелочных металлов.
2) Д.И. Менделеев - о положении щелочных металлов в периодической системе элементов.
3)Химическое свойства металлов (взаимодействие с солями, водой)
а)Li и CuSO4
б)Li и CaCl2
в)Li и MgCl2
г) Li и Al2(SO)3
д) Li и FeCl3
3) Значение и применение щелочных металлов
3.Заключение………………………………………………………………..……19
4. Список литературы……………………………………………………..……..20
5. Приложение……………………………………………………..………..21 - 25
1.Введение.
Гипотеза:
основываясь на положении металлов в электрохимическом ряду напряжений Н.Н.Бекетова, что каждый металл, расположенный впереди должен вытеснять все последующие металлы из раствора солей. Но это не всегда так. Если учитывать, что активные металлы, реагируя с раствором соли, взаимодействуют с водой, а не с солью, образуя при этом совсем другие продукты реакции.
Цель:
экспериментально доказать отличие свойств щелочного металла от других металлов, при взаимодействии их с растворами солей и выявить роль воды, находящейся в растворах.
Задачи:
1)Углубить знания по химии щелочных металлов.
2)Приобрести навыки в исследовательской деятельности.
3) Подготовиться к экзаменам и расширить кругозор.
Объект исследования:
Щелочной металл литий и растворы солей.
Методы исследования:
1)Исследовательский метод.
2)Метод выдвижения и проверки гипотез.
Актуальность темы:
Современную жизнь невозможно представить без использования металла.
Литий - ионные аккумуляторы используются в мобильных телефонах, ноутбуках и фотоаппаратах, а наиболее мощные перспективны для электротранспорта и даже аэрокосмической отрасли.
Так как в заданиях ОГЭ, а именно в заданиях 6 и 11, и ЕГЭ могут встречаться взаимодействия щелочных металлов с растворами солей, то эта работа поможет нам разобраться в реакциях и не допустить ошибки.
Наука есть достояние общее, а потому справедливость требует не тому отдать наибольшую научную славу, кто первый высказал известную истину, а тому, кто сумел убедить в ней других, показал ее достоверность и сделал ее применимой в науке.
- Дмитрий Менделеев -
2.Основная часть.
I. Вступление.
О том, что химия важна и применяется людьми осознанно и неосознанно в самых разнообразных сферах, говорил еще великий ученый М. В. Ломоносов. Это было в 18 веке, сегодня же, когда технологии совершили огромный скачок вперед, невозможно представить жизнь человечества без этой сложной и многогранной науки.
По сути, химия окружает нас повсюду. Каждый день мы наблюдаем и осуществляем химические реакции, зачастую сами того не подозревая. Для этого не нужно вспоминать свой школьный курс химии, достаточно лишь внимательно посмотреть вокруг. Растворение сахара в чае может служить самым простым наглядным примером. Вокруг можно увидеть огромное количество предметов, созданных с помощью химии. Косметика и парфюмерия на женских туалетных столиках, пластик, резина, металлы и всевозможные полимеры, из которых изготовлены мебель и техника, таблетки и вакцины, используемые врачами и фармацевтами. Роль химии нельзя недооценить. Существует даже версия, что испытываемое людьми чувство любви есть ни что иное, как набор своеобразных химических реакций, протекающих в нашем организме. Химическая наука сейчас развивается семимильными шагами и к изучению ее стоит отнестись ответственно. Всевозможные открытия поощряются. Так Нобелевская премия по химии 2014 года присуждена Эрику Бетцигу (США), Уильяму Мернеру (США) и Штефану Хеллю (Германия) за развитие флуоресцентной микроскопии со сверхвысоким разрешением. Эти методы получили широкое распространение начиная с 2008 года, когда микроскопия сверхвысокого разрешения была признана «методом года» в специальном выпуске журнала Nature Methods. Суперфлуоресцентная микроскопия позволяет изучать строение разных объектов в очень малых масштабах и c рекордно высоким разрешением. С помощью этой методики можно, например, изучать структуру биологических молекул, что важно с точки зрения создания новых лекарств.
II.
1) Общая характеристика щелочных металлов.
Щелочны́е мета́ллы — это элементы 1-й группы периодической таблицы химических элементов. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щелочами.
В Периодической системе они располагаются в первой группе главной подгруппе, поэтому особенность строения атомов щелочных металлов заключается в том, что они содержат один электрон на внешнем энергетическом уровне: их электронная конфигурация ns1. Для всех щелочных металлов характерны восстановительные свойства. В большинстве соединений щелочные металлы присутствуют в виде однозарядных катионов. Однако существуют и соединения, где щелочные металлы представлены анионами.
Физические свойства щелочных металлов
Простые вещества, образованные этими элементами, — мягкие серебристо-белые металлы, легко режутся ножом. На свежем разрезе хорошо виден металлический блеск. Щелочные металлы характеризуются малой плотностью и низкими температурами плавления и кипения. Наименьшую плотность имеет литий (0,53 г/см3, т.е. почти в два раза легче воды), самую низкую температуру плавления — франций. В связи с высокой химической активностью эти металлы хранят под слоем керосина или минерального масла.
С целью формирования правильных представлений об отношении щелочных металлов к растворам различных солей мы проводили опыты с литием, так как они вполне безопасны при строгом выполнение обычных мер предосторожности, при работы со щелочными металлами. Литий реагирует с растворами солей достаточно энергично, но без воспламенения, выделяющегося водорода.
2)Д.И.Менделеев - о положении щелочных металлов в периодической системе элементов
Дмитрий Иванович Менделеев (1834 – 1907) – российский химик, разносторонний учёный, педагог. В 1869 году открыл периодический закон
химических элементов – один из основных законов естествознания.
По легенде, мысль о системе химических элементов пришла к Менделееву во сне, однако известно, что однажды на вопрос, как он открыл периодическую систему, учёный ответил: «Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
Сущность открытия Менделеева заключалась в том, что с ростом атомной массы химических элементов их свойства меняются не монотонно, а периодически. После определённого количества разных по свойствам элементов, расположенных по возрастанию атомного веса, свойства начинают повторяться. Например, натрий похож на калий, фтор похож на хлор, а золото похоже на серебро и медь. Разумеется, свойства не повторяются в точности, к ним добавляются и изменения.1
Предпосылки открытия периодического закона следует искать в книге Д.И. Менделеева «Основы химии». «Основы химии» Дмитрий Иванович начал писать в 1868 г. К этому времени было известно 63 химических элемента, описать которые и предстояло Менделееву. В 1868 г. Дмитрий Иванович успел написать всю 1-ую часть «Основы химии», состоящий из 2-х выпусков. Выпуск 1 был напечатан уже летом этого же года. В самом начале этого выпуска, т.е. в самом начале «Основы химии», Менделеев привёл список тех же 63 элементов, расположенных в той же алфавитной последовательности, но без атомных весов.
«Основы химии» делились на 2 части. В свою очередь каждая часть составлялась из 2-х выпусков. Выпуск 1-ый части 1-ой вышел в свет ещё летом 1868 г. Он был посвящен
главным образом общим вопросам химии, наряду с которыми Менделеев начал описание первых элементов, игравших роль типических; это были водород (Н), кислород (О) и азот (N), причём описание азота только было ещё начато в выпуске 1-ом. Очевидно, что выпуск 2 «Основы химии» должен был включить в себя, кроме описания азота ещё и углерод (С), т.е. последнего из 4-х типичных элементов. Кроме того, как показал набросок плана «Основы химии», в это выпуск Менделеев предполагал включить CL, Fe, Br, I и щелочные металлы, (впервые металлы I группы (Na и K) были получены английским химиком Х. Дэви в 1807г. электролизом щелочей, откуда и возникло их групповое название – щелочные металлы2). Следовательно, выпуск 2, а тем самым и всю 1-ую часть «Основы химии», Менделеев первоначально предполагал закончить щелочными металлами.
Дмитрий Иванович намечал описывать элементы и их соединения в следующем порядке:
NaCl(гл.20), CL, ClO, т.е. соединение CL с O(гл.21) и аналоги хлора – I, Br и F(гл.22). Сейчас же вслед за галоидами в плане у Менделеева шли Nа, K, Cs и Ag (последний был затем вычеркнут и перенесён во 2-ую часть «Основы химии»). 3
Набросок плана «Основы химии» Дмитрий Иванович сделал в середине 1868 г., а дальнейшие изменения в этом плане сделал несколько позднее, возможно во второй половине 1868 г. Согласно этому наброску плана в 1-ую часть «Основы химии» должны были войти, кроме 4-х органогенных элементов (H,O,N,C), ещё 4-е (CL, F, Br, I) и 5 щёлочных металлов (Na, Li, K, Rb, Cs), т.е. всего 13 элементов.
В таком случае во 2-ую часть следовало включить остальные 50 элементов. Однако, Менделеев решил перенести изложение материала о щелочных металлах во 2-ую часть «Основы химии», с тем чтобы 1-ую часть завершить галоидами, а во 2-ую часть начать с Na. Тем самым непосредственный переход от галоидов к щелочным металлам стал для Дмитрия Ивановича практическим вопросом о переходе от 1-ой части «Основы химии» ко 2-ой их части. Итак, Дмитрий Иванович к этому моменту уже изменил план разделения элементов между обеими частями «Основы химии». В 1-ой части осталось 8 элементов : органогены (H,О,N,С) и галоиды (Cl, Br, J); остальные 55 элементов приходились на 2-ую часть «Основы химии».
Первые главы 2-ой части «Основы химии» (вып.3) Дмитрий Иванович написал вначале 1869 г., как он сам об этом сообщил. Из этих глав 1-ая посвящается Na, 2-ая – его аналог, 3-ья – теплоёмкос-
ти, 4-ая – щелочноземельным металлам. За первые полтора месяца 1869 г. (до 15 февраля), Дмитрий Иванович смог написать только первые из этих глав, возможно, что главу 3-ью он дописал позднее. Ко дню открытия периодического закона (17 февраля), он вероятно,
успел уже изложить вопрос о соотношении таких полярно противоположных элементов, как щелочные металлы и галоиды, которые были сближены между собою по величине их атомности,
а так же вопрос о соотношении самих щелочных металлов по величине их атомных весов.
Переходя к главе 2-ой части 2-ой «Основы химии», посвященной аналогами Na Дмитрий Иванович сразу же начинает с сопоставлениями названные выше 2-х групп элементов. Дальше Дмитрий Иванович развивает ту же мысль, подчеркивая вместе с тем полярную противоположность в химических отношений обеих групп. Он пишет: «В качественном отношении галоиды, с одной стороны, и щелочные металлы с другой , суть элементов, наиболее
противоположные друг другу, и в ряду всех прочих элементов эту противоположность характеризуют чаще всего называя галоиды электроотрицательными, а щелочные металлы – электроположительными телами…»
При всем этом качественном различии есть, однако, важное количественное сходство между галоидами и щелочными металлами, Это сходство выражают, причисляя оба эти разряды элементов к числу одноатомных. Достаточно сравнить в этом отношении с водой КНО , К О, HclO и Cl O. Этим доказывается, что в количественном отношении галоиды и щелочные металлы сходственны с водородом.
Следовательно, в начале 1869 г., при написании первых глав 2 –ой части «Основы химии», Дмитрий Иванович был занят мыслью о проведении параллели между обоими упоминаемыми группами элементов, при одновременном подчеркивании их полярной противоположности : он обращает также свое внимание и на то обстоятельство, что величина атомных весов позволяет выяснить те отношения, которые существуют между элементами, входящими в одну естественную группу.
Для решающего шага к открытию периодического закона оставалось сопоставить и сблизить обе группы по величине атомных весов их членов.
Другой вопрос, который стал особенно интересовать Дмитрия Ивановича, как только он приступил к написанию 2-ой части «Основы химии», состоял в том, каким образом надо было располагать вслед за щелочными металлами остальные 50 элементов.4
2)Химическое свойства металлов (взаимодействие с растворами солей и водой)
а)Li и CuSO4
б)Li и CaCl2
в)Li и MgCl2
г) Li и Al2(SO4)3
д) Li и FeCl3
Каким образом будет происходить реакция между Li и раствором CuSO4?
Используя ряд Бекетова, возможно реакция пойдёт так, т.к литий стоит левее меди
2Li + CuSO4 = Cu + Li2SO4
a) экспериментально устанавливаем направление реакции, наблюдаем энергичное выделение газа. Подносим зажженную спичку к отверстию пробирки и по хлопку убеждаемся, что это Н2 . В верхней части образуется интенсивный черный осадок, постепенно распространяющийся по всему объёму раствора.
Li + CuSO4( р-ра) = H2 + осадок черного цвета.
Определим какое вещество выпало в осадок.
Нам известно только одно соединение Сu с черной окраской CuO – оксид меди (2)
Li + CuSO4( р-ра) = H2 + CuO
Но это неожиданно, назревает конфликтная ситуация, как же так? То есть, при этой ситуации новые факты и опыты вступают в противоречие с известными установленными представлениями (должен был получиться Сu – красного цвета + соль)
Чтобы разобраться с этим и выдвинуть правильную гипотезу, проделаем ряд дополнительных опытов: Li с другими солями.
а) 2Li + 2H2O = 2LiOH + H2 + Q
2LiOH + CaCl2 (р-ра) = Ca(OH)2↓ + 2LiCl
2Li + CaCl2 (р-ра) + 2H2O = Ca(OH)2↓ + 2LiCl + 2H2
б)2Li + 2H2O = 2LiOH + H2 + Q
2LiOH + MgCl2 = Mg(OH)2 ↓+ 2LiCl
Как и все слабые основания, гидроксид магния термически неустойчив. Разлагается при нагревании до 350 °C:
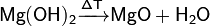
2Li + 2H2O + MgCl2 = MgO ↓+ H2O + 2LiCl + H2
в) 2Li + 2H2O = 2LiOH + H2 + Q
6LiOH + Al2(SO4)3 = 2Al(OH)3↓ + 3Li2SO4
При нагревании разлагается: 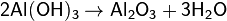
6Li + 2H2O + Al2(SO4)3 = Al2O3 ↓+ H2O + 3Li2SO4 + H2
г)2Li + 2H2O = 2LiOH + H2 + Q
3LiOH + FeCl3 = Fe(OH)3↓ + 3LiCl
Разлагается при нагревании:
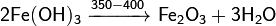
6Li + 2H2O + 2FeCl3 = Fe2O3 ↓+ H2O + 6LiCl + H2
Наблюдаем происходящие явления и анализируем
А)Во всех пробирках выделяется Н2
Б)Выпадают осадки гидроксидов соответствующих металлов.
Эти опыты наглядно убедили нас в том, что при действии активного щелочного металла на растворы солей не происходит вытеснение менее активного металла, так как мы предполагали ранее, а образуется нерастворимые гидроксиды. А так как щелочные металлы активно взаимодействуют с Н2О, образуя щелочь + Н2 , реакция +Q – экзотермичная. Тогда уравнение реакции выглядит так:
2Li + 2H2O = 2LiOH + H2 + Q
В этой же пробирке щелочь начинает реагировать с растворами солей и получается нерастворимое в воде основание.
2LiOH + MgCl2 = Mg(OH)2 ↓ + 2LiCl
Суммарное уравнение реакции выглядит так:
2Li + 2H2O + MgCl2 = Mg(OH)2 ↓ + 2LiCl + H2
Аналогично объясняем и другие опыты.
После первой реакции экспериментальные данные позволяют объяснить проблему, возникшую при выполнение первого опыта (CuO – оксид меди 2)
Вывод: мы установили, что при взаимодействие щелочных металлов с растворами солей реакция идет преимущественно в направление образования нерастворимого основания. Мы решили данную проблему по частям, что дало нам лучше осознать и найти правильный путь к решению.
Тогда возникает следующий вопрос: почему в результате первого опыта образуется не голубой осадок Cu(ОН)2, а чёрный осадок CuО.
Выдвигаем гипотезу: очевидно, Cu(OH)2, который первоначально должен образоваться (Li + соль), но в ходе опыта сразу разлагается на CuO + H2O за счет выделения теплоты, при взаимодействие Li с H2O. Чтобы подтвердить эту гипотезу нужна дополнительная информация о разложении при нагревании.
По справочнику:
Гидроксид меди(II) — Cu(ОН)2, голубое аморфное или кристаллическое вещество с ромбической кристаллической решеткой. Cu(ОН)2 практически не растворим в воде. При нагревании до 70-90 °C порошка Cu(ОН)2 или его водных суспензий разлагается до CuО и Н2О.
Оказалось, что температура разложения 500
Cu(OH)2 = CuO + H2O
Повторяем этот опыт и измеряем в конце опыта температуру в конце части пробирки (около 700), что вполне достаточно для разложения Cu(OH)2
Обобщение:
Установив все особенности опытов, проверив гипотезу и свои аргументы, мы смогли дать объяснение необычной демонстрации и составить уравнения всех протекающий в растворах реакций.
2Li + 2H2O = 2LiOH + H2 + Q
2LiOH + CuSO4( р-ра) = Cu(OH)2 ↓+ Li2SO4
Cu(OH)2 = CuO + H2O
2Li + 2H2O + CuSO4 ( р-ра) = CuO ↓+ H2O + Li2SO4 + H2
Можно проверить найденное решение проблемы.
Опыт 3
Получить реакцию обмена между раствором соли Cu и растворам щелочи NaOH и добавить в пробирки Li, через
некоторое время голубой осадок Cu(OH)2 , превращается в черный CuO – оксид меди 2.
Что нам это дало?
1.Эти опыты дают возможность ученикам активно оперировать знаниями, прогнозировать преимущественное направление некоторых химический реакций.
2.В методическом отношении они полезны для предотвращения некоторых распространенных ошибок в знаниях учеников и при подготовке к ОГЭ/ЕГЭ по химии.
3)Значение и применение щелочных металлов
Литий – очень лёгкий, мягкий, блестящий щелочной металл. Ионы лития окрашивают пламя в розовый цвет. Его температура плавления -180 гр; температура кипения -1340 гр; плотность -0,524 г/cм3. Литий – очень активный металл, сильный восстановитель. Даже при комнатной температуре литий быстро реагирует с азотом воздуха, покрываясь слоем нитрида:
6Li + N2 = 2Li3N.
Литий относительно спокойно реагирует с водой, так же литий реагирует с кислотами, серой, аммиаком, углекислым газом, кремнием и др. В кислоте и на воздухе литий горит, подобно магнию, ослепительно белым пламенем, продукты горения раздражают дыхательные пути:
4Li + O2 = 2Li2O
Из металлического лития делают кадоты литиевых элементов питания. Металл можно извлечь из кнопочных и пальчиковых литиевых батареек. В них электроны сделаны из длинной ленты, для компактности скрученной в рулон. Сразу же после извлечения литий переплавляется под слоем осушенного машинного масла для получения компактного слитка и удаления окислов. Далее литий можно хранить в этом же масле или других инертных жидкостях в герметичной посуде. Металлический литий приобрел большое техническое значение. Его используют во все возрастающих количествах в сплавах, так как небольшие добавки этого металла существенно улучшают свойства многих сплавов. Преимущественно литий (и наряду с натрием и кальцием) применяют для свинцово-подшипниковых сплавов и при производстве склерона. Кроме того, он служит в качестве раскисляющего средства для меди и при рафинировании содержащего никеля.
Металлический натрий, с тех пор как его изготовление стало дешевым, находит широкое техническое применение. Его используют в качестве исходного продукта при производстве перекиси натрия (моющее средство), а также амида натрия и натрийцианамида. Его используют также в больших количествах в органических синтезах (например, в красильном производстве). В осветительной технике его применяют в натриевых газоразрядных лампах. В лабораториях натрий используют в качестве восстановителя. Металлический калий также иногда употребляют в лаборатории. Кроме того, калий и прежде всего цезий применяют в фотоэлементах. Помимо этого, рубидий и цезий в свободном состоянии мало применяются.
Перекись натрия в больших количествах используется при производстве моющих средств. В лаборатории ее применяют как энергичный окислитель в водном растворе и в расплаве. Гидроксиды калия и натрия в технике и в лаборатории часто применяют в качестве сильных оснований. Вследствие небольшой гигроскопичности оксида и гидроксида лития, их используют для приготовления фотографических проявителей в виде порошков. Соли щелочных металлов натрия и калия также имеют широкое применение. Если требуется ввести в реакцию какой-либо кислотный остаток, то его применяют большей частью в виде соответствующей соли щелочного металла (натрия или калия). Такое предпочтение для реакций щелочных солей объясняется их легкой плавкостью и растворимостью, а также и тем, что они не вызывают нежелательных побочных реакций. Однако, для технических целей, могут использовать и другие соединения, если они являются дешевле. Некоторые соли лития, например салицилат, карбонат и цитрат принимают как лечебное средство от подагры. Минеральные воды, употребляемые для борьбы с этой болезнью, в качестве действующей составной части содержат соли лития.
3. Заключение
Мы смогли углубить знания по химии металлов, нашли исторические факты о размещение металлов в периодической системе химических элементов Д.И.Менделеева. Установив все особенности опытов щелочных металлов, проверив гипотезу и свои аргументы, мы смогли дать объяснение необычной демонстрации и составить уравнения всех протекающих в растворах реакций. Мы осуществили реакции взаимодействия лития с солями и водой. Эти демонстрации помогли убедиться в том, что щелочные металлы не вытесняют другие, менее активные металлы из растворов солей, а образует нерастворимые гидроксиды. Эти реакции экзотермичны и сопровождаются выделением большого количества теплоты, процесс протекает сложно, и важная роль в этом процессе принадлежит взаимодействию щелочного металла с водой, что приводит к образованию щелочей, которые и реагируют с раствором соли.
4. Список литературы:
1. Агофошин Н.П «Периодический закон и периодическая система Д.И.
Менделеева» Пособие для учащихся. — М.: Просвещение, 1982. 31-33 стр.
2.«Биография великих химиков» Кари Хойниг.
3. Кедров Б.М 2001 г. 20-25 стр «День одного великого открытия».
4. «Энциклопедический словарь юного химика» 2 – е изд., Педагогика, 1990
5. ХИМИЯ ( учебно – методический журнал для учителей химии и естествознания №3)
6. Электронная энциклопедия – Википедия.
7. Электронная страница:
http://talkio.ru/goloe97stoemy/%D0%A2%D0%B0%D0%B1%D0%BB%D0%B8%D1%86%D0%B0_%D0%9C%D0%B5%D0%BD%D0%B4%D0%B5%D0%BB%D0%B5%D0%B5%D0%B2%D0%B0#.D0.98.D1.81.D1.82.D0.BE.D1.80.D0.B8.D1.8F_.D0.BE.D1.82.D0.BA.D1.80.D1.8B.D1.82.D0.B8.D1.8F
8. Электронная страница:
http://www.ronl.ru/referaty/elementi_periodicheskoj_sistemi_mendeleeva/17057/
9. Электронная страница:
http://khimie.ru/himiya-elementov/svoystva-shhelochnyih-metallov
5. Приложение














1� http://talkio.ru/goloe97stoemy/%D0%A2%D0%B0%D0%B1%D0%BB%D0%B8%D1%86%D0%B0_%D0%9C%D0%B5%D0%BD%D0%B4%D0%B5%D0%BB%D0%B5%D0%B5%D0%B2%D0%B0#.D0.98.D1.81.D1.82.D0.BE.D1.80.D0.B8.D1.8F_.D0.BE.D1.82.D0.BA.D1.80.D1.8B.D1.82.D0.B8.D1.8F
2� http://www.ronl.ru/referaty/elementi_periodicheskoj_sistemi_mendeleeva/17057/
3� Агофошин Н.П «Периодический закон и периодическая система Д.И.Менделеева» Пособие для учащихся. — М.: Просвещение, 1982. 31-33 стр.
4� «День одного великого открытия» Кедров Б.М 2001 г. 20-25 стр.