Просмотр содержимого документа
«Презентация по теме "Аммиак"»

Девиз урока:
«Скажи мне, и я забуду, покажи мне, и я запомню, вовлеки меня, и я научусь»
Китайская пословица

Из истории…
Посредине ливийской пустыни стоял храм, посвященный богу Амон Ра. В древности арабские алхимики получали из оазиса Амон, находившегося около храма, бесцветные кристаллы. Его растирали в ступках, нагревали – и получали едкий газ. . .
Храм Амон Ра
- Затем его именовали «аммониак», а потом сократили название до «аммиак».
Они звали вещество «нушадир»
В средние века этот газ называли почему-то «щелочной воздух», а его раствор и поныне называется «нашатырный спирт».
Бог Амон в образе барана

Тема урока
Аммиак

Из истории…
- Аммиак NH 3 – это самое важное из водородных соединений азота.
- В чистом виде аммиак впервые был собран в конце XVIII в. англичанином Дж. Пристли.
- Однако, несмотря на то, что ученый смог описать свойства аммиака, ему не удалось определить состав соединения из-за несовершенства существовавших в то время экспериментальных методик.
- Заслуга в этом принадлежит К. Л. Бертолле. Он разложил аммиак действием электрической искры и получил точные данные о его количественном составе.
Джозеф Пристли.
Клод Луи Бертолле

- Состав и строение молекулы аммиака.
- Физические свойства аммиака.
- Способы получения аммиака
- Химические свойства аммиака.
- Применение аммиака
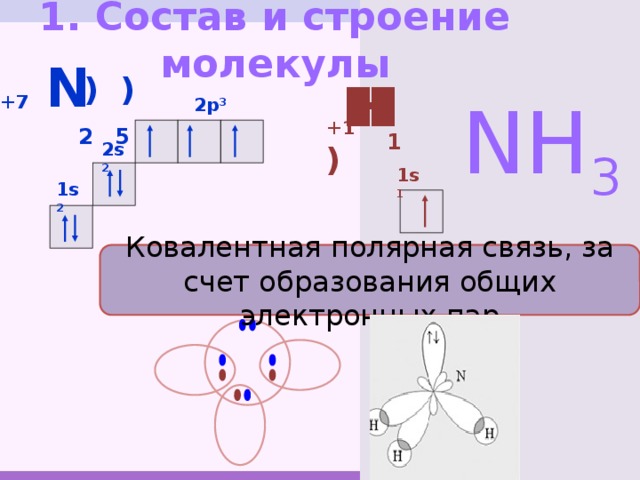
1. Состав и строение молекулы
N
+7 ) )
2 5
H
H
H
+1 H )
NH 3
2p 3
1
2s 2
1s 1
1s 2
Ковалентная полярная связь, за счет образования общих электронных пар
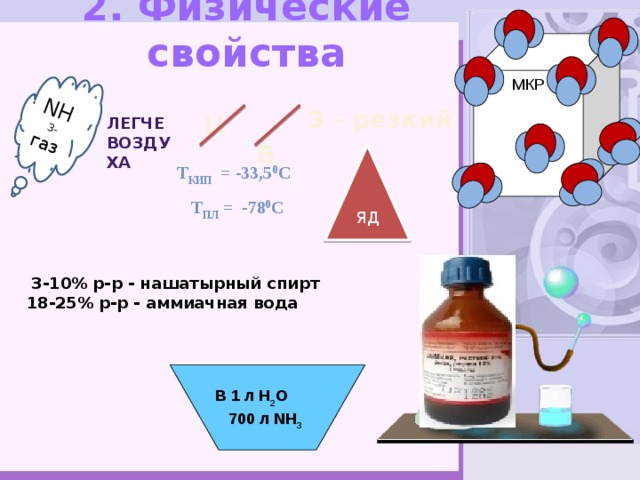
2. Физические свойства
NH 3-
газ
МКР
З - резкий
Ц
В
легче воздуха
Т кип = -33,5 0 С
ЯД
Т пл = -78 0 С
3-10% р-р - нашатырный спирт
18-25% р-р - аммиачная вода
В 1 л Н 2 О 700 л NH 3

3. ПОЛУЧЕНИЕ АММИАКА
А) в промышленности
Способ основан на прямом взаимодествии водорода и азота.
кат.
N 2 (г) + 3H 2 (г) ↔ 2NH 3 (г) + 45,9 кДж
Характеристика реакции:
1 - это реакция по типу вступающих и образующихся веществ - ?
2 – по тепловому эффекту
3- по изменению степени окисления
4- по обратимости
5- по наличию веществ, ускоряющих реакцию
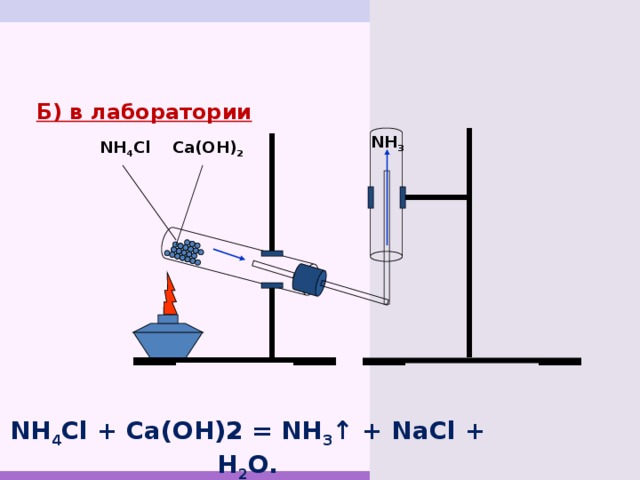
Б) в лаборатории
NH 3
Ca(OH) 2
NH 4 Cl
NH 4 Cl + Ca(OH)2 = NH 3 ↑ + NaCl + H 2 O.
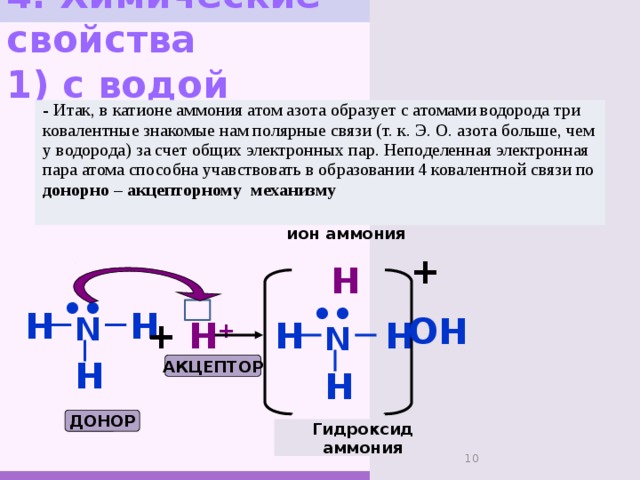
4. Химические свойства 1) с водой
- Итак, в катионе аммония атом азота образует с атомами водорода три ковалентные знакомые нам полярные связи (т. к. Э. О. азота больше, чем у водорода) за счет общих электронных пар. Неподеленная электронная пара атома способна учавствовать в образовании 4 ковалентной связи по донорно – акцепторному механизму
ион аммония
+
H
••
••
H
H
N
ОН
+ H +
H
H
N
H
АКЦЕПТОР
H
ДОНОР
Гидроксид аммония
7

Вывод: аммиак обладает основными (щелочными) свойствами
Следует запомнить так же, что в ионе аммония валетность азота IV,
а степень окисления -3.
Гидроксид аммония или «нашатырный спирт» (10% р-р аммиака в воде)

Химические свойства
2) с кислотами
NН 3 +НСI NН 4 СI
хлорид аммония( нашатырь)
3)Аммиак горит в кислороде
- Запишите в тетрадь с учебника обе реакции: горения аммиака в чистом кислороде и в присутствии катализатора.
- Выполните задание: 1 вариант – проставьте степень окисления у азота в первой реакции , 2 вариант – во второй, и в паре обсудите, какие продукты образуются в обеих реакциях и в каком случае аммиак теряет больше электронов
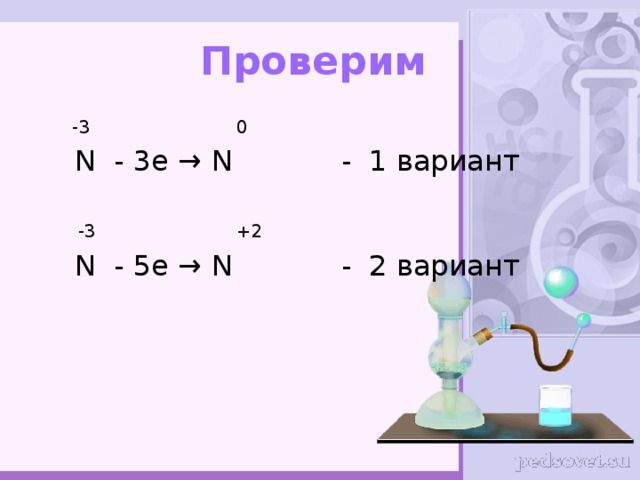
Проверим
-3 0
N - 3e → N - 1 вариант
-3 +2
N - 5e → N - 2 вариант

- Состав и строение молекулы аммиака.
- Физические свойства аммиака.
- Способы получения аммиака
- Химические свойства аммиака.
- Применение аммиака

Правильные ответы:
1вариант 2 вариант
1 – г 1 – б
2 –б 2 – г
3 – б 3 – а
4 – в 4 – б
5 – а 5 – в
Критерии оценивания:
- 5 правильных ответов - оценка «5»
- 4 правильных ответа - оценка «4»
- 3 правильных ответа - оценка «3»
- 2 правильных ответа - оценка «2»

ИТОГИ УРОКА
- С каким газом мы сегодня познакомились?
- Что мы про него узнали?
- Чему вы научились на уроке?
Домашнее задание:
параграф 17, применение аммиака
Применение
NH 3

Спасибо за урок!



































