
РАСТВОР КАК ОСНОВА ЖИЗНЕДЕЯТЕЛЬНОСТИ КЛЕТОК ОРГАНИЗМА
Представлен интегрированный урок по химии и биологии. Данная методическая разработка объединяет как теоретическую часть, так и экспериментально-практическую.
Толегенова К.К.
900igr.net

ЦЕЛЬ УРОКА
Цель деятельности педагога
Интеграция школьных естественнонаучных предметов для дальнейшего развития и совершенствования химического образования в школе.
Собственно цель урока
Систематизация, углубление знаний о растворах как основы жизнедеятельности клеток организма.

ЗАДАЧИ УРОКА
- Дидактические задачи. Обобщение знаний учащихся о растворах, осуществление коррекции знаний, создание условий для этих знаний применения при изучении цитологии, закрепление умений решать расчетные задачи.
- Воспитательные задачи. Формирование умений работать самостоятельно и в малых группах способствует развитию навыков само- и взаимоконтроля, сотрудничества и чувства ответственности основано на принципе сочетания коллективных и индивидуальных форм обучения.

ЗАДАЧИ УРОКА
- Развивающие задачи. Развитие логического мышления, а именно синтетико-аналитического на основе выполнения практических заданий, а также познавательного интереса к естественным наукам, формирование целостной картины мира.
- Научные задачи. Развитие навыков синтезировать и анализировать материал, формирование научной картины окружающего мира, формирование исследовательской культуры.

АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ
Например, водный раствор хлорида натрия с массовой долей 20% - это такой раствор в 100 единицах массы которого содержится 20 единиц массы хлорида натрия и 80 единиц массы воды

АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ
МОЛЯРНАЯ ДОЛЯ –
отношение количества растворенного вещества (или растворителя) к сумме количеств веществ, составляющих раствор.
Допустим, раствор содержит 1 моль растворителя и 2 моль растворенного вещества.
Тогда
N 1 = 1 / ( 1 + 2 ) молярная доля растворителя
N 2 = 2 / ( 1 + 2 ) молярная доля растворенного вещества

АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ
МОЛЯРНАЯ КОНЦЕНТРАЦИЯ (МОЛЯРНОСТЬ) – отношение количества растворенного вещества (или растворителя) к объему раствора.
Например, 2 М H 2 SO 4 означают, что в 1 литре раствора содержится 2 моля серной кислоты, т.е. С=2 моль/л

АКТУАЛИЗАЦИЯ ОСНОВНЫХ ПОНЯТИЙ
Эквивалентная (нормальная) концентрация
отношение числа эквивалентов растворенного вещества к объему раствора.
Пример
2 Н серной кислоты означает раствор, в 1 литре, которого содержится 2 эквивалентные массы серной кислоты

РЕШЕНИЕ ЭКСПЕРИМЕНТАЛЬНО-РАСЧЕТНЫХ ЗАДАЧ ПО РАСТВОРАМ
Оборудование:
штатив с пробирками, растворы хлорид бария, серная кислота, коническая колба, воронка, фильтровальная бумага, стеклянная палочка, спиртовка, спички, держатель для пробирок, мерный цилиндр

ЗАДАЧА №1 определение массы вещества по заданной концентрации
ДАНО:
m (BaSO 4 ) = 23,3
( H 2 SO 4 ) = 20%
m (20% раствора H 2 SO 4 ) - ?
РЕШЕНИЕ :
BaCl 2 + H 2 SO 4 = BaSO 4 +2HCl
(получить экспериментально)
m (20% раствора H 2 SO 4 ) = = (9,8 20) 100=49 ( г )
ОТВЕТ : масса 20% раствора серной кислоты равна 49 г.

ЗАДАЧА № 2 определение объема раствора по известной его концентрации
РЕШЕНИЕ :
Эквивалентная масса H 2 SO 4 = 49 г
В одном л 0,5Н раствора содержится 24,5 г, тогда в 2 л раствора - 49 г
Пусть x – масса 96% раствора H 2 SO 4
100 : 96= x:49 x=51,04 г
V (H 2 SO 4 ) = m/ ρ = 27,74 ( см 3 )
ДАНО:
(H 2 SO 4 ) = 96 %
ρ (H 2 SO 4 ) = 1,84 г/см 3
V = 2 л 0,5 Н раствора
V (H 2 SO 4 ) - ? см 3
ОТВЕТ : объем 96% раствора серной кислоты равен 27,73 см 3 .

АКТУАЛИЗАЦИЯ МЕЖПРЕДМЕТНЫХ ПОНЯТИЙ
Осмос – это переход молекул растворителя из области с высокой концентрации в область с более низкой концентрацией через полупроницаемую мембрану
Диффузия – это движение молекул или ионов из области с высокой концентрации в область с более низкой концентрацией
Осмотическое давление – гидростатистическое давление, которое необходимо приложить для предотвращения поступления воды в раствор, в случае отделения данного раствора избирательно проницаемой мембраной от чистой воды.

ОПЫТ №1 Изучение осмоса в живых растительных клетках
Материал и оборудование
эпидермис (кожица) лука или молодого ревеня, микроскоп, 2 покровных и 2 предметных стекол, скальпель, пинцет, дистиллированная вода, 1М раствор сахароза, 2 пипетки с грушей, фильтровальная бумага
Методика проведения опыта
Скальпелем и пинцетом отделите полоску эпидермиса с нижней поверхности луковицы или с черенка листа ревеня. Быстро перенесите оторванную полоску эпидермиса на предметное стекло и капните на него 2-3 капли дистиллированной воды. Накройте покровным стеклом и посмотрите, как выглядят клетки эпидермиса под микроскопом. Зарисуйте несколько разных клеток.

ОПЫТ №1 Изучение осмоса в живых растительных клетках
Методика проведения опыта
- Скальпелем отделите другую полоску эпидермиса с нижней поверхности луковицы или с черенка листа ревеня. Повторите всю процедуру, капнув вместе воды 1М раствора сахарозы. Понаблюдайте под микроскопом за ней в течение 15 минут при большом увеличении. Зарисуйте происходящие изменения в одной или нескольких клетках.
- Проведем эксперимент наоборот. Последнюю полоску под микроскопом необходимо дистиллированной водой промыть для удаления раствора сахарозы. Затем избыток жидкости убрать фильтрованной бумагой.

ОПЫТ №1 Изучение осмоса в живых растительных клетках
Результаты : учащиеся должны были определить, какие процессы происходили с полосками эпидермиса луковицы (ревеня).
А именно: плазмолиз (от греч. plásma — вылепленное, оформленное и lýsis — разложение, распад) – протопласт под действием раствора сахарозы сморщивается и отстает от клеточной стенки;
обратный процесс – деплазмолиз

ОПЫТ №2 Определение среднего осмотического давления клеточного сока в препарате растительных клеток методом начинающего плазмолиза
Материал и оборудование
черенок ревеня или луковица, микроскоп, 4 чашки Петри, 4 пробирки, штатив для пробирок, этикетка или восковой карандаш, 2 градуированные пипетки на 10 или 25 мл, 2 стакана на 100 мл, тонкая кисточка для рисования, скальпель, тонкий пинцет, дистиллированная вода, 1М раствор сахарозы, предметно и покровное стекла, миллиметровка.
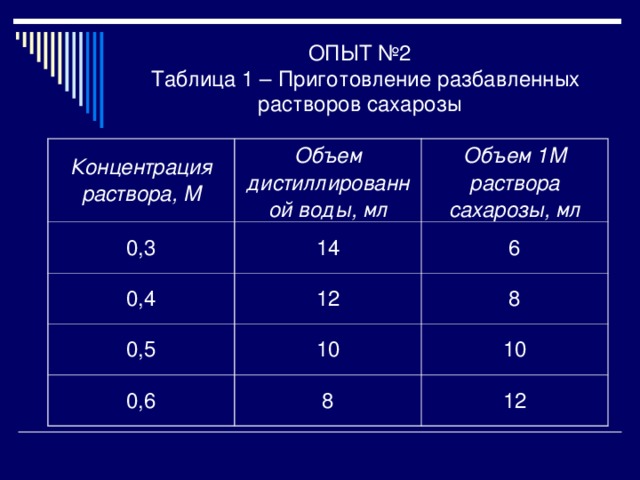
ОПЫТ №2 Таблица 1 – Приготовление разбавленных растворов сахарозы
Концентрация раствора, М
Объем дистиллированной воды, мл
0,3
Объем 1М раствора сахарозы, мл
14
0,4
12
6
0,5
8
10
0,6
8
10
12

ОПЫТ №2 Таблица 2 – Осмотическое давление растворов сахарозы при 20 С
Концентрация раствора, М
Осмотическое давление, кПа
0,3
Осмотическое давление, атм
820
0,4
1120
8,1
0,5
11,1
1450
0,6
1980
14,3
19,5

ПРОВЕРКА ПОЛУЧЕННЫХ ЗНАНИЙ
ВОПРОСЫ
ЗАДАЧА
Содержание белка в организме человека составляет 17 % от массы тела. Азота в белке содержится 16%. Определить массу азота в собственном организме, исходя из массы твоего тела (кг).
- Расскажите, как произвести плазмолиз опытным путем?
- В чем суть деплазмолиза?
- Существует ли зависимость между количеством плазмолизированных клеток и молярностью раствора сахарозы? Какая?
- Дайте определение диффузии. Что такое «осмос»?
- Как зависит осмотическое давление от концентрации раствора сахарозы?
- Какое значение имеют растворы в жизнедеятельности клеток организма?

Пример решения проверочной задачи
РЕШЕНИЕ
m б = m т б = 11,9 (кг) –
масса белка в организме
ma = m б а = 1,9 (кг) –
масса азота в организме
ДАНО:
m т = 70 кг
б =0,17
а =0,16
m а - ?
ОТВЕТ: масса азота в организме равна 1,9 кг.



































