

- При электролизе окислителем и восстановителем является электрический ток.
- Процессы окисления и восстановления разделены в пространстве, они совершаются не при контакте частиц друг с другом, а при соприкосновении с электродами электрической цепи.
- Катод - отрицательно- заряженный электрод.
- Анод – положительно-заряженный электрод.
- Катион- «+»ион, анион- «-» ион.

- Катодные процессы в водных растворах электролитов :катионы или молекулы воды принимают электронов и восстанавливаются.
- Li,K,Ca, | Mn,Zn,Fe,Ni,| H 2 |Cu,Hg,Ag,Pt
Na,Mg,Al Sn,Pb Au
Катионы металлов не | Катионы металлов и молекулы воды| Катионы
восстанавливаются . восстанавливаются металлов
Восстанавливается вода восстанавливаются

1. Катионы металлов со стандартным электродным потенциалом, большим, чем у ВОДОРОДА, расположены в ряду напряжений после него: Cu 2+ , Hg 2+ , Ag + , Pt 2+ , ..., до Pt 4+ . При электролизе они почти полностью восстанавливаются на катоде и выделяются в виде металла.
- Cu 2+ + 2e – = Cu 0 , E 0 =0,337 В
- 2H 2 O + 2e – = H 2 + 2OH – , E 0 =–0,83 В

2. Катионы металлов с малой величиной стандартного электродного потенциала (катионы металлов начала ряда напряжений Li + , Na + , K + , Rb + , ..., до Al 3+ включительно). При электролизе на катоде они не восстанавливаются, вместо них восстанавливаются молекулы воды.
- 2H 2 O + 2e – = H 2 + 2OH – , E 0 =–0,83 В

3. Катионы металлов со стандартным электродным потенциалом меньшим, чем у ВОДОРОДА, но большим, чем у алюминия (Mn 2+ , Zn 2+ , Cr 3+ , Fe 2+ , ..., до H). При электролизе эти катионы, характеризующиеся средними величинами электроноакцепторной способности, на катоде восстанавливаются одновременно с молекулами воды.
- 2H 2 O + 2e – = H 2 + 2OH –

- Cu 2+ + 2e – = Cu 0 , E 0 = + 0,337 В
4. На катоде легче всего разряжаются катионы того металла, которому отвечает наиболее положительный потенциал. Так, например, из смеси катионов Cu 2+ , Ag + и Zn 2+ при достаточном напряжении на клеммах электролизера вначале восстанавливаются ионы серебра ( E 0 =+0,79 В), затем меди ( E 0 =+0,337 В) и, наконец, цинка ( E 0 = – 0,76 В).
- Ag + + 2e – = Ag 0 , E 0 = + 0, 79 В
E 0 = - 0, 76 В

- На аноде происходит окисление анионов или молекул воды ( частицы отдают электронов - окисляются)
- Анионы по их способности окисляться располагаются в следующем порядке:
Iˉ,Brˉ,S²ˉ,Clˉ,OHˉ, SO 4 ²ˉ,NO 3 ˉ,Fˉ
------------------------------------------------- --------- →
Восстановительная активность уменьшается.

- 2Cl – – 2e – = Cl 2 2H 2 O – 4e – = O 2 + 4H +
4OH – – 4e – = 2H 2 O + O 2
- Анионы кислородосодержащих кислот не окисляются, так как их стандартный потенциал намного превышает потенциал воды 2SO 4 2– – 2e – = S 2 O 8 2– , E 0 =+2,01 В
поэтому вместо них окисляется вода:
2H 2 O – 4e – = O 2 + 4H + , E 0 =1,228 В

- При электролизе водного раствора соли из активного металла и кислородосодержащей кислоты на катоде выделяется Н 2 , а на аноде – О 2 .
К- Na 2 SO 4 А +
← Na + SO 4 ²ˉ →
2H 2 O + 2e – → H 2 + 2OH – | 2H 2 O- 4e ˉ → O 2 +4H +
Электролиз воды 2H 2 O → Н 2 ↑ +О 2 ↑

2H 2 O + 2NaCl = H 2 + Cl 2 + 2NaOH
Если металл средней активности связан с кислородосодержащим анионом , то на катоде образуется металл и Н2, на аноде – О 2 .
ZnSO 4 +2H2O→Zn+H2+O2+H2SO4
При электролизе раствора соли из металла средней активности и бескислородной кислоты на катоде образуется металл и Н2, на аноде – неметалл. 2ZnCl2+2H2O→Zn+H2+Zn(OH)2+2Cl2

- При электролизе водного раствора соли из мало активного металла и кислородосодержащей кислоты на катоде выделяется металл, а на аноде – О 2 и кислота . K- С uSO 4 A +
Cu 2+ SO 4 ²ˉ
← →
Cu 2+ + 2e – = Cu 0 2H 2 O – 4e – = O 2 + 4H +
2 С uSO 4 + 2H 2 O=2 С u+ O 2 +2H 2 SO 4

- При электролизе катиона аммония N H 4 +
восстанавливается вода.
- При электролизе солей органических кислот на катоде восстанавливается вода, на аноде анион кислоты с образованием алкана и углекислого газа.
2CH 3 COONa +2H 2 O=C 2 H 6 ↑+2CO 2 ↑+H 2 ↑+2NaOH

- Электролиз раствора щелочи – это электролиз воды.
- Электролиз раствора кислородосодержащей кислоты – это тоже электролиз воды.
- Электролиз бескислородной кислоты: на катоде образуется водород, на аноде –неметалл.

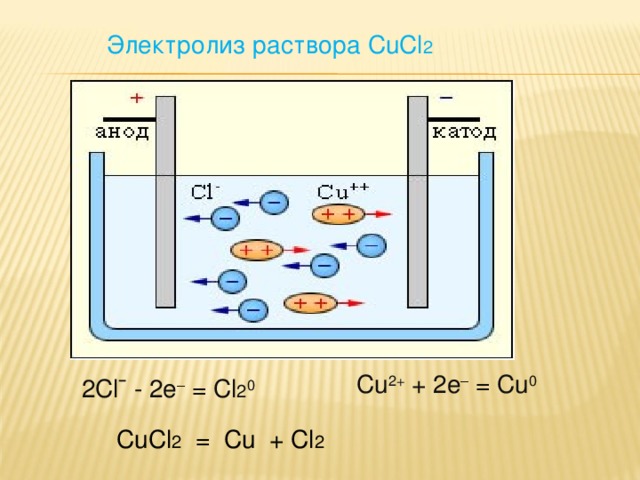
2 C lˉ - 2e – = C l 2 0
Электролиз раствора CuCl 2
Cu 2+ + 2e – = Cu 0
CuCl 2 = Cu + Cl 2































