
ГАОУ СО «Лицей –интернат 64» ЗАГАДКА ВОДЫ
Выполнил: Комиссаров Кирилл, обучающийся 10 класса направления «Биотехнологии» Руководитель: Романова Вероника Олеговна , учитель химии, Кандидат Химических Наук.

В этом году во многих регионах России стояли сильные морозы и в сети появилось много видео с интересным названием «Дубак челлендж». Красивая картинка получалась из-за того, что капельки кипятка на сильном морозе мгновенно превращались в льдинки. Любопытно то, что с холодной водой это явление не наблюдается. Хотя у нас стояли не столь сильные морозы всего-то -25, мне все-таки удалось наблюдать это явление. Я проделал такой опыт, т.е. выплёскивал над собой и кипяток, и воду комнатной температуры.

- https://disk.yandex.ru/i/wlXxV8_BUtt3gg

Действительно, кипяток успевал замёрзнуть, а холодная вода - нет. Я поискал объяснения в сети, а там всё сводится к ещё большей загадке - парадоксу Мпембы. Суть его в том, что более горячая вода замерзает (кристаллизуется) раньше холодной.

- Цель работы: Попытаться объяснить природу парадокса Мпембы.
- Задачи: Провести эксперимент и изучить структуру воды.

Эффект Мпембы
- С этим парадоксом люди знакомы с давних времён, однако не придавали ему значения. Явление при котором горячая вода замерзает быстрее холодной отмечал ещё Аристотель. Начало научного изучения этого явления было положено в 1963году. Пытливый юноша из Танзании Эрасто Мпемба, будучи студентом кулинарного техникума обратил внимание на то, что при приготовлении мороженого более горячая смесь замёрзла раньше более холодной . Он повторил эксперимент с водой и парадоксальный эксперимент подтвердился.

Случилось так, что Мпембе посчастливилось встретиться с профессором Деннисом Осборном и изложить ему суть эксперимента. Осборн заинтересовался наблюдениями юноши, провёл ряд экспериментов, подтвердивших наличие эффекта, но причины установлены не были. Было выдвинуто много гипотез о причинах возникновения эффекта. В 2012 году Британским Королевским химическим обществом был объявлен конкурс гипотез, объясняющих эффект. Было выдвинуто более 20000 научных работ от учёных всего мира, но не одна статья не внесла ясности в это загадочное явление. Я не буду перечислять все версии, их можно увидеть открыв в поисковике «Эффект Мпембы». Самое последнее объяснение предложили учёные из Китая и США.

Авторы опирались на поведение кластеров молекул воды объединённых водородными связями. Водородные связи намного слабее ковалентных, однако, сила их зависит от геометрии взаимного расположения молекул, между которыми эта связь образуется. По мере нагревания водородные связи ослабевают и, как показало моделирование, молекулы воды в кластерах меняют положение, занимая такие позиции, из которых им проще переходить к кристаллической структуре льда. В холодной воде всё происходит также, только энергии на разрыв водородных связей требуется больше – и замерзание, соответственно, должно проходить медленнее

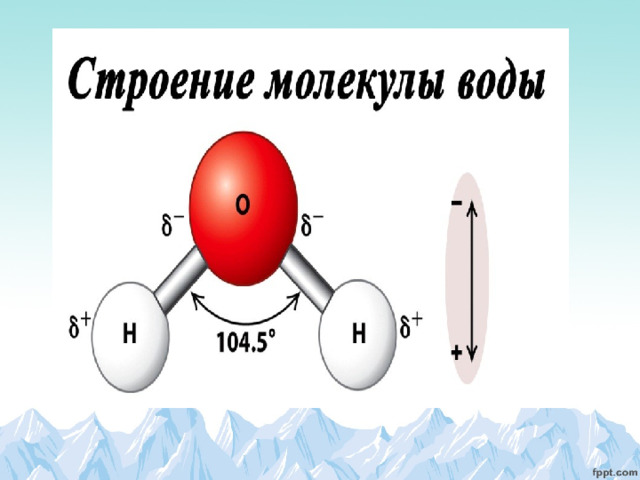
Чтобы как то понять эту гипотезу я решил обратиться к строению воды. Казалось бы что может быть проще воды, но как оказывается самое простое бывает крайне сложным. Не смотря на то, что вода была известна человечеству от начала его существования, впервые в лабораторных условиях она была получена лордом Г. Кавендишем в 1781году при сгорании водорода.

В 1783году Лавуазье предложил истинный состав воды как сложного соединения кислорода и водорода. В 1800году А. Карлейль и У. Никольсон электрическим током от вольтова столба разложили воду на кислород и водород 1805год. Ж. Л. Гей-Люссак и А. Гумбольдт установили, что для образования воды необходимо 2 объёма водорода и 1 объём кислорода. 1842год. Ж. Б. Дюма установил весовое соотношение водорода и кислорода как 2:16. 1860год. С. Канницаро предложил точную химическую формулу воды как H 2 O .
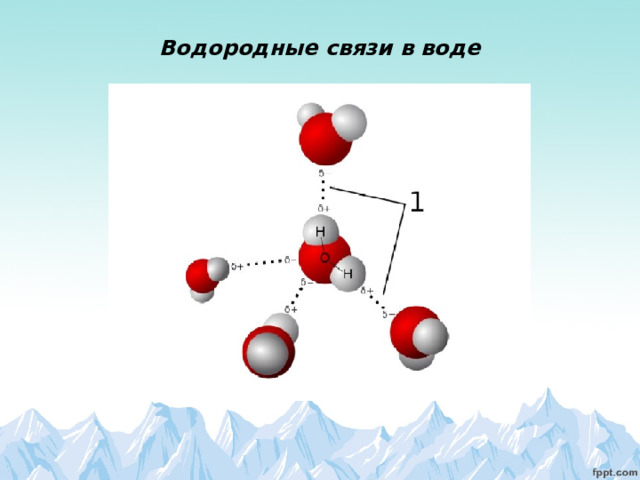
Водородные связи в воде
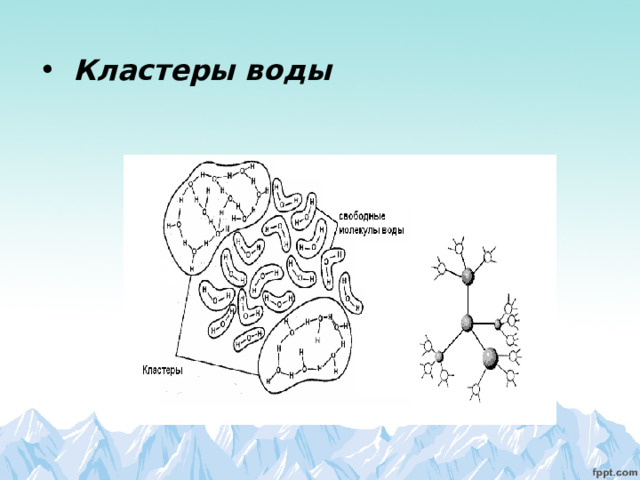

Чтобы попасть каждой молекуле в узел кристаллической решётки нужно разрушить каждый кластер. У холодной воды кластер крупнее и молекулы при распределении в кристалле требуют больше энергии для разрушения кластера, следовательно и процесс замерзания у неё дольше. Вот теперь с теоретической точки зрения всё стало ясно и понятно. Решил экспериментально проверить существование эффекта Мпембы, ведь в каких- то случаях он может и не проявляться. Поместил в морозильную камеру одинаковые по массе но разные по температуре образцы воды налитой из под одного и того же крана.

Проанализировав явления кристаллизации металлов и воды, у меня возникла аналогия. Пусть мы роняем шарик в ванну с водой с различной высоты

В первом случае шарик коснётся поверхности воды раньше, чем во втором случае, ведь время падения зависит от высоты. Совсем недавно у нас на эту тему была лабораторная работа по физике. Однако, слой воды второй шарик пройдёт быстрее, т.к. у него большая скорость при входе в воду, чем у первого. А вот какой шарик достигнет дна быстрее, зависит от суммы времени прохождения расстояния в воздухе и в воде. Итоговый результат может быть разным. Всё зависит от начального положения шариков. Похожая ситуация с остыванием и кристаллизацией. Более нагретый образец во всех случаях остывает дольше, но кристаллизуется быстрее. Поэтому, в каких то случаях эффект Мпембы наблюдается, а в каких то- нет, всё зависит от начальных температур взятых образцов.

Каждые пять минут я снимал показания термометров, результат свёл в график.
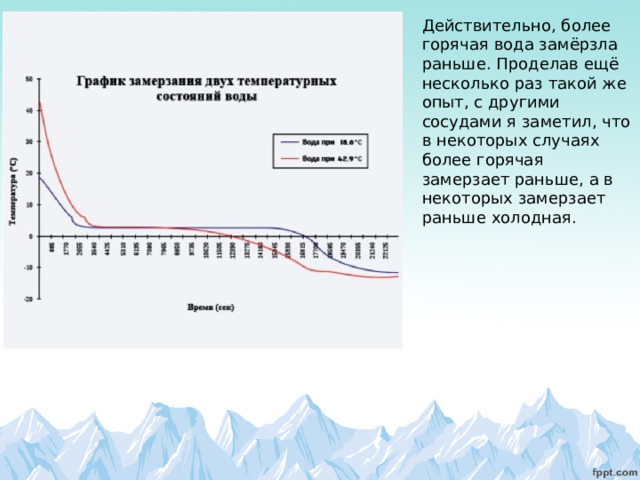
Действительно, более горячая вода замёрзла раньше. Проделав ещё несколько раз такой же опыт, с другими сосудами я заметил, что в некоторых случаях более горячая замерзает раньше, а в некоторых замерзает раньше холодная.

Но во всех опытах время кристаллизации более горячей воды меньше времени кристаллизации более холодной.
Я провёл ещё один эксперимент. Заморозил одинаковое количество воды в одинаковых сосудах, одну воду замораживал в морозилке до -18 градусов C , другую на улице до -7 градусов С, затем занес их в комнату с температурой +23 градуса.

Каждые три минуты снимал показания термометров, по результатам построил график.
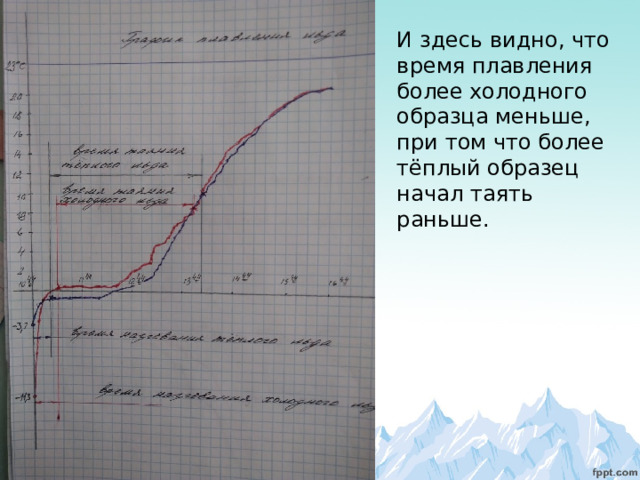
И здесь видно, что время плавления более холодного образца меньше, при том что более тёплый образец начал таять раньше.

Вывод: Чем больше разница температур взятого образца воды с температурой замерзания (таяния), тем меньше время фазового перехода .
В своих опытах я увидел как это происходит, что подтверждает теоретические объяснения.
И тут мне пришло в голову расплавить свечку .

Я отрезал кусочек свечи и расплавил его и нагрел расплав до 100 С, при остывании он затвердел за 13 минут.
Когда же я нагрел его до 150 С, то он застывал 8 минут.


Но свеча изготовлена из стеарина, т.е органического вещества и здесь возможны водородные связи, кроме того стеарин---аморфен.
Этот эксперимент ничего не доказывает.
Я стал плавить олово.

Нагревал до полного плавления при температуре 232 С , и держал над огнём ещё пол минуты, снимал с огня и засекал время от начала кристаллизации до полного отвердевания. Время кристаллизации составило1 мин. 10 сек.
Затем расплавлял то же олово, и держал над огнём 3 минуты. Время кристаллизации составило 55 секунд.


Я взял свинец. Расплавил и подержал над огнём пол минуты. Время кристаллизации составило 20 сек. После того как я держал свинец над огнём в течении 3 минут после плавления, время кристаллизации составило 15 сек.
Тоже самое я проделал с цинком. Время кристаллизации «холодного» образца – 1 мин., время кристаллизации «горячего» -51 сек.

Но ведь в металлах водородных связей нет, а эффект присутствует. Следовательно, версия американских и китайских учёных относительно эффекта Мпембы, к сожалению, не состоятельна.
Мне не удалось достичь цели своей работы: я не смог объяснить парадокс Мпембы. Но я познакомился поближе с водой и выяснил, что чем больше разница температур взятого образца и температуры плавления (кристаллизации) тем быстрее протекает фазовый переход из жидкости в твёрдое состояние.

Вывод:
Более быстрое замерзание горячей воды по сравнению с холодной обусловлено более быстрым торможением молекул горячей воды.














































