Проверочная работа.
1. Годом открытия периодического закона Д. И. Менделеева считают:
А. 1868; В. 1869; С. 1861; D. 1943.
2. В основе современной классификации химических элементов лежит:
А. валентность; В. строение атома; С. атомная масса; D. число протонов в ядре атома.
3. Химические свойства элемента определяются, прежде всего:
А. зарядом ядра атома; В. положение элемента в периодической системе;
С. атомной массой; D. строением внешнего электронного уровня.
4. У химических элементов каждого периода с возрастанием атомного номера:
А. атомный радиус и электроотрицательность уменьшаются;
В. атомный радиус увеличивается, электроотрицательность возрастает;
С. атомный радиус увеличивается, электроотрицательность уменьшается;
D. атомный радиус уменьшается, электроотрицательность возрастает.
5. Какой объём (л, н.у.) кислорода потребуется для горения 16 г S?
А. 22,4; В. 11,2; С. 44,8; D. 56.
6. В каком из следующих соединений массовая доля хлора наибольшая?
А. NaCl; В. KCl; С. CaCl2; D. AlCl3.
7

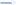 . Найдите вещество Х в следующем превращении. Al AlCl3 X Al2O3
. Найдите вещество Х в следующем превращении. Al AlCl3 X Al2O3
А) Al2(SO4)3 В) AlBr3 С) Al(OH)3 D) Al(NO3)3
8. Масса соли для приготовления 20%-ного раствора массой 300 г равна:
А. 320 г; В. 280 г; С. 60 г; D. 30 г.
9. Какому химическому элементу соответствует электронная формула…3d104s24p5?
А. Cl; В.Br; С.Mn; D. Co.
10. При воздействии на какие вещества соляной кислотой можно получить хлорид железа (III)? 1) Fe, 2) FeO, 3) Fe2O3, 4) Fe(OH)2, 5) Fe(OH)3, 6) FeS2.
А. 1,2,4,6; В. 2,3,6; С. 3,5; D. 1,3.
11. Молярная масса оксида железа (III) равна:
А. 72 г/моль; В. 160 г/моль; С. 232 г/моль; D. 420 г/моль.
12. В каком ряду химических элементов знаки расположены в порядке возрастания их электроотрицательности?
А) Ag, Fe, H, C, Cl; В) Ca, Si, Al, P, Br; С) K, Cu, Zn, S, O; D) B, Se, As, Ge, Ga.
13. 80 г 15 % раствора добавили 20 г воды. Найдите концентрацию образовавшегося раствора? А. 12 %; В. 15 %; С. 20 %; D. 18 %.
14. Число атомов в 12 г углерода? А. 6.09*1023; В. 6.02*1023; С. 6.05*1025; D. 6.02*1020.
15. Число атомов в 18 г углерода?
А. 6.02*1023; В. 3.01*1023; С. 9.03*1023; D. 6.02*1020.
16. Найдите массу газа кислорода занимающего при н.у. объем 5,6 л.
А) 8 В) 16 С) 32 D) 48
17. Какое вещество образуется при горении железа в кислороде?
А) FeO В) Fe2O3 С) Fe3O4 D) железо в кислороде не горит.
18. В хлориде цезия химическая связь ____________.
19. Вещество состоит из 26,5 % калия, 35,4 % хрома, 38,1 % кислорода. Вычислите формулу.
20. Подгруппы, включающие только элементы больших периодов, называются….
Проверочная работа.
1. Годом открытия периодического закона Д. И. Менделеева считают:
А. 1868; В. 1869; С. 1861; D. 1943.
2. В основе современной классификации химических элементов лежит:
А. валентность; В. строение атома; С. атомная масса; D. число протонов в ядре атома.
3. Химические свойства элемента определяются, прежде всего:
А. зарядом ядра атома; В. положение элемента в периодической системе;
С. атомной массой; D. строением внешнего электронного уровня.
4. У химических элементов каждого периода с возрастанием атомного номера:
А. атомный радиус и электроотрицательность уменьшаются;
В. атомный радиус увеличивается, электроотрицательность возрастает;
С. атомный радиус увеличивается, электроотрицательность уменьшается;
D. атомный радиус уменьшается, электроотрицательность возрастает.
5. Какой объём (л, н.у.) кислорода потребуется для горения 16 г S?
А. 22,4; В. 11,2; С. 44,8; D. 56.
6. В каком из следующих соединений массовая доля хлора наибольшая?
А. NaCl; В. KCl; С. CaCl2; D. AlCl3.
7

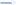 . Найдите вещество Х в следующем превращении. Al AlCl3 X Al2O3
. Найдите вещество Х в следующем превращении. Al AlCl3 X Al2O3
А) Al2(SO4)3 В) AlBr3 С) Al(OH)3 D) Al(NO3)3
8. Масса соли для приготовления 20%-ного раствора массой 300 г равна:
А. 320 г; В. 280 г; С. 60 г; D. 30 г.
9. Какому химическому элементу соответствует электронная формула…3d104s24p5?
А. Cl; В.Br; С.Mn; D. Co.
10. При воздействии на какие вещества соляной кислотой можно получить хлорид железа (III)? 1) Fe, 2) FeO, 3) Fe2O3, 4) Fe(OH)2, 5) Fe(OH)3, 6) FeS2.
А. 1,2,4,6; В. 2,3,6; С. 3,5; D. 1,3.
11. Молярная масса оксида железа (III) равна:
А. 72 г/моль; В. 160 г/моль; С. 232 г/моль; D. 420 г/моль.
12. В каком ряду химических элементов знаки расположены в порядке возрастания их электроотрицательности?
А) Ag, Fe, H, C, Cl; В) Ca, Si, Al, P, Br; С) K, Cu, Zn, S, O; D) B, Se, As, Ge, Ga.
13. 80 г 15 % раствора добавили 20 г воды. Найдите концентрацию образовавшегося раствора? А. 12 %; В. 15 %; С. 20 %; D. 18 %.
14. Число атомов в 12 г углерода? А. 6.09*1023; В. 6.02*1023; С. 6.05*1025; D. 6.02*1020.
15. Число атомов в 18 г углерода?
А. 6.02*1023; В. 3.01*1023; С. 9.03*1023; D. 6.02*1020.
16. Найдите массу газа кислорода занимающего при н.у. объем 5,6 л.
А) 8 В) 16 С) 32 D) 48
17. Какое вещество образуется при горении железа в кислороде?
А) FeO В) Fe2O3 С) Fe3O4 D) железо в кислороде не горит.
18. В хлориде цезия химическая связь ____________.
19. Вещество состоит из 26,5 % калия, 35,4 % хрома, 38,1 % кислорода. Вычислите формулу.
20. Подгруппы, включающие только элементы больших периодов, называются….







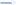 . Найдите вещество Х в следующем превращении. Al AlCl3 X Al2O3
. Найдите вещество Х в следующем превращении. Al AlCl3 X Al2O3









