
Урок по химии в 8 классе в соответствии с ФГОС второго поколения
Колесникова Оксана Михайловна
учитель химии МБОУ «СШ №55» Г. Иваново.

Основные классы неорганических соединений уже изученные:
n

Распределите формулы по классам в таблицу
оксиды
основания
HCl HNO 3 H 2 SO 4
Ca(OH) 2 K 2 O Na 2 O
Al 2 O 3 Zn(OH) 2 Fe(OH) 3
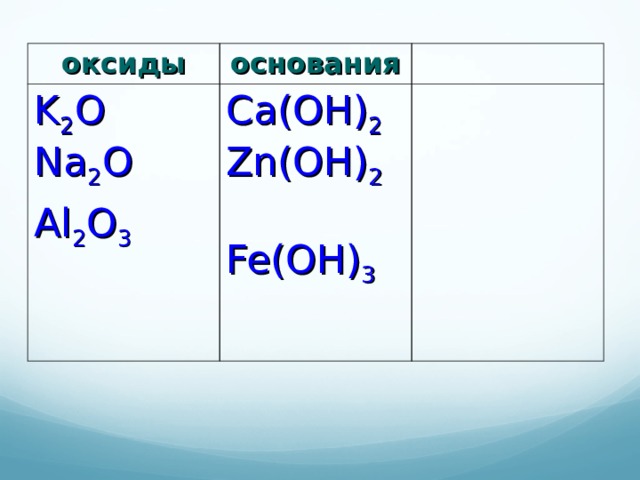
оксиды
основания
K 2 O Na 2 O
Al 2 O 3
Ca(OH) 2 Zn(OH) 2 Fe(OH) 3
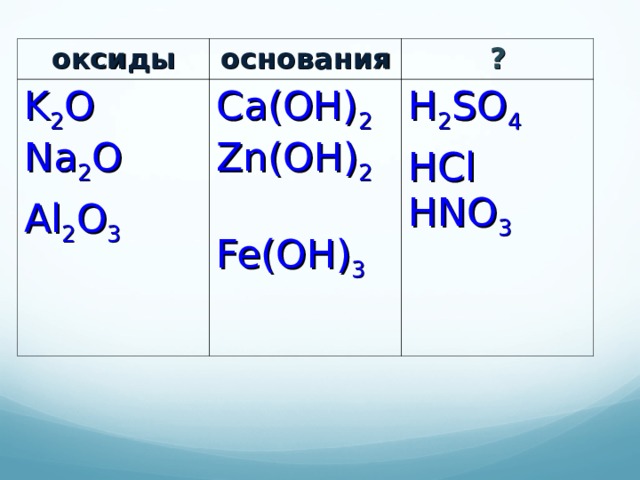
оксиды
основания
K 2 O Na 2 O
Al 2 O 3
?
Ca(OH) 2 Zn(OH) 2 Fe(OH) 3
H 2 SO 4
HCl HNO 3

Тема урока: Кислоты.
ПУТЕШЕСТВИЕ
В МИР КИСЛОТ

ЦЕЛИ УРОКА :
- Сформировать понятие «кислоты».
- Познакомиться с составом, классификацией и представителями кислот.
- Формировать умения экспериментировать, наблюдать, и делать выводы.

МАРШРУТ ПУТЕШЕСТВИЯ
- Станция Информационная
- Станция Историческая
- Станция C топ! Красный свет!
- Станция Индикаторная
- Станция Практическая

СТАНЦИЯ ИНФОРМАЦИОННАЯ
Кислоты – это сложные вещества , состоящие из атомов водорода и кислотных остатков.
Н Cl H NO 3 H 2 SO 4
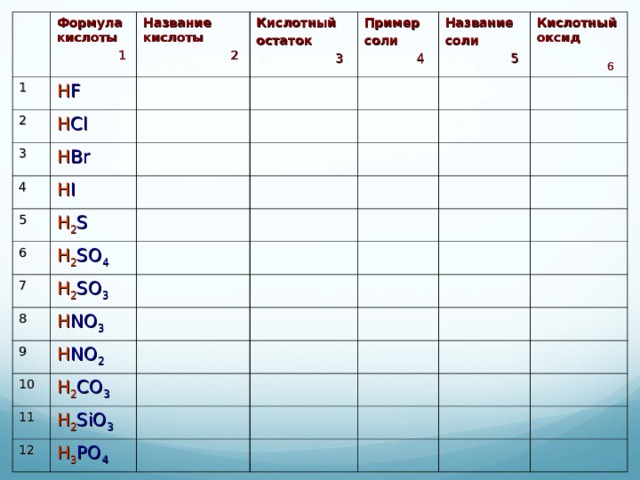
1
Формула кислоты
1
Название кислоты
2
2
H F
3
Кислотный
остаток
3
H Cl
Пример
соли
4
H Br
4
5
Название
соли
5
H I
6
Кислотный оксид
6
H 2 S
7
H 2 SO 4
8
H 2 SO 3
H NO 3
9
10
H NO 2
11
H 2 CO 3
H 2 SiO 3
12
H 3 PO 4
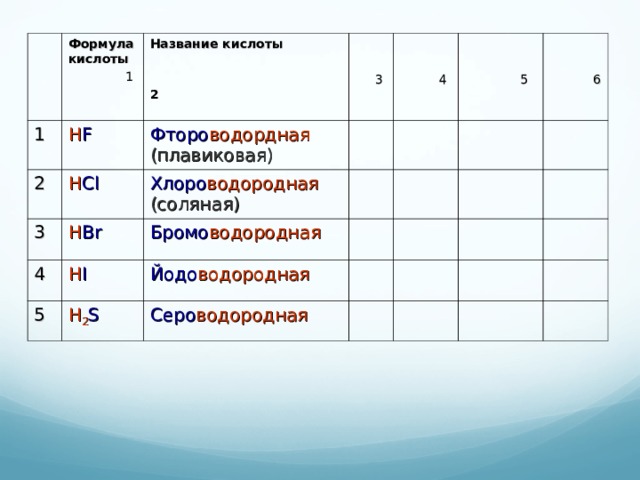
1
Формула кислоты
1
Название кислоты
2
H F
2
3
3
Фторо водордная (плавиковая)
H Cl
4
H Br
Хлоро водородная (соляная)
4
Бромо водородная
H I
5
5
Йодо водородная
H 2 S
6
Серо водородная
6
7
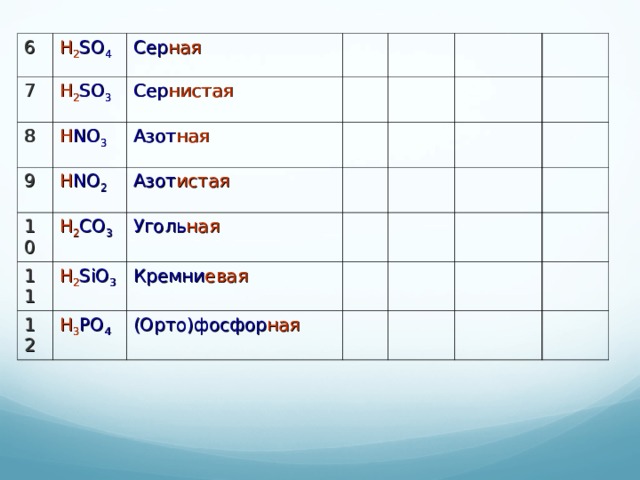
H 2 SO 4
Сер ная
H 2 SO 3
8
Сер нистая
H NO 3
9
Азот ная
H NO 2
10
11
Азот истая
H 2 CO 3
Уголь ная
H 2 SiO 3
12
Кремни евая
H 3 PO 4
(Орто)фосфор ная
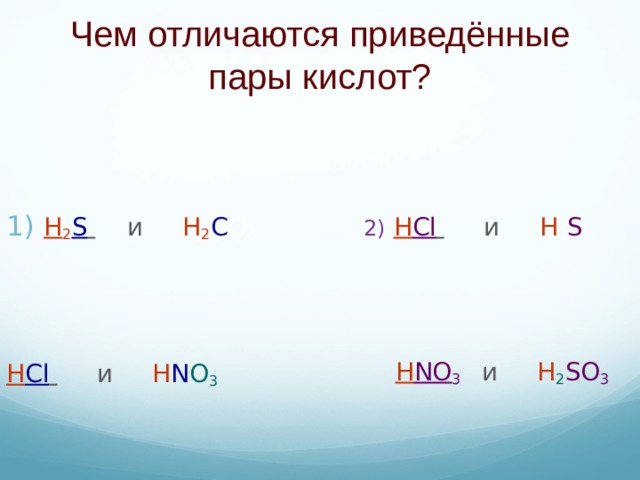
Чем отличаются приведённые пары кислот ?
2) H Cl и H 2 S
H NO 3 и H 2 SO 3
H Cl и H N O 3

Классификация кислот
1. По содержанию кислорода.
бескислородные
HF HCl
HBr HI H 2 S
кислородсодержащие
HN O 3 H 2 S O 4
H 2 C O 3 H 3 P O 4
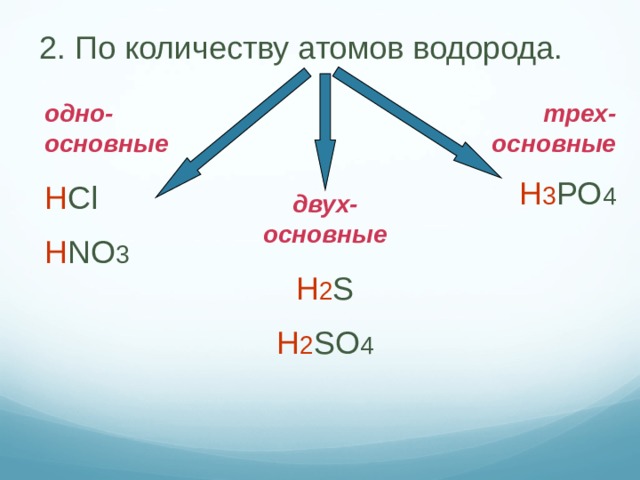
2. По количеству атомов водорода.
одно-основные
трех-основные
H Cl
H NO 3
H 3 PO 4
двух-основные
H 2 S
H 2 SO 4

3. По происхождению.
ОРГАНИЧЕСКИЕ:
ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ, ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ.

НЕОРГАНИЧЕСКИЕ:
СЕРНАЯ, СОЛЯНАЯ, ПЛАВИКОВАЯ, ФОСФОРНАЯ, АЗОТНАЯ.

СТАНЦИЯ ИСТОРИЧЕСКАЯ
Благодаря работам
выдающегося шведского
химика Карла
Вильгельма Шееле к
концу XVIII в
стало известно около
десяти различных
органических кислот.
Он выделил и описал
лимонную, молочную,
щавелевую и другие кислоты..

Молочная кислота
Была открыта в 1780г. К. Шееле.
Она содержится в квашеной капусте, соленых огурцах, образуется при созревании сыра.
Молочная кислота – консервант, т. е. ее добавка предохраняет продукты от порчи.
- Была открыта в 1780г. К. Шееле. Она содержится в квашеной капусте, соленых огурцах, образуется при созревании сыра. Молочная кислота – консервант, т. е. ее добавка предохраняет продукты от порчи.

- содержится не
только в лимонах, но и в
землянике, смородине,
ананасах и других
фруктах.
Чаще всего ее
используют в кондитерских
изделиях и напитках.
Для выведения пятен от
чернил и ржавчины на
белье.


СТАНЦИЯ “ СТОЙ! КРАСНЫЙ СВЕТ ! ”
ОСТОРОЖНО!
КИСЛОТЫ РАЗРУШАЮТ КОЖУ , ТКАНИ , ДРЕВЕСИНУ!
Запомни!
«Сначала вода затем кислота»

Первая помощь при ожоге едкими кислотами:
- Удалить вещество с поверхности кожи.
- Обильно промыть водой.
- Промыть 2% раствором пищевой соды.
- Наложить повязку из раствора фурацилина.

Как можно распознать кислоты?
“ Ни одна наука не нуждается в эксперименте в такой степени как химия. Ее основные законы, теории и выводы опираются на факты, поэтому постоянный контроль опытом необходим”.
Слова М. Фарадея .
Проведем эксперимент: Исследование окраски индикаторов в кислотных средах, соблюдая технику безопасности.

Станция индикаторная
Запомни!
УНИВЕРСАЛЬНАЯ ИНДИКАТОРНАЯ БУМАГА (ЛАКМУСОВАЯ БУМАГА)
НЕЙТРАЛЬНАЯ СРЕДА
МЕТИЛОВЫЙ ОРАНЖЕВЫЙ
КИСЛОТНАЯ СРЕДА
ФЕНОЛФТАЛЕИН
Помни! Нерастворимые кислоты не меняют окраску индикаторов.

Станция Практическая
Кислоты применяются в медицине.
Аскорбиновая, фолиевая,
Липоевая, ацетилсалициловая
и другие.

Кислоты применяются в кулинарии.
Уксусная и лимонная
кислоты.

Задание А)
Дан «текст»,
в котором «спрятаны» формулы кислот.
Подчеркните и назовите их.
H 2 OSOHBrNa 2 CO 3 MgBaH 2 CO 3 SO 4 KOH
H 3 PO 4 P 2 O 5 CaH 2 SHPH 3 NO 2 CS 2 NH 3 CO 3
HClBaSHKSHH 2 NaOH 2 SiO 3 NaClH 2 SO 4

Проверь задание А - у своего соседа по парте:
H 2 OSO HBr Na 2 CO 3 MgBa H 2 CO 3 SO 4 KOH
H 3 PO 4 P 2 O 5 Ca H 2 S HPH 3 NO 2 CS 2 NH 3 CO 3
HCl BaSHKSHH 2 NaO H 2 SiO 3 NaCl H 2 SO 4

Задание Б)
« Третий лишний»
Укажите кислоту, которая не соответствует признаку, объединяющему две другие.
Назовите кислоты.
а) H 2 S б) H 2 SO 4 в) HNO 3 HNO 3 H 3 PO 4 HF H 3 PO 4 H 2 CO 3 HBr
H 2 S H 3 PO 4 HNO 3

Задание В)
Пользуясь нижеприведенной таблицей,
распределите по классам следующие соединения:
NO 2 , Ba(OH) 2 , HBr , SO 2 , Mn(OH) 2 , HNO 3 ,
Zn(OH) 2 , MgO, Fe 2 O 3 , CuO, H 2 CO 3 , KOH,
H 2 SO 4 , Fe(OH) 3 , H 3 PO 4
Оксиды
Основания
Кислоты

Проверь задание В:
Оксиды
Основания
NO 2
Кислоты
SO 2
MgO
Fe 2 O 3
CuO
Ba(OH) 2
Mn(OH) 2
Fe(OH) 3
KOH
Zn(OH) 2
HNO 3
H 2 CO 3
H 2 SO 4
HBr
H 3 PO 4

Самостоятельно сделайте вывод, достигли ли вы учебной цели?
- Какие новые понятия вы узнали на уроке?
- Что вызвало больший интерес?
- Чему научились ?
- Что на уроке понравилось ?
- Что не понравилось? Почему?
- Охарактеризуйте урок одним словом. Урок был _________________________

Домашнее задание:
Выучить все новые понятия, формулы и названия кислот. Подготовиться к химическому диктанту .




















































