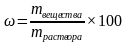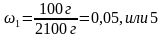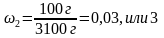Конспект урока по теме «Растворы. Растворение»
Цель урока: учащиеся должны усвоить понятие раствор, изучить типы растворов, факторы, влияющие на растворимость веществ в воде.
Воспитательные задачи:
научить учащихся устанавливать причинно-следственные связи в процессе изучения типов растворов;
воспитывать сосредоточенность, внимательность на уроке.
Образовательные задачи:
учащиеся должны изучить типы растворов, факторы, влияющие на растворимость веществ в воде;
учащиеся должны изучить понятия раствор, растворение, гидраты, кристаллогидраты;
в процессе объяснения темы учащиеся должны закрепить навыки вести наблюдение за ходом эксперимента и на его основе делать соответствующие выводы.
Развивающие задачи:
развивать познавательный интерес учащихся к предмету при изучении типов растворов;
развивать у учащихся умение рассуждать и делать выводы;
развивать логическое мышление путем сравнения, обобщения, анализа.
Тип урока: изучение нового материала
Оборудование и материалы:
компьютер, проектор, мультимедийная презентация;
таблица растворимости кислот, оснований, солей в воде
вода, песок, соли NaCl, 5 стаканчиков, стеклянная палочка, медный купорос CuSO4.5H2O, спиртовка, спички.
План урока
Организационный момент;
Изучение нового материала;
Закрепление знаний;
Подведение итогов, д/з.
Ход урока
Организационный момент
Учитель проверяет готовность учащихся к уроку, организует начало урока. Отмечает отсутствующих. Оглашает кратко цели и ход урока.
II. Изучение нового материала
Учитель: Ребята, вспомните, что изучает химия? (вещества)
В каком виде могут встречаться вещества в природе? (смеси, сплавы, минералы, растворы)
Слайд 1
Запишите тему урока: Растворение. Типы растворов
Учитель: Растворы играют важную роль в природе, технике и науке.
Где используются растворы? (ответы учащихся)
Учитель: Велика роль растворов в возникновении и развитии жизни на Земле. Одной из теорий возникновения организмов является теория зарождения жизни в первичном океане, который представлял собой воду с растворенными в ней веществами. Из этого раствора организмы получали необходимые для роста и развития ионы и молекулы.
В организме человека находятся физиологически важные растворы. Какие? (кровь, желудочный сок и др.)
Различные процессы, происходящие в организме, протекают в растворах. Например, усвоение пищи связано с переводом питательных веществ в раствор.
В природе водные растворы участвуют в процессах почвообразования и снабжают растения питательными веществами.
В технике такие процессы, как получение соды, удобрений, бумаги, также протекают в растворах.
Так как растворы играют важную роль в жизни человека, изучение их свойств очень важно.
Что такое раствор и процесс растворения?
Существует несколько теорий растворов.
1. Теории растворов
Слайд 2 (а)

Представители физической теории растворов развивали такие ученые как Я.Х.Вант-Гофф, С.Аррениус, В.Оствальд. Они считали, что процесс растворения является результатом диффузии, т.е. проникновения растворенного вещества в промежутки между молекулами воды.
Слайд 2 (б)
Сторонники химической теории, Д.И.Менделеев, И.А.Каблуков, доказывали, что растворение – это результат химического взаимодействия растворенного вещества с молекулами воды.
Слайд 2 (в)
Доказательством химического взаимодействия служат такие признаки химических реакций как выделение или поглощение тепла при растворении.
Например, растворение серной кислоты в воде протекает с выделением большого количества тепла и раствор может закипеть.
Какое правило нужно соблюдать при смешивании раствора серной кислоты и воды?
Сначала вода, потом кислота,
Иначе случиться большая беда!
Растворение же такого вещества как нитрата калия, сопровождается, наоборот, поглощением тепла.
В результате химического взаимодействия образуются соединения гидраты – непрочные соединения веществ с водой, существующие в растворе.
Косвенным доказательством гидратации является существование твердых кристаллогидратов.
Кристаллогидраты – соли и другие твердые вещества, в состав которых входит вода.
В этом случае вода называется кристаллизационной.
Слайд 3
К кристаллогидратам относится хорошо известная всем соль голубого цвета – медный купорос CuSO4 . 5H2O
Проделаем эксперимент
Насыпем небольшое количество медного купороса в пробирку. Отметьте цвет вещества. (ярко синий) Нагреем. Что наблюдаете? (вещество стало светло серого цвета). В чем причина изменения цвета? (отщепилась вода)
Растворим в стаканчике с водой небольшое количество сухого сульфата меди (II). Что наблюдаете? (раствор окрасился в синий цвет)
Изменение цвета сульфата меди (II) при растворении его в воде на синий является еще одним доказательством химической теории растворов.
Слайд 4

В настоящее время принята теория, объединяющая обе точки зрения – физико-химическая теория
Слайд 5
Растворение – физико-химический процесс. Раствор – однородная система, состоящая из частиц растворенного вещества, растворителя и продуктов их взаимодействия.
От чего зависит растворимость веществ в воде?
2. Факторы, от которых зависит растворимость веществ
Проделаем эксперимент
В пробирку с раствором ацетата свинца прильем раствор йодида калия. Что наблюдаете? (выпал осадок ярко желтого цвета).
Нагреем пробирку с осадком йодида свинца. Что наблюдаете? (осадок растворился).
Поместим пробирку в холодную воду. Что наблюдаете? (осадок вновь выпал)
Какой вывод можно сделать? (растворимость твердых веществ с повышением температуры увеличивается)
Почему мы кладем сахар в горячий чай? (чтобы быстрее растворился)
Растворимость газов, напротив, с повышением температуры уменьшается. Поэтому воду можно почти полностью освободить от растворенных в ней газов кипячением.
Слайд 6 (а)

Проделаем эксперимент
В 3 стаканчика нальем воды и добавим в 1 – нитрат натрия, во 2 – сульфат кальция, в 3 – песок. Перемешаем. Что наблюдаете? (NaNO3 растворился, CaSO4 частично, песок не растворился)
Слайд 6 (б)
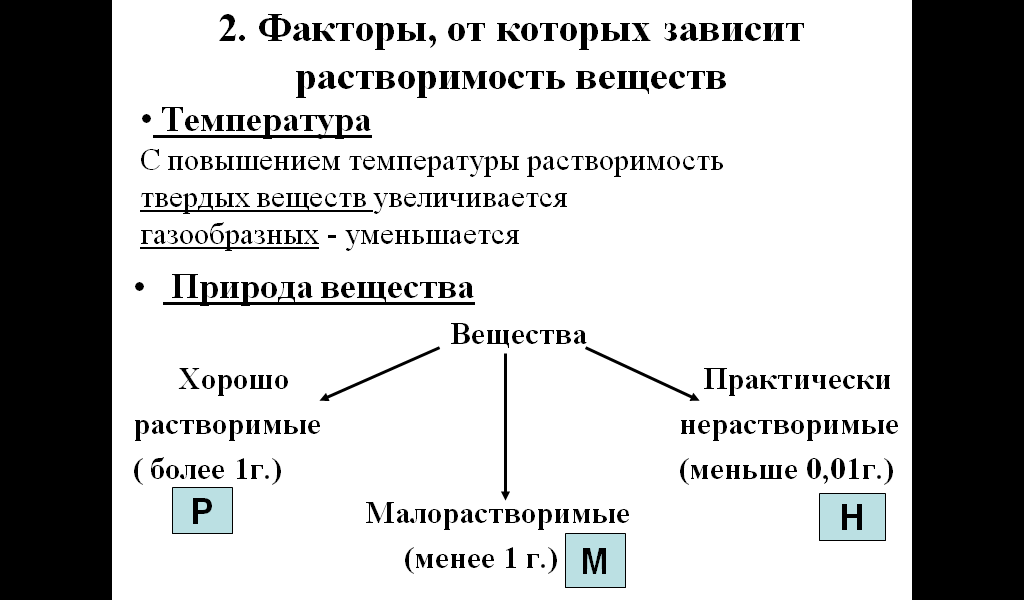
Посмотрите в таблицу растворимости и приведите примеры растворимых, малорастворимых и нерастворимых веществ. (ученики приводят примеры)
Из чего состоит раствор? (растворителя и растворенного вещества)
По содержанию растворенного вещества выделяют три типа растворов.
3. Типы растворов
Если растворить в данном объеме воды, например, соль при комнатной температуре, то раствориться может только определенное количество, сколько бы мы не перемешивали раствор с остатком нерастворившейся соли, больше соли не раствориться.
В этом случае говорят, что раствор насыщен этой солью при данной температуре.
Слайд 7 (а)

Какой образуется раствор, если же при этой температуре в данном объеме воды растворить немного меньшее количество соли? (ненасыщенный)
Слайд 7 (б)

При осторожном и медленном охлаждении насыщенного раствора возникает избыток растворенного вещества, если оно не выпадает в осадок, то образуется пересыщенный раствор.
Слайд 7 (в)

4. Концентрация растворов
На этикетках разнообразных растворов, используемых в быту, можно прочитать указания в них растворенного вещества. Например, уксусная кислота 70%, настойка йода 5%. Это один из способов выражения концентрации растворов, который называют массовой долей.
Как обозначают массовую долю вещества в растворе?
Слайд 8

Данная формула необходима для практического использования при приготовлении и работе с растворами.
Закрепление знаний
По рис. учебника ответьте на вопросы:
1. Какова растворимость хлорида калия при 30 0С? (40 г)
2. Какова растворимость сульфата калия при 80 0С? (20 г)
3. При какой температуре в 100 г воды может раствориться 60 г хлорида бария? (при 90 0С)
4. Растворимость какого вещества при 55 0С составляет 60 г на 100 г воды? (сульфата магния)
Решите задачу:
Для консервирования огурцов приготовили рассол: на 2 л воды взяли 100 г соли, а для консервирования томатов приготовили рассол из 100 г соли и 3 л воды. Какой рассол получится более концентрированным?
| Дано: V(H2O)2 = 2 л m (соли1) = 100 г V(H2O)2 = 3 л m (соли2) = 100 г
ω1 - ? ω2 - ? | Решение: Чтобы определить массовую долю вещества в растворе воспользуемся формулой 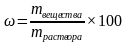 1. Найдем массу первого раствора m (р-ра1) = m (соли1) + m(H2O)1 = 100 г + 2000 г = 2100 г 2. Определим массовую долю растворенного вещества в первом растворе. 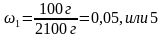 3. Найдем массу второго раствора m (р-ра2) = m (соли2) + m(H2O)2 = 100 г + 3000 г = 3100 г 4. Определим массовую долю растворенного вещества во втором растворе. 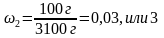 5. ω1 ˃ ω2, первый раствор более концентрированный. Ответ: рассол для консервирования огурцов более концентрированный. |
Определите массу соли и массу воды в 750 кг медного купороса.
Подведение итогов, д/з
Домашнее задание § 17
5