Урок химии в 8 классе
Урок №____________
Дата:_______________
Тема: «Закон Авогадро. Молярный объём газов»
Цель: сформировать понятие «молярный объем газов», раскрыть суть закона Авогадро, научить решать расчетные задачи.
Задачи:
образовательная: научить вычислять молярный объем газа по известной массе, количеству вещества;
развивающая: уметь применять и преобразовывать схемы для решения учебной задачи;
воспитательная: воспитывать интерес к химии как науке через связь с жизнью.
Тип урока: урок изучения нового.
Методы: объяснительно-иллюстративный, частично-поисковый, репродуктивный
Оборудование: периодическая система химических элементов Д.И. Менделеева, куб со стороной ≈ 28 см., варианты тестовых заданий, таблица с зданием.
Ход урока:
"Знание только тогда знание,
когда оно приобретено усилиями
своей мысли, а не памятью"
Л.Н.Толстой
Организационный этап.
Повторение пройденного материала (выполнение тестовой работы, Приложение 1).
Мотивация учебной деятельности.
В 1811 году известным итальянским ученым был сформулирован закон – очень важный для развития химии как науки. Сейчас этот закон носит его имя. Попробуйте определить фамилию ученого, используя подсказки:
1. Его именем назван кратер на Луне.
2. Этот химик впервые ввел понятие про молекулу как наименьшую частицу вещества, способную к самостоятельному существованию.
3. Его именем названа постоянная, которая показывает число структурных частиц в 1 моль вещества и она равна 6,02*1023.
Да, действительно, речь идет об Амедео Авогадро. Несмотря на значимость его вклада в науку и всемирную известность, ученый вел достаточно скромный образ жизни, был многодетным отцом и глубоко верующим человеком. В отличие от многих значимых в обществе персон, он презирал роскошь, богатство, славу. Возможно, именно в связи с такой нелюбовью ко всему светскому детали его биографии до сих пор остаются неизвестными — несоразмерно его вкладу в науку и развитие цивилизации.
Во многом именно благодаря открытиям Амедео Авогадро химия и физика достигли современного уровня развития. Сделанные им выводы известны всему миру и внесены в основы естественных наук. В то время как о жизни такого значимого человека известно мало. Вероятно, причиной этому стали особенности его характера и мировоззрения.
Стоит отметить, что при жизни значительная часть достижений итальянца какое-то время оставалась недооцененной. Вот и его стройная гипотеза была опровергнута другим известным ученым, обладавшим непревзойденным авторитетом в науке – Я. Берцелиусом, как не соответствующая экспериментальным данным.
Изучение нового материала.
На доске написано незаконченное предложение
«В … объемах … газов при одинаковых условиях (температуре и давлении) содержится … число молекул».
Итак, тема сегодняшнего урока «Закон Авогадро. Молярный объём газов».
Определение целей урока – за отведенное нам на урок время восстановить историческую несправедливость, вновь открыв закон Авогадро.
Мы уже говорили с вами о том, что в 1808 году французский ученый Ж.Л. Гей-Люссак сформулировал закон объемных отношений, согласно которому объёмы вступающих в реакцию и образующихся в результате реакции газов соотносятся как небольшие целые числа, которые совпадают с коэффициентами в уравнении реакции. Например:
N2 + 3H2 = 2NH3
1V 3V 2V
1 объем азота взаимодействует с 3 объемами водорода и образуется 2 объема аммиака.
Дети анализируют следующее уравнение реакции:
H2 + Cl2 = 2HCl
Вспомните, пожалуйста, что в уравнении реакции нам показывает количество вещества реагентов и продуктов? (Коэффициенты). Т.е. соотношение количества вещества нам показывают коэффициенты.
А сейчас давайте проанализируем два процесса (учитель вместе с обучающимися заполняют таблицы):
| N2 + O2 = 2NO |
| V | 1 | 1 | 2 |
| n | 1 | 1 | 2 |
| NA | 6,02*1023 | 6,02*1023 | 12,04*1023 |
| 2NO + O2 = 2NO2 |
| V | 2 | 1 | 2 |
| n | 2 | 1 | 2 |
| NA | 12,04*1023 | 6,02*1023 | 12,04*1023 |
Скажите, какие объемы кислорода и азота вступают в реакцию? (по 1V)
А каково соотношение количества вещества этих газов? (по 1 моль)
Сколько частиц содержится в 1 моль вещества? (6,02*1023)
А эти газы одинаковые? (нет, газы разные)
А какие объемы оксида азота (II) и оксида азота (IV) вступают в реакцию? (по 2V)
А чему равно их количество вещества по уравнению 2? (2 моль)
Сколько молекул каждого из газов содержится в 2 моль оксидов? (12,04*1023)
А газы одинаковые? (нет, газы разные)
Заполните пропуски во фразе, написанной на доске:
«В равных объемах разных газов при одинаковых условиях – (температуре и давлении) содержится одинаковое число молекул».
Поздравляю! Вы сформулировали закон Авогадро. Трудно представить, что такая стройная гипотеза была опровергнута научным миром.
Из рассмотренных уравнений видно, что коэффициенты химических реакций совпадают с количеством вещества и с объемами газообразных веществ.
Из закона Авогадро вытекает два следствия:
Один моль любого газа при одинаковых условиях занимает один и тот же объем.
При нормальных условиях (н.у.), т.е. при температуре 273 К (0 градусов Цельсия) и давлении 101,3 кПа (1 атм.), 1 моль любого газа занимает объем, равный 22,4 л. Этот объем называют молярным объемом.
Т.о., объем 1 моль газообразного вещества называют молярным объемом.
Он обозначается Vm и измеряется в л/моль. Он был экспериментально измерен и равен 22,4 л/моль
Vm = 22,4 л/моль
Молярный объем можно рассчитать по формуле:
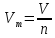
Откуда, 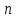
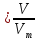 ; V=п
; V=п Vт
Vт
При постоянном давлении и температуре плотность газа определяется только его молярной массой.
О втором следствии из закона мы поговорим с вами более подробно на следующем уроке. А сегодня мы остановимся на следствии №1, которое показывает нам зависимость количества вещества от объема.
Обобщение и систематизация знаний.
Практическое усвоение материала (решение задач на применение формул):
Рассчитайте объем 1,5 моль кислорода.
Рассчитайте объем 16 г. кислорода.
Рассчитайте объем 24,08 *1023 кислорода.
Какое количество вещества составляют 2,8л. углекислого газа?
Самостоятельная работа. Заполнить таблицу:
| Формула | m | n | V | N | M |
| NH3 | 68г. |
|
|
|
|
| Cl2 |
|
| 44,8л. |
|
|
| O3 | 144г. |
|
|
|
|
| O2 |
| 4 моль |
|
|
|
| CO2 |
|
|
| 9,03*1023 |
|
Дети заполняют только две строчки. Все расчеты полностью оформляются в тетради. Учитель консультирует обучающихся по возникающим вопросам.
Рефлексия, выставление отметок.
Прием «Комплимент».
Комплимент-похвала, комплимент деловым качествам, комплимент в чувствах, в котором учащиеся оценивают вклад друг друга в урок и благодарят друг друга и учителя за проведенный урок.
Домашнее задание: Изучить параграф 38, выучить формулировку закона и следствия из него; заполнить оставшиеся три строчки таблицы.
Тестовая работа
Вариант 1
Количество вещества:
А) величина, которая показывает массу 1 моль вещества;
Б) величина, равная отношению массы вещества к его солярной массе;
В) масса вещества;
Г) физическая величина, которая показывает число структурных частиц и имеет размерность «моль».
Число 6,02*1023 является постоянной:
А) Планка; Б) Авогадро;
В) Гей-Люссака; В) Лавуазье
3. Какую массу имеют 3 моль Н2?
А) 3г.; Б) 6 г;
В) 4 г; Г) 2 г
4. Молярная масса - это физическая
величина, которая определяется по
формуле:
А) M = n/m Б) M = n * m
В)M = m/n
5. Молярная масса вещества – это:
А) относительная атомная масса;
Б) относительная молекулярная масса;
В) масса одной молекулы вещества;
Г) масса одного моля вещества.
6. Молярная масса О3
А) 16г/моль;
Б) 32 г/моль;
В) 48 г/моль;
Г) 8 г/моль.
-
-
Приложение 1
Тестовая работа
Вариант 2
Термин «моль» ввел в химию:
А) Ж. Пруст; Б) А. Авогадро;
В) В. Оствальд; Г) И. Кант
2. Молярная масса численно равна:
А) относительной молекулярной массе;
Б) относительной атомной массе;
В) количеству вещества;
Г) массе молекулы.
3. Количество вещества обозначается символом:
А) m;
Б) n;
В) NA;
Г) N.
4. Единица измерения молярной массы:
А) л / моль; В) л / г;
Б) моль / г; Г) г / моль.
5. Определите количество вещества Н2, в котором содержится 18,06 · 1023 молекул:
А) 0,2 моль; Б) 3 моль;
В) 0,3 моль; Г) 1 моль.
6. Определите число молекул кислорода, содержащихся в 2 моль О2
А) 1,204 · 1023;
Б) 6,02 · 1023;
В) 12,04 · 1023;
Г) 0,602 · 1023.
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Формула | m | n | V | N | M |
NH3 | 68г. | -
| -
| -
| -
|
Cl2 | -
| -
| 44,8л. | -
| -
|
O3 | 144г. | -
| -
| -
| -
|
O2 | -
| 4 моль | -
| -
| -
|
CO2 | -
| -
| -
| 9,03*1023 | -
|
-
-
Формула | m | n | V | N | M |
NH3 | 68г. | -
| -
| -
| -
|
Cl2 | -
| -
| 44,8л. | -
| -
|
O3 | 144г. | -
| -
| -
| -
|
O2 | -
| 4 моль | -
| -
| -
|
CO2 | -
| -
| -
| 9,03*1023 | -
|
-
Формула | m | n | V | N | M |
NH3 | 68г. | -
| -
| -
| -
|
Cl2 | -
| -
| 44,8л. | -
| -
|
O3 | 144г. | -
| -
| -
| -
|
O2 | -
| 4 моль | -
| -
| -
|
CO2 | -
| -
| -
| 9,03*1023 | -
|
-
-
Формула | m | n | V | N | M |
NH3 | 68г. | -
| -
| -
| -
|
Cl2 | -
| -
| 44,8л. | -
| -
|
O3 | 144г. | -
| -
| -
| -
|
O2 | -
| 4 моль | -
| -
| -
|
CO2 | -
| -
| -
| 9,03*1023 | -
|
-
-
Формула | m | n | V | N | M |
NH3 | 68г. | -
| -
| -
| -
|
Cl2 | -
| -
| 44,8л. | -
| -
|
O3 | 144г. | -
| -
| -
| -
|
O2 | -
| 4 моль | -
| -
| -
|
CO2 | -
| -
| -
| 9,03*1023 | -
|
-
-
Формула | m | n | V | N | M |
NH3 | 68г. | -
| -
| -
| -
|
Cl2 | -
| -
| 44,8л. | -
| -
|
O3 | 144г. | -
| -
| -
| -
|
O2 | -
| 4 моль | -
| -
| -
|
CO2 | -
| -
| -
| 9,03*1023 | -
|
-






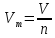
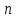
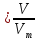 ; V=п
; V=п Vт
Vт









