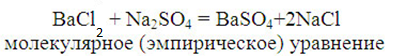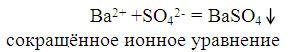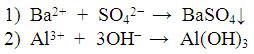Ход урока
1. Организационный момент
Учитель: Приветствие. Проверка готовности учащихся к уроку.
2. Стадия вызова
2.1. Актуализация опорных знаний учащихся, проверка знаний учащихся прошлого материала
Фронтальный опрос по определениям:
Какие вещества называются электролитами и неэлектролитами?
Какие вещества к ним относятся?
С образованием каких ионов диссоциируют растворы кислот, солей и щелочей?
Какие основания называются щелочами?
Задание №1: Выпишите формулы веществ ,составляющих выигрышный путь, как в игре “крестики-нолики”, где три вещества являются: 1 вариант - электролитами, 2 вариант - неэлектролитами.
| C2H5OH
(этиловый спирт) | CO2 | C12H22O11
(сахароза) раствор |
| NaNO3
(кристал) | AgCL | SiO2 |
| HNO3 (раствор) | Na2SO4
(раствор) | KOH
(раствор) |
2.2. Мотивация учебной деятельности учащихся
Создание проблемной ситуации:
Учитель: Проведём два эксперимента (демонстрационный опыт), в которых попарно взаимодействуют бесцветные вещества.
Опыт №1. Смешивает - хлорид бария и сульфат натрия (кристаллические) и их растворы.
Учитель:
Почему в первом случае реакция не протекает, а во втором – наблюдаем выпадение осадка?
Что происходит с веществом при растворении их в воде? Какова роль воды?
Какое вещество выпало в осадок?
Опыт №2. Смешиваем кристаллические хлорид натрия и сульфат калия. Добавляем воду к кристаллическим веществам.
Формулировка проблемного вопроса:
Почему же в случае с хлоридом бария и сульфатом натрия реакция протекает в растворе, а в случае с сульфатом калия и хлоридом натрия не наблюдаем признаков протекания реакции, реакция не протекает ни в одном растворе, ни при смешивании кристаллических веществ.
3. Стадия осмысления
3.1. Постановка учебной задачи и цели урока
Учитель: Сегодня нам и предстоит выяснить:
Что может происходить в растворе между ионами?
Какие взаимодействия между ними возможны?
Отвечая на проблемный вопрос (опираясь на знания о реакциях обмена и условиях их протекания до конца, а также электролитической диссоциации кислот, солей, оснований при растворении в воде), нам предстоит научиться:
определять и объяснять произойдет химическая реакция или нет, т.е. пройдет ли она до конца;
раскрывать сущность химических реакций с позиции теории электролитической диссоциации,
записывать уравнения в трех видах: молекулярном, полном и сокращенном ионном; пользоваться алгоритмом, памяткой и таблицей растворимости;
3.2. Изучение нового материала.
Учитель: Запишите тему урока: “Ионные уравнения реакций”
Федя снял аккумулятор с "Жигуля":
Напряжение упало до нуля.
Феде посоветовал Андрей:
"Ты электролит туда залей!"
Федор взял на кухне соли:
Он учил когда-то в школе,
Что любой электролит,
Если он водой залит,
Распадается на ионы.
Этих ионов - миллионы!..
Соль - она электролит.
Вот готов раствора литр.
Федор взял аккумулятор…
Догадайтесь-ка, ребята:
Что сказал ему отец?
Тут истории конец.
- Каждое химическое свойство, проявляемое сильными электролитами в растворах, - это свойство ионов, на которые электролит распался: либо катионов, либо анионов. Между тем, реакции обмена между электролитами в водных растворах мы раньше изображали молекулярными уравнениями, не учитывая, что в этих реакциях участвуют не молекулы электролита, а ионы, на которые он диссоциирован.
BaCl2+Na2SO4= BaSO4+2NaCl
K2SO4+NaCl= KCl+Na2SO4
Определите тип химической реакции?
Вспомните, какие реакции называются реакциями обмена?
В каких случаях возможно протекание данных реакций? (В первой реакции обмена в осадок выпадает нерастворимый сульфат бария, а во второй все вещества растворимые и поэтому протекать данная реакция не может.)
Учитель: Следовательно, не всегда при сливании попарно растворов солей можно говорить о протекании реакции обмена. Попробуем разобраться, какими составными частями обмениваются сложные вещества в свете представлений теории электролитической диссоциации (ТЭД).
Опыт
Давайте с Вами попробуем разобраться – в каких случаях реакции проходят до конца, а в каких- нет. Для этого используем опыт
Но только повторим правила техники безопасности
Вспомним правила ТБ по работе с химическими веществами.
В XIX веке жил знаменитый ученый-химик Карл Либих. Его коллега (тоже химик) Карл Фогт вспоминает один такой случай… как-то входит Либих, а у него в руке склянка с притертой пробкой. Он подходит к Фогту и говорит: «Ну-ка, обнажите свою руку», - и влажной пробкой прикасается к руке Фогта и спрашивает: «Жжет, не правда ли?» Я только что получил муравьиную кислоту.
Правильно ли поступил Карл Либих?
Конечно же нет. У Фогта после этого долго болела рука и остался шрам.
А вы знаете, как надо обращаться с реактивами?
Перед каждым из вас на столе лежит инструкционная карта. По ходу выполнения опытов заполните ее, пожалуйста!
Слайд - правило
Реакции протекает в растворе, где вещества находятся в виде ионов, а не молекул. И правильнее записывать уравнения реакций не только в молекулярном виде (взаимодействие молекул), но и в ионном виде, где отражается взаимодействия между реально существующими частицами в растворах солей, оснований и кислот.
Итак, запишем определение - реакции между ионами – ионными реакциями, а уравнения таких реакций - ионными уравнениями.
Составить ионное уравнение достаточно просто. Надо только запомнить, что в ионном виде в уравнении реакции представляют только сильные электролиты.
- Разбор алгоритма составления ионных реакций (таблица выведена на экран, на каждую парту раздается алгоритм составления ионных уравнений и лист с правилами составления ионных уравнений, по которым работают весь урок).
Правила составления ионных уравнений реакций
Сильные электролиты записывают в виде ионов.
Формулы слабых электролитов (в том числе и воды), нерастворимых и газообразных веществ записываются в молекулярной форме.
Если вещество выпадает в осадок, то рядом с его формулой ставят стрелку, направленную вниз; а если в ходе реакции выделяется газообразное вещество, то рядом с его формулой ставят стрелку, направленную вверх.
Сумма зарядов в левой части ионного уравнения равна сумме зарядов в правой части ионного уравнения
Учитель: Используя знания о диссоциации веществ, напишем уравнения, проведенных реакций в ионном виде. Сливая растворы BaCl2 и Na2SO4, мы наблюдаем образование осадка.
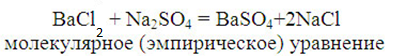
Чтобы записать полное ионное уравнение реакции необходимо пользоваться таблицей растворимости солей и оснований. И так, обе исходные соли – сильные электролиты, полностью диссоциирующие в воде, а вот BaSO4, – нерастворимое соединение, не диссоциирующее в воде, поэтому его переписываем в молекулярном виде. Итак, уравнение реакции между веществами можно записать так:

Что же произошло при сливании растворов? Видно, что в левой и правой частях ионного уравнения записаны одинаковые ионы. Эти ионы -ион натрия и хлорид-ионы - в реакции не участвовали, они остались такими, какими были до сливания растворов, следовательно, мы можем исключить их обозначение из левой и правой частей полного ионного уравнения. Что осталось? Ионы бария и сульфат- ионы - именно они принимают участие в образовании осадка, ионы соединились и образовали сульфат бария – осадок.
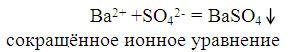
Это уравнение показывает, что суть данной реакции сводится к взаимодействию Ba2+ и SO42- , в результате которого образуется осадок BaSO4.
Данные ионы могли входить в состав любого растворимого электролита и наблюдалась бы аналогичная реакция.
По таблице растворимости выберите любые другие электролиты, содержащие ионы.
Учитель: Итак, полное ионное уравнение – это запись всех веществ в ионной форме с учетом коэффициентов, кроме веществ выпавших в осадок или газообразных
Сокращенное ионное уравнение – уравнение без указания ионов, которые не принимают участие. По результатам его видно, какие ионы образовали то, что нерастворимо или малорастворимо — газообразные продукты или реагенты, осадки или малодиссоциирующие вещества.
Мы с вами и ответили на проблемный вопрос, который поставили в начале урока?
Если слить растворы двух электролитов и между ними произойдет химическая реакция, то это будет взаимодействие определенных ионов.
4. Контроль и самопроверка знаний
Учитель: Реакции ионного обмена широко используются в практических целях, например, для осаждения ионов, приносящих существенный вред людям и животным. Предложите решение следующей задачи (задания и ответы высвечиваются на слайде).
Задача 1. Предложите ионные реакции для очистки сточных вод автотранспортного предприятия от катионов Pb2+ и Cu2+, оказывающих токсическое действие на живые организмы.
Задача 2. “Меткий стрелок”. Выпишите ионы, которые попадут в цель.
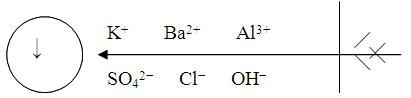
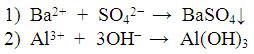
5. Подведение итогов урока. Рефлексия
Итак, давайте подведём итоги нашего урока, достигнуты ли наши цели урока, оценим результаты своей работы.
Обсуждение, формулировка результатов урока:
Научились проводить реакции ионного обмена и рассмотрели реакции, протекающие в растворах электролитов с образованием осадка, газа или малодиссоциирующего вещества.
Узнали, что реакции в растворах электролитов сводятся к реакциям между ионами.
Сокращенные ионные уравнения показывают сущность процесса, протекающего между растворами электролитов.
1) Задача (обязательное): С какими веществами может реагировать фосфорная кислота, образуя а) газ; б) воду; в) осадок? Запишите уравнения реакций в молекулярном, полном и сокращённом ионном видах.
Выводы:
Если выделит ГАЗ - Это раз;
И получится ВОДА - Это два;
А ещё нерастворимый
Осаждается продукт…
«Есть ОСАДОК», - говорим мы...
Это третий важный пункт,
Химик «правила обмена»
Не забудет никогда:
В результате – непременно
Будет ГА3 или ВОДА,
Выпадет ОСАДОК – Вот тогда порядок!!!
Молодцы ребята вы смогли превратить наш урок в научную лабораторию.
Мы прошли с вами все этапы научного познания всего лишь на одном уроке.
Анализ урока:
Тип урока: комбинированный.
Технология построения урока: изучение нового материала, первичное закрепление.
Вид урока: объяснительно-иллюстративный с элементами проблемного обучения.
Цель урока: показать суть химических реакций, протекающих в растворах и научить учащихся составлять ионные уравнения реакций.
Задачи.
Дидактические:
на основе усвоенных понятий о реакциях обмена и электролитической диссоциации веществ разных классов развить понятие “реакции ионного обмена”, сформировать у учащихся представление о сущности реакций ионного обмена; закрепить понятие “реакции нейтрализации”;
научить школьников применять знания о диссоциации кислот, оснований, солей при написании ионных уравнений реакций;
научить составлять эмпирические, полные и сокращённые ионные уравнения; по сокращённому ионному уравнению определять продукты реакции;
экспериментально доказать, что реакции в растворах электролитов являются реакциями между ионами; выявить условия, при которых они идут практически до конца;
дать первоначальные представления о качественных реакциях.
Развивающие:
развивать положительные мотивы учебно-познавательной деятельности, интерес к предмету, творческую инициативу и активность;
совершенствовать учебные умения школьников при составлении химических уравнений, при выполнении лабораторных опытов; развивать умение соблюдать правила техники безопасности при работе в химическом кабинете;
продолжить формирование химической речи учащихся, творческого мышления, правил научного общения, умение наблюдать за происходящим опытом и на основе наблюдений, делать аргументированные выводы, прогнозировать результат деятельности;
продолжить развивать общеучебные умения и навыки, логическое мышление, умение применять знания и собственный опыт в различных ситуациях, в том числе и проблемных: умение анализировать, делать вывод; умения работать самостоятельно и в группе.
Воспитательные:
содействовать воспитанию у учащихся организованности, аккуратности при проведении эксперимента, чувство ответственности, уверенности в себе, требовательности к себе; умения организовывать взаимопомощь при проведении групповой работы, духа соревновательности при выполнении упражнений; умения проводить самооценку.
Опорные знания: основные положения ТЭД, диссоциация кислот, щелочей, солей.
Основные понятия темы: реакции ионного обмена, ионные реакции, ионные уравнения, молекулярные (эмпирические) уравнения реакций, полные и сокращённые ионные уравнения реакций, реакции нейтрализации
Межпредметные связи: электропроводность веществ - связь с уроками физики. Составление ионных уравнений: связь с уроками математики.
Методы и приемы организации обучения:
Технологии (в т.ч. элементы): технология развития критического мышления.
Методы: репродуктивный, частично-поисковый, исследовательский.
Форма организации познавательной деятельности: фронтальная, парная, групповая.