Просмотр содержимого документа
«Реакции разложения»

Работу выполнила:
Васильева Е. В.

Цель урока: Изучить механизм реакций разложения. Познакомиться с понятиями «катализатор», «фермент». Отработать навыки составлять уравнения химических реакций.


Признак реакции – в нее вступает одно сложное вещество, а образуются два новых простых вещества.

Разложение воды электрическим током с помощью специальной установки – электролизера.
2 H 2 O = 2H 2 ↑ + O 2 ↑

Разложение пероксида водорода (перекись водорода):
2 H 2 O 2 = 2H 2 О + O 2 ↑
Если эту реакцию проводить с использованием оксида марганца ( IV ) – то эта реакция будет идти быстрее. Оксид марганца ( IV ) – катализатор этой реакции.

Катализатор – это вещество, изменяющее скорость химической реакции, но по окончании её остающееся качественно и количественно неизменным.
Биологические катализаторы называют ферментами .

Если подогреть на пламени спиртовки голубой студенистый осадок гидроксида меди ( II ), то содержимое пробирки почернеет из-за получившегося оксида меди ( II ):
Cu(OH) 2 = CuO + H 2 О

В промышленности разложение минерала известняка ( CaCO 3 ) используют для получения негашеной извести ( CaO ):
CaCO 3 = CaO + CO 2 ↑
Этот производственный процесс называют обжигом известняка .

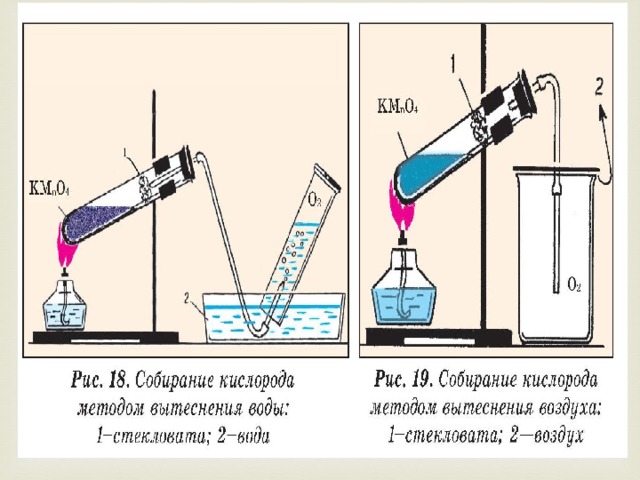
Разложение перманганата калия KMnO 4 , в быту называемого марганцовкой:
2 KMnO 4 = K 2 MnO 4 + MnO 2 + O 2 ↑
В данном случае в реакцию вступило одно сложное вещество, а образовалось три новых вещества.

Реакции разложения – это такие реакции, в результате которых из одного сложного вещества образуется два и более новых веществ.

Домашнее задание
§ 30, упр. 1, 2, 4, 5






























