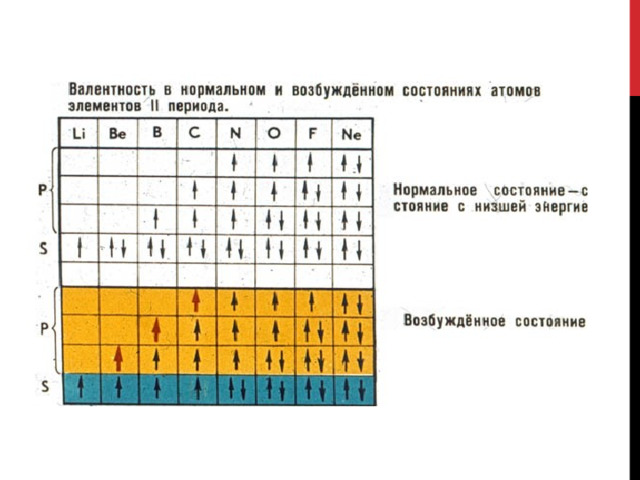
Современные представления о строении атома
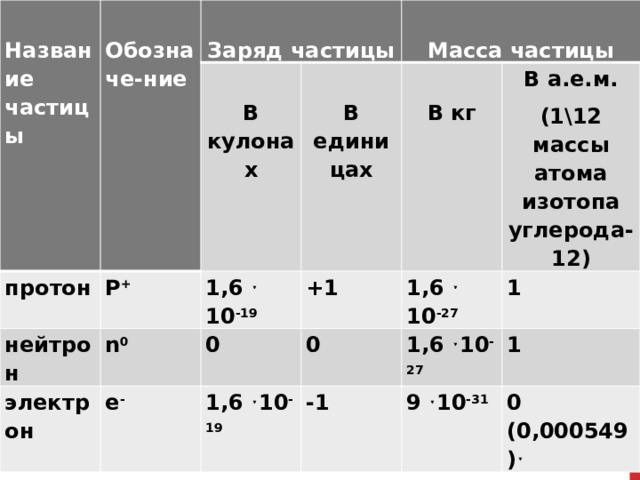
Название частицы
протон
Обозначе-ние
нейтрон
P +
Заряд частицы
электрон
n 0
В кулонах
1,6 ˑ 10 -19
+1
0
e -
Масса частицы
В единицах
1,6 ˑ 10 -19
В а.е.м.
В кг
1,6 ˑ 10 -27
0
-1
1
1,6 ˑ 10 -27
(1\12 массы атома изотопа углерода-12)
9 ˑ 10 -31
1
0 (0,000549) ˑ

Число протонов как и число электронов в атоме определяется порядковым номером элемента в периодической системе химических элементов . Число протонов определяет заряд ядра атома (обозначается Z). Количество нейтронов рассчитывается как разность между массовым числом атома и зарядом ядра (A-Z).
Совокупность атомов с определенным значением заряда ядра Z , массового числа A, называется нуклидом . Например: 37 Cl, 15 P.
Если атомы одного и того же элемента отличаются по массе, то они являются изотопами .
В атомах изотопов содержится разное количество нейтронов Например: 1 H , 2 H, 3 H – водород (H), дейтерий (D) и тритий (T).

Понятие об электронном облаке и s -,p -, d -, f- электронах
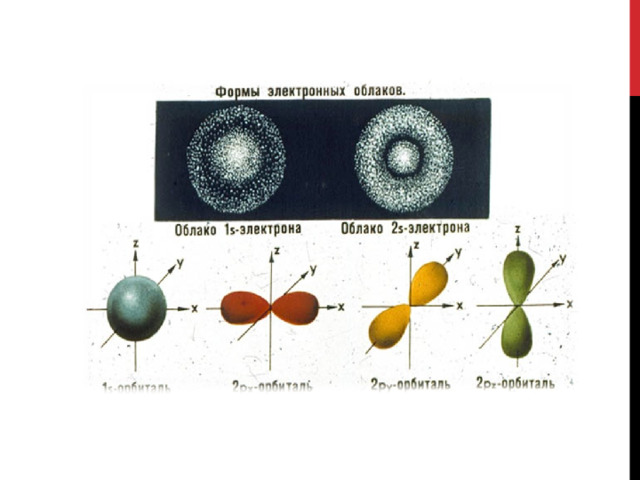
Область пространства вокруг ядра, где наиболее вероятно нахождение электрона, называют атомной орбиталью. Атомные орбитали имеют различные формы, размеры и ориентацию в пространстве.

Состояние электронов в пространстве описывают с помощью четырех квантовых чисел.
Главное квантовое число n – соответствует номеру энергетического уровня, на котором расположен электрон. (Количество энергетических уровней в атоме соответствует номеру периода, в котором расположен элемент.). Энергетический уровень – это совокупность энергетических состояний электрона в атоме, характеризующихся одним и тем же значением квантового числа n. Максимальное число электронов на каждом энергетическом уровне равно 2n 2 . Главное квантовое число принимает значения из множества натуральных чисел.

Орбитальное квантовое число l – определяет форму атомной орбитали. Принимает значения: для s- орбитали= 0, для p-орбитали=1, для d =2, а для f =3 Орбитальное квантовое число принимает значения (n-l).
Совокупность орбиталей одной формы (с одинаковым значением орбитального квантового числа) на данном энергетическом уровне образует энергетический подуровень.
На основании математических расчетов определили, что электронные облака имеют следующую форму: s – орбиталь - форму сферы, р – орбиталь форму вытянутой восьмерки, формы d - и f - еще более сложные. На каждом энергетическом уровне (кроме первого) содержится несколько разных орбиталей. На первом уровне – одна - s. На втором - две- s и p . На третьем – три s,p,d. На четвертом – четыре s, p, d, f и т.д.
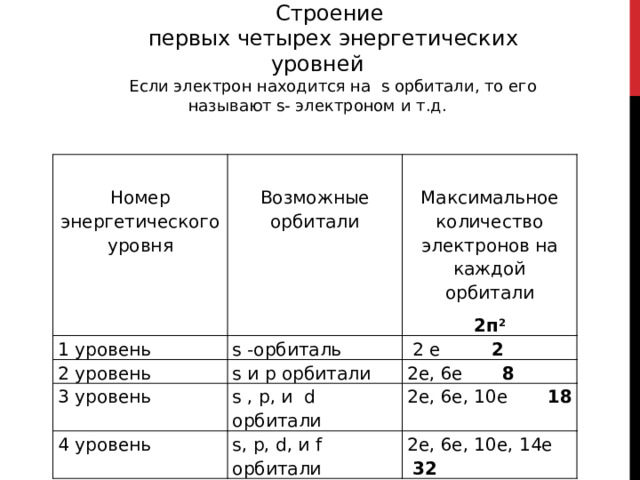
Строение
первых четырех энергетических уровней
Если электрон находится на s орбитали, то его называют s- электроном и т.д.
Номер энергетического уровня
1 уровень
Возможные орбитали
s -орбиталь
2 уровень
Максимальное количество электронов на каждой орбитали
s и p орбитали
3 уровень
2 е 2
2п 2
4 уровень
2е, 6е 8
s , p, и d орбитали
s, p, d, и f орбитали
2е, 6е, 10е 18
2е, 6е, 10е, 14е 32
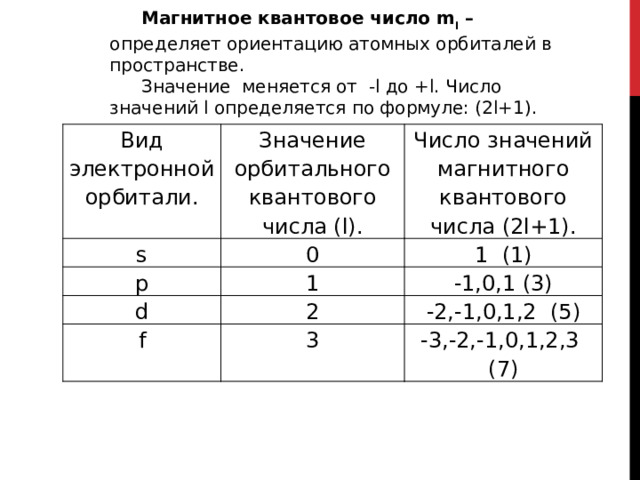
Магнитное квантовое число m l – определяет ориентацию атомных орбиталей в пространстве.
Значение меняется от -l до +l. Число значений l определяется по формуле: (2l+1).
Вид электронной орбитали.
Значение орбитального квантового числа (l).
s
0
p
Число значений магнитного квантового числа (2l+1).
1
1 (1)
d
2
f
-1,0,1 (3)
3
-2,-1,0,1,2 (5)
-3,-2,-1,0,1,2,3 (7)

Магнитное спиновое квантово число – m s - принимает два значения -1\2 и +1\2.
На каждой орбитали могут одновременно находиться не более двух электронов, они будут отличаться друг от друга значением спинового квантового числа.

Принцип заполнения электронами атомных орбиталей подчиняется запрету Паули: в атоме не может быть двух электронов с одинаковым значением всех четырех квантовых чисел, т.е. в атоме не может быть электронов, которые находились бы в одинаковом квантовом состоянии.
Правило Хунда : Наиболее устойчивым состоянием является такое, при котором будет максимально возможное число неспаренных электронов на каждом из подуровней.

Строение электронных оболочек описывают с помощью электронных формул, ее также называют электронной конфигурацией . Заполнение электронами электронных оболочек подчиняется правилу Хунда и правилу Клечковского .
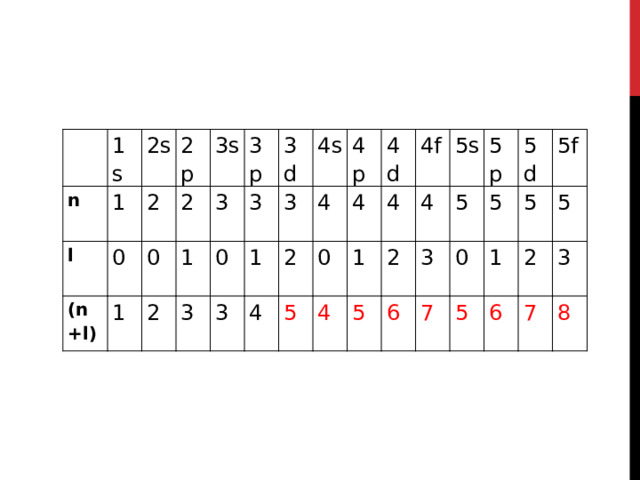
В соответствии с правилом Клечковского атомные орбитали заполняются электронами в порядке плавного возрастания суммы (n+l). При одинаковых значениях (n+l) сначала заполняются орбитали с наименьшим значением n.
1s
n
2s
1
l
0
2p
(n+l)
2
1
0
3s
2
1
3p
2
3
3
0
3d
3
1
4s
3
3
4p
4
4
2
4d
0
4
5
1
4f
4
4
5s
2
5
4
6
3
5
5p
0
5d
5
7
1
5f
5
5
2
5
6
3
7
8

Таким образом, электронная конфигурация будет иметь вид:
1s2s2p3s3p4s3d4p5s4d5p6s4f5d6p7s5f6d и т.д.
Примеры:
S 1s 2 2s 2 2p 6 3s 2 3 p 4 p – элемент (т.к. последней заполняемой орбиталью является p-орбиталь);
Ca 1s 2 2s 2 2p 6 3s 2 3p 6 4 s 2 s – элемент;
V 1s 2 2s 2 2p 6 3s 2 3p 6 4s 4 3 d 3 d – элемент;
Pr 1s 2 2s 2 2p 6 3s 2 3p 6 4s 4 3d 10 4p 6 5s 2 4d 10 5p 6 6s 2 4 f 3 5d 0 f - элемент

Радиус атома. Радиус атома – половина межъядерного расстояния в молекулах простых и сложных веществ в среднем достигают 10 -10 м. По периоду радиус атома немонотонно уменьшается . С увеличением заряда ядра атома число энергетических уровней остается постоянным. Т.о. электронная оболочка испытывает более сильное притяжение ядра, которое приводит к сжатию атома, т.е. уменьшению радиуса. В главных подгруппах радиус атома увеличивается. По мере увеличения номера периода происходит увеличение заполняющихся электронами уровней.

Основное и возбужденное состояние атома. Основное состояние атома – это то состояние, которое следует при составлении электронной конфигурации с учетом принципа минимума энергии, когда каждый электрон стремиться занять положение ближайшее к ядру. Для объяснения валентных возможностей атома элемента иногда прибегают к понятию возбужденного состояния атома. При этом происходит распаривание общих электронных пар, расположенных на валентном уровне и перевод электронов на другую валентную орбиталь. Пример обозначения состояния атома: основное возбужденное, C C *